Growth, age and mortality rate of the crown-of-thorns starfish, Acanthaster planci, in the southern gulf of California, Mexico, during an outbreak event (2017-2018)
Héctor Reyes-Bonilla a, Frida J. Sánchez-Luna b, c, Luis E. Calderón-Aguilera d, *, Jenny Carolina Rodríguez-Villalobos e, f y María Dinorah Herrero-Pérezrul e
a Universidad Autónoma de Baja California Sur, Departamento Académico de Biología Marina, Carretera al sur Km 5.5, Col. El Mezquitito, 23090 La Paz, Baja California Sur, México
b Ghent University, Faculty of Sciences, Krijgslaan 281/N60, 9000 Gent, Bélgica
c Università Politecnica delle Marche, Via, Dipartimento di Scienze della Vita e dell’Ambiente, Brecce Bianche, 60131 Ancona, Italia
d Centro de Investigación Científica y de Educación Superior de Ensenada, Baja California, Carretera Tijuana – Ensenada 3918, 22860 Ensenada, Baja California, México
e Centro Interdisciplinario de Ciencias Marinas, Instituto Politécnico Nacional, Av. Instituto Politécnico Nacional s/n, Col. Playa Palo de Santa Rita, 23096 La Paz, Baja California Sur, México
f Ecosistemas y Conservación (Proazul Terrestre, A.C.), calle Héroes de Independencia 2440, 23000 La Paz, Baja California Sur, México
*Autor de correspondencia: leca@cicese.mx (L.E. Calderón-Aguilera)
Recibido: 18 febrero 2025; aceptado: 22 octubre 2025
Resumen
El asteroideo Acanthaster planci es un importante coralívoro y se requiere investigar en detalle aspectos de su ecología poblacional. El objetivo del estudio fue estimar parámetros demográficos de A. planci en el archipiélago Espíritu Santo, golfo de California. Entre julio 2017 y octubre 2018 se midió el diámetro del disco de 356 especímenes y con base en análisis de frecuencia de tallas, se calculó el diámetro de disco máximo teórico, la tasa de crecimiento y mortalidad, y la longevidad de la población. El tamaño máximo del disco fue de 30.8 cm, la tasa de crecimiento de 0.429/año, la longevidad de 6 años y la tasa de mortalidad fue de 1.039/año. La edad de los individuos revisados en 2017 fluctuó entre 1.0 y 1.25 años, y en 2018 fue de 1.75 a 2.25 años, lo que sugiere que la cohorte de 2016 causó el notable aumento poblacional registrado para A. planci en 2017. Este evento pudo haber resultado de la combinación del alto reclutamiento larval favorecido por el agua cálida aportada por el evento de El Niño de 2015 y una alta sobrevivencia de juveniles debido a la presencia de abundante alimento algal como consecuencia de La Niña en 2016.
Palabras clave: Frecuencia de tallas; FISAT; Mortalidad; Crecimiento; Reclutamiento; Brote poblacional
Abstract
The asteroid Acanthaster planci is an important corallivore, and the investigation of some aspects of its population ecology are required. The objective of this study was to estimate demographic parameters of A. planci at Espíritu Santo Archipelago, Gulf of California. Between July 2017 and October 2018, the disk diameter of 356 specimens was measured, and with these data the theoretical maximum diameter, growth and mortality rates, and longevity of the population were estimated on the basis of size frequency analyses. The maximum disk size was 30.8 cm, growth rate was 0.429 yr-1, longevity was 6 years, and mortality rate was 1.039 yr-1. Age of the individuals assessed in 2017 fluctuated between 1.0 and 1.25 years, and in 2018 was from 1.75 to 2.25 years, which suggests that the 2016 cohort caused a noteworthy population to increase recorded for A. planci in 2017. This event may have resulted from the combination of high larval recruitment favored by the warm water brought by the 2015 El Niño, and high juvenile survival due to abundant algal food as consequence of La Niña in 2016.
Keywords: Length frequency; FISAT; Mortality; Growth; Recruitment; Outbreak
Introducción
La estrella corona de espinas (Acanthaster spp.) es uno de los equinodermos que ha sido más estudiado en arrecifes del Indo-Pacífico debido al interés que genera el incremento excesivo en la densidad de sus poblaciones. Cuando ésto ocurre, la intensidad de la depredación de la estrella sobre los corales supera las tasas de crecimiento de las colonias y el asteroideo se convierte en una de las mayores amenazas para los arrecifes coralinos (De’ath et al., 2012; Kayal et al., 2012; Pratchett et al., 2014). Hasta la fecha (septiembre 2025), de acuerdo con el Registro Mundial de Especies Marinas (World Register of Marine Species; WoRMS: https://www.marinespecies.org/aphia.php?p=taxdetailsyid=205212), se reconocen 4 especies pertenecientes al género Acanthaster: A. planci (Linneo, 1758), A. mauritiensis de Loriol, 1885, A. brevispinus, Fisher, 1917 y A. benziei Worheide, Kaltenbaher, Cowan y Hazprunar, 2022, aunque estudios genéticos apuntan a que A. planci en realidad es un complejo de posiblemente 5 taxones (Hazprunar y Spies, 2014), y refieren que la especie presente en la costa del Pacífico de América podría ser Acanthaster sp. cf. solaris Schreber, 1793. Aunque este último nombre se ha usado en publicaciones recientes relativas a la ecología de Acanthaster en el Pacífico oriental (Martínez-Sarabia y Reyes-Bonilla, 2021; Rodríguez-Villalobos y Ayala-Bocos, 2018, 2021), la discusión sigue activa y por motivos de estabilidad taxonómica, en el presente trabajo se decidió utilizar el nombre de A. planci para referirse a la especie de interés.
A pesar de su presencia en los arrecifes rocosos y coralinos de la región del Pacífico oriental tropical, la estrella no ha recibido demasiada atención quizás debido a sus densidades relativamente bajas (Enochs y Glynn, 2017; Reyes-Bonilla y Calderón-Aguilera, 1999; Rodríguez-Villalobos et al., 2016), así como a la poca evidencia de daño masivo sobre los corales (Rodríguez-Villalobos et al., 2015). Sin embargo, Rodríguez-Villalobos y Ayala-Bocos (2018, 2021) señalaron que en 2017 hubo un incremento abrupto en la densidad de los individuos de esta especie en el Parque Nacional Zona Marina del Archipiélago Espíritu Santo (PNZMAES) acompañado por la mortalidad masiva de colonias de coral de los géneros Pocillopora, Porites y Pavona. Este evento tuvo efectos importantes sobre las comunidades coralinas e incluso afectó esfuerzos de restauración que se estaban llevando a cabo en la misma región (Martínez-Sarabia y Reyes-Bonilla, 2021).
Las causas del incremento de A. planci en el sur del golfo de California son desconocidas. En el Indo-Pacífico las fluctuaciones del tamaño de la población de la estrella se han relacionado con condiciones ambientales como aumentos de temperatura, alta concentración de clorofila y baja salinidad (Fabricius et al., 2010; Hoegh-Guldberg y Pearse, 1995; Lamare et al.,2014). Aunque hasta el momento no hay una explicación universal para la formación de brotes poblacionales (Babcock et al., 2016), el fenómeno debe estar relacionado con las características biológicas de la estrella, tales como alto potencial reproductivo y fecundidad, buena sobrevivencia larval y reclutamiento de individuos, sistemas defensivos en su fase adulta (que incluyen espinas, saponinas y compuestos alelopáticos), y alta capacidad competitiva; además, existen pocos depredadores naturales que controlen el crecimiento de sus poblaciones (Pratchett et al., 2014).
A partir de la observación del aumento anómalo de su abundancia en la región sur del golfo de California y para tener mejores herramientas para el manejo del problema, surgió la interrogante de conocer la estructura de edades de A. planci en la región para elucidar la posible relación del incremento de abundancia con un pulso previo de alto reclutamiento. Así, el objetivo de este trabajo fue obtener los parámetros de la ecuación de crecimiento para una población de A. planci en fase explosiva y calcular la edad relativa de los organismos, además de la tasa de mortalidad natural.
Materiales y métodos
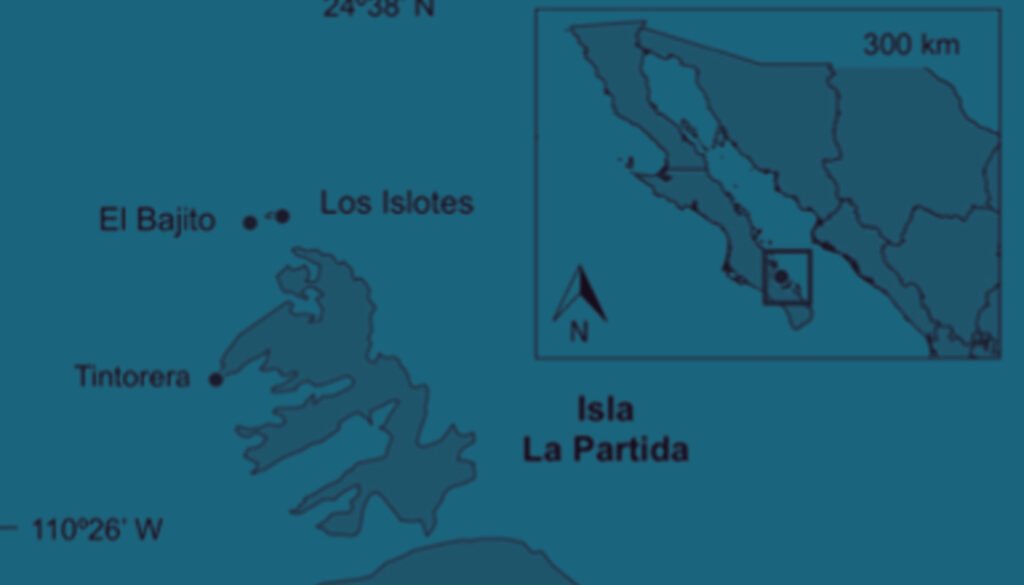
El archipiélago Espíritu Santo se encuentra al oriente de la bahía de La Paz (24º28’17” N, 110º19’57” O; fig. 1). Topográficamente, el litoral oriental de la isla es rocoso y homogéneo, mientras que la costa occidental cuenta con entrantes y salientes que forman zonas protegidas. Las zonas someras en el lado oeste de Espíritu Santo permiten la formación de arrecifes rocosos con la presencia de parches coralinos distribuidos de manera discontinua (Reyes-Bonilla y López-Pérez, 2009). Se registran temperaturas mínimas de 20 ºC a finales del invierno (febrero) y máximas de 30 ºC a mediados del verano (agosto). Adicionalmente, se observan corrientes de menor intensidad en la parte norte y de mayor intensidad en la parte sur (canal de San Lorenzo) (Conanp, 2018).
Se visitaron 10 localidades en el archipiélago (fig. 1) en julio y agosto de 2017, y en septiembre y octubre de 2018 para determinar la abundancia y el diámetro del disco (en cm) de todos los ejemplares de la estrella que se encontraban dentro de transectos de banda de 25 x 3 m, desplegados en paralelo a la línea de costa a una profundidad de 2 a 10 m. Para estimar la tasa de crecimiento y de mortalidad, se empleó el paquete FISAT II (FAO-ICLARM Fish Stock Assessment Tools versión 1.2.2). Se decidió aplicar la curva de crecimiento de von Bertalanffy (Haddon, 2011), ya que Pratchet et al. (2014), después de un análisis de los diversos trabajos al respecto, indican que este es el modelo que mejor expresa el crecimiento de Acanthaster a partir del segundo año de vida.
Para la aplicación del modelo, la talla máxima teórica L∞ fue calculada empleando la técnica de Powell-Wetherall (Haddon, 2011), la cual parte de la suposición que la población está en estado estable (tasa de mortalidad proporcional a la tasa de reclutamiento), y se fundamenta en las siguientes ecuaciones:
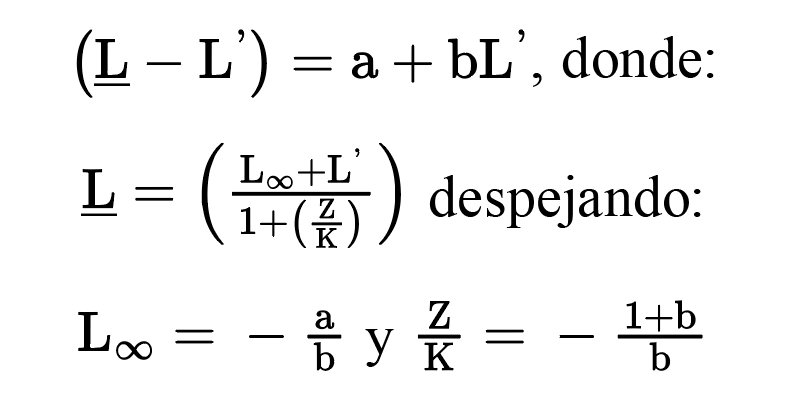
Por otra parte, la tasa de crecimiento K se obtuvo con el método de Shepherd (Haddon, 2011), el cual busca maximizar una función no paramétrica S, que se define como
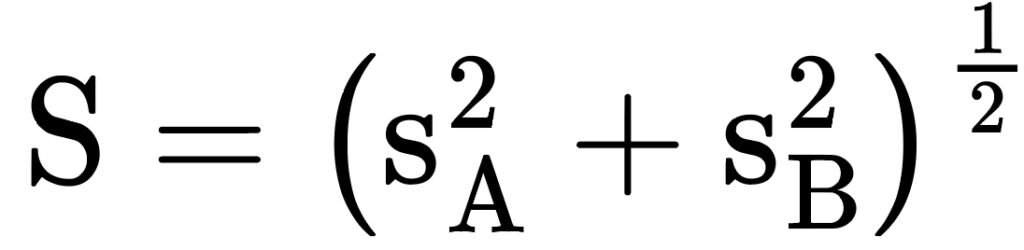
donde SAy SB son los valores de bondad de ajuste (“scores”) obtenidos en tiempo calendario (stz) para SA = 0 y SB = 0.25 años a partir del origen de la curva de crecimiento de VB. Las ecuaciones aplicadas son:

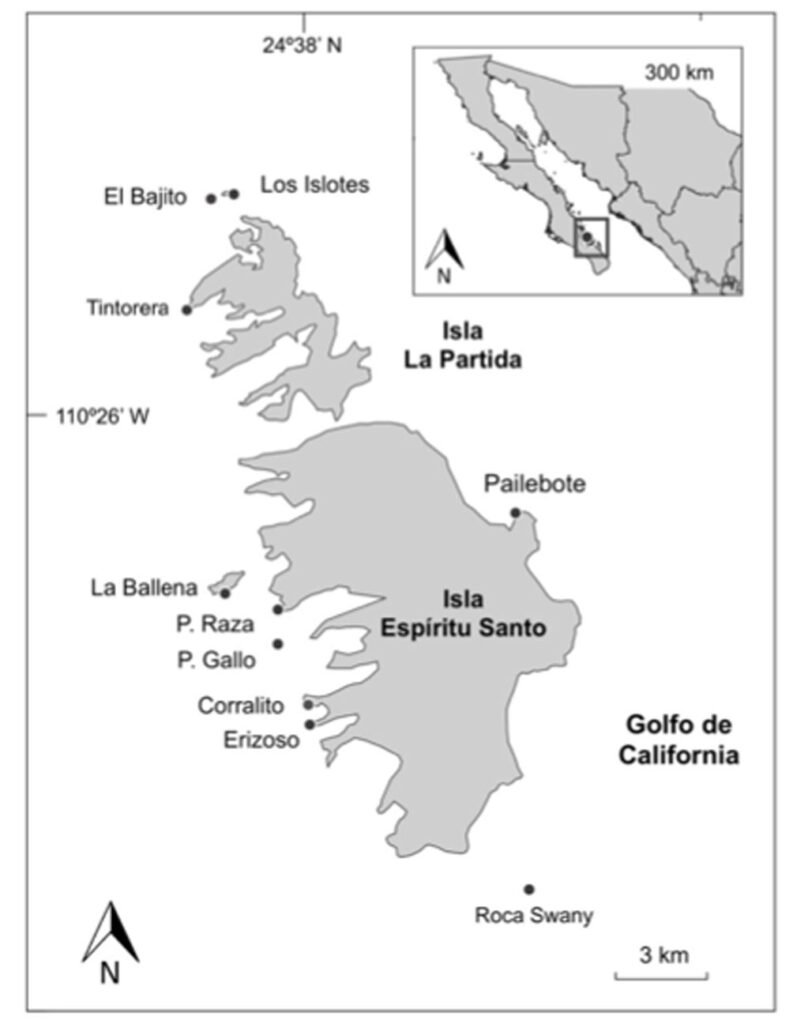
Figura 1. Localización de los puntos de muestreo para la determinación de tallas de Acanthaster planci en el Parque Nacional Zona Marina del Archipiélago Espíritu Santo (PNZMAES).
Una vez con los parámetros L∞ y K, se procedió a trazar la curva teórica de crecimiento de la especie (expresando el diámetro en cm en relación con la edad del organismo en intervalos de 0.25 años) a construir la tabla diámetro de disco-edad, con lo cual se determinó la edad de los individuos muestreados en 2017 y 2018. Tomando en cuenta que los estudios previos sobre crecimiento de la estrella corona de espinas han sido hechos con base en el diámetro total de los individuos (Zann et al., 1987), se trazó una curva teórica para evaluar el crecimiento en esta dimensión, considerando que Glynn (1982) determinó que el diámetro total de Acanthaster en Panamá podría ser aproximado a partir del diámetro del disco ya que este representa 56% del total.
Finalmente, para calcular la tasa de mortalidad de la población (M) de especies a las que no se les puede asignar directamente la edad con base en estructuras óseas u otros procedimientos, se emplean ecuaciones empíricas o basadas en aspectos teóricos del crecimiento de organismos marinos (Sparre y Venema, 1995). La bibliografía cita el uso de diversas metodologías para evaluar este parámetro en equinodermos comerciales (Herrero-Pérezrul y Chávez, 2005; Reyes-Bonilla y Herrero-Pérezrul, 2003), pero para el caso de Acanthaster no todas son aplicables ya que su uso requiere información no disponible; por ejemplo, la ecuación de Rikhter y Efanov utilizada por Penchaszadeh y Molinet (2020), necesita la edad de primera madurez (la cual es desconocida para Acanthaster en el Pacífico americano), mientras que métodos como el de Beverton y Holt (Sparre y Venema, 1995) solo son aplicables a especies de consumo humano porque requieren datos de talla de primera captura. Por lo anterior, se decidió estimar valores de M usando 3 métodos: la ecuación de Pauly (1984) basada en la temperatura promedio local (25 °C) y el valor de L∞ y K; la de Jensen (1997), fundamentada en el valor de K; y la curva de captura de Ricker (1975), obtenida de la frecuencia de individuos y sus respectivas edades estimadas.
Resultados
Se midieron 356 individuos de A. planci en 2017 y 2018. Los especímenes de 2017 fueron en promedio 5.5 cm más pequeños que los de 2018 (tabla 1, fig. 2; t de Student para varianzas desiguales t318 = 13.413, p < 0.001). La distribución de tallas de los individuos se presenta en las figuras 2 y 3, y puede observarse que en 2017 solamente un individuo alcanzó un diámetro de disco superior a 20 cm, mientras que en el año siguiente 21 de 227 organismos (9.3%) superan ese umbral. En 2017, 9% de las estrellas fueron menores a 8 cm de diámetro.
A partir de los análisis de tallas, el diámetro máximo de disco estimado para la población de Acanthaster estudiada (L∞) fue de 30.8 cm mientras que su tasa anual de crecimiento (K) fue de 0.429∙año-1. La ecuación de crecimiento toma entonces la siguiente forma:
Lt = 30.8 * (1 – e [-0.429* (t – 0.01)]),
donde: Lt = diámetro de disco (en cm) a la edad t y t = edad (años).
Los organismos crecen rápidamente de tal modo que al final del año 1 cuentan con 10.7 cm de diámetro de disco, para el año 2 alcanzan 17.7 cm, y para el 3 llegan a 22.2 cm. El modelo teórico junto con la edad estimada de los individuos se presenta en la figura 4. Para facilitar comparaciones con otras publicaciones donde se hace referencia a la talla de A. planci en el Pacífico americano y donde la medida de los organismos se hizo tomando en cuenta el diámetro total, en la figura 5 se presenta la curva teórica de crecimiento aquí generada y la esperada para el diámetro total, considerando que el diámetro del disco representa 55% del diámetro total de la estrella según Glynn (1982).
La estructura esperada de edades para los años 2017 y 2018 a partir de la ecuación de von Bertalanffy y calculada con el diámetro del disco, se presenta en la figura 6. Se observa que la edad predominante en el primer año de muestreo fue entre 1 y 1.5 años (a partir de julio), indicando que los individuos posiblemente se reclutaron a finales de 2015. Esto es corroborado en la figura 6, ya que para 2018 hubo una alta frecuencia de animales con edades de 1.75 a 2.25 años.
Tabla 1
Estadísticos descriptivos (en cm) del diámetro del disco de la población de Acanthaster planci estudiada en el Parque Nacional Zona Marina del Archipiélago Espíritu Santo (PNZMAES) en 2017 y 2018.
| Estadístico | 2017 | 2018 | Ambos años |
| Promedio | 11.43 | 16.96 | 14.96 |
| Desviación típica | 5.44 | 4.28 | 4.78 |
| Error típico | 0.29 | 0.23 | 0.25 |
| Moda | 11 | 16 | 16.0 |
| Mediana | 10.9 | 16.5 | 15.0 |
| Máximo | 23.3 | 28.0 | 28.0 |
| Mínimo | 3.8 | 5.2 | 3.8 |
| N | 129 | 227 | 356 |
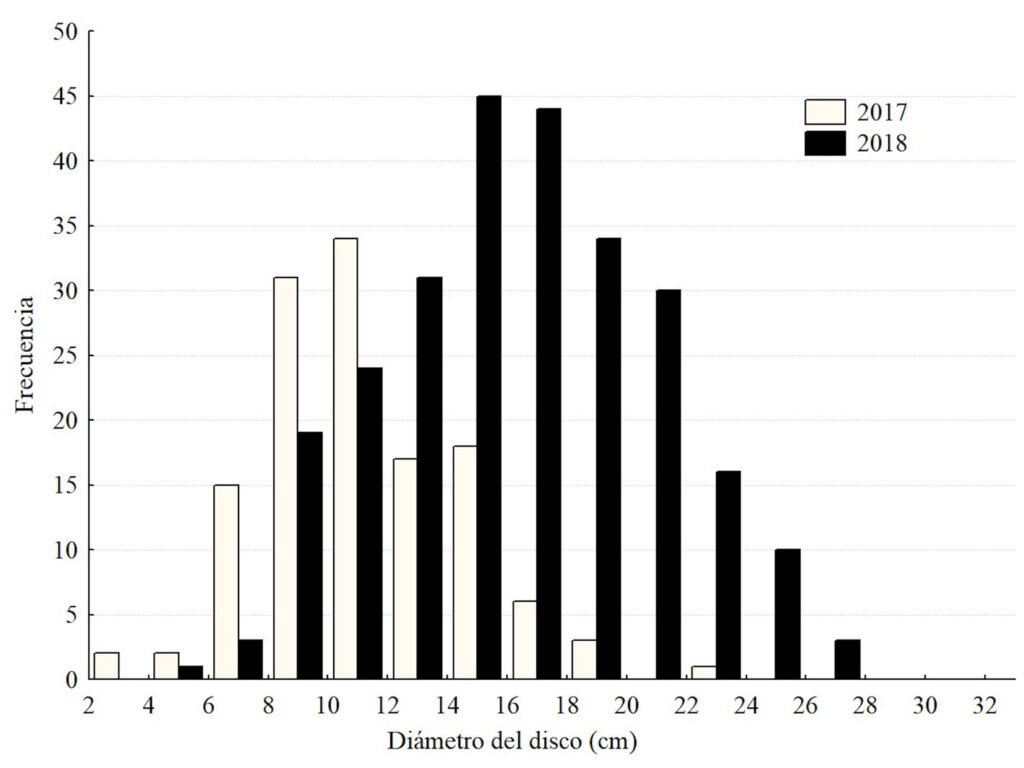
Figura 2. Histogramas del diámetro del disco (en cm) para la población de Acanthaster planci en el Parque Nacional Zona Marina del Archipiélago Espíritu Santo (PNZMAES) durante los años 2017 y 2018.
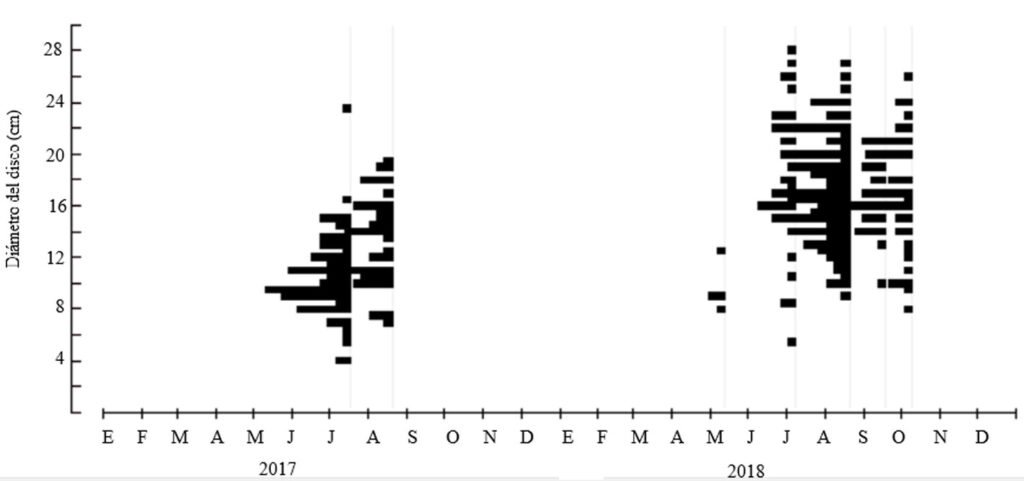
Figura 3. Frecuencia de diámetro del disco de Acanthaster planci en el Parque Nacional Zona Marina del Archipiélago Espíritu Santo (PNZMAES) durante los años 2017 y 2018.
Por último, la tasa anual de mortalidad esperada para la población de A. planci analizada, dependiendo del método indirecto aplicado, fue de 1.0392 (ecuación de Pauly), 0.3983 (curva de captura) y 0.6433 (ecuación de Jensen), con un promedio de 0.6936∙año-1. La mortalidad en el año 1 es alta, ya que el método que arrojó los valores más conservadores (Ricker) indica pérdidas de 33% de la cohorte teórica, mientras que el método de Pauly indica que apenas sobrevive 35%. Al tomar en cuenta el valor promedio de las 3 estimaciones del parámetro M, para el año 1 sobrevive 49.9% de la cohorte, para el año 3 apenas 12.5% de los individuos originales permanece y solo 3.1% alcanza la edad de 5 años. Estos valores se reflejan en los histogramas de edad (fig. 6) donde la edad máxima observada (5.75 años) fue de un individuo de 28 cm.
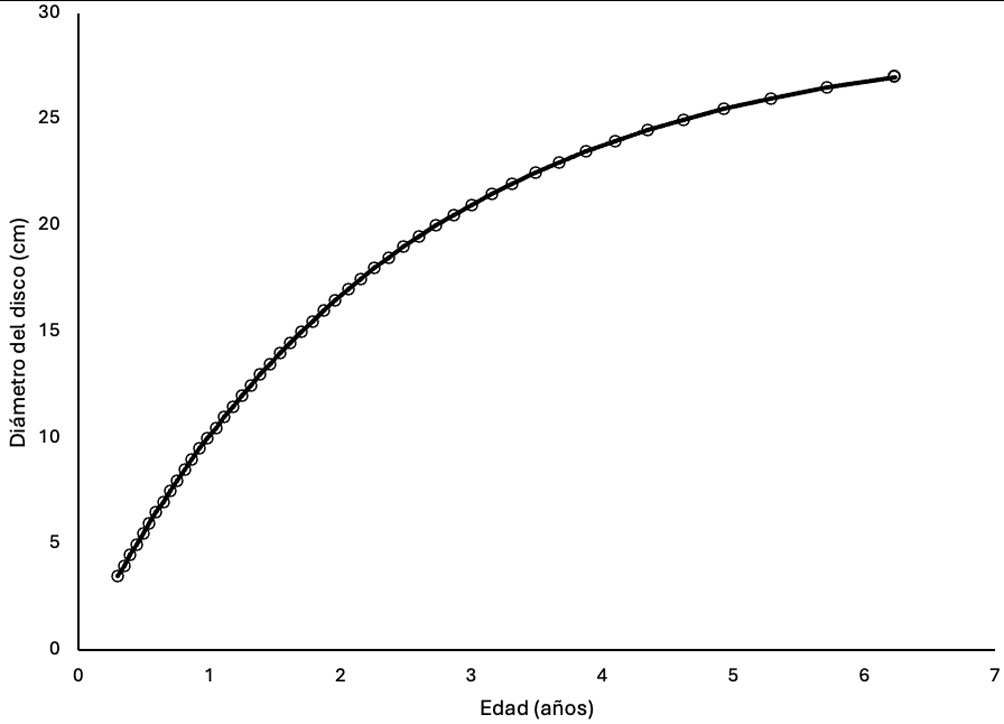
Figura 4. Curva talla-edad de Acanthaster planci en el Parque Nacional Zona Marina del Archipiélago Espíritu Santo (PNZMAES, n = 356).
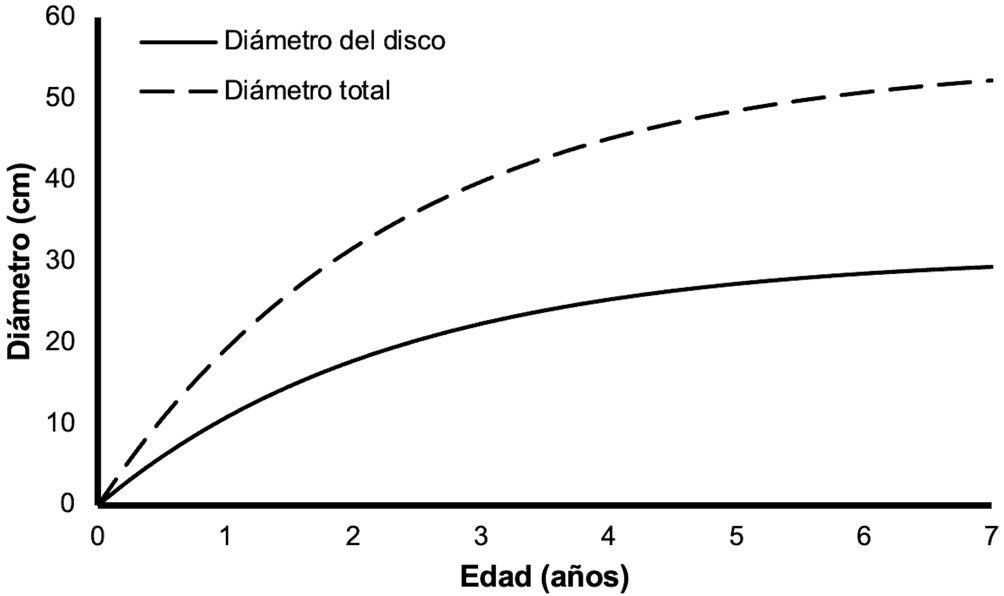
Figura 5. Curvas de crecimiento individual de Acanthaster planci en el Parque Nacional Zona Marina del Archipiélago Espíritu Santo (PNZMAES). La línea puntuada representa la curva extrapolada a partir de la ecuación de Glynn (1982).
Discusión
Este es el primer estudio de crecimiento de Acanthaster planci en el Pacífico oriental y uno de los pocos a escala mundial (MacNeil et al., 2017; Pratchett et al., 2014; Zann et al., 1987). El cálculo de los parámetros de crecimiento de esta especie ha sido difícil de realizar especialmente porque los marcajes en campo para hacer seguimiento de tallas a lo largo del tiempo no han sido exitosos, ya que los individuos eliminan los colorantes o autotomizan la espina o incluso el brazo donde se coloca la marca (Chim y Tan, 2013; MacNeil et al., 2016; Pratchett et al., 2014). Además, en el caso del continente americano, otro motivo que hace complicado conducir estudios demográficos es que las poblaciones son relativamente pequeñas (menos de 70 ind/ha, equivalente a encontrar 1 individuo cada 142.8 m2, según Rodríguez-Villalobos et al. [2021]), lo cual hace complejo tener tamaños de muestra adecuados para realizar análisis en detalle.
Para solucionar ésto, la mayor parte de los trabajos sobre crecimiento de Acanthaster se han basado en especímenes mantenidos en confinamiento (Lucas, 1984; Yamaguchi, 1974; Zann et al., 1987), pero por las dificultades logísticas que implica mantener ejemplares a largo plazo, los experimentos no han durado más de 1 o 2 años. Otra opción para estimar la edad de Acanthaster ha sido la relación entre el número de anillos de las espinas (tomado como indicador indirecto de la edad) y el diámetro total medido en el campo (MacNeil et al., 2017; Stump, 1996), pero la debilidad de estos estudios radica en que no se ha logrado demostrar que los anillos sean anuales. Finalmente, Kenchington (1977) empleó información de 10 años de mediciones de organismos en la Gran Barrera Arrecifal y a partir de cambios en las modas estimó que a la edad de 3 años un individuo podrá superar los 30 cm de diámetro máximo; es decir, el autor empleó un método indirecto similar al utilizado en el presente trabajo. En resumen, los métodos empleados en esta investigación permiten alcanzar estimaciones de crecimiento con una precisión muy semejante a las que se han obtenido en otras partes del mundo, por lo que los resultados obtenidos son confiables.
La talla promedio que se observó tomando en cuenta los años 2017 y 2018 (14.96 + 0.25 cm; tabla 1) frecuentemente se observa en individuos residentes de los arrecifes del Pacífico oriental tropical (Glynn, 1982; Narváez y Zapata, 2010), pero muy inferior a la que se alcanza en el Indo-Pacífico (MacNeil et al., 2016; Mendonça et al., 2010). Esta diferencia se puede explicar con base en los argumentos de Kettle y Lucas (1987) y Hernández-Morales et al. (2021), quienes anotan que la talla de Acanthaster es proporcional a la calidad del alimento consumido, por lo que el pequeño tamaño de los individuos en la zona de estudio y a lo largo del Pacífico oriental tropical se puede deber a que las poblaciones de la estrella corona de espinas tienen una dieta pobre, probablemente debido a que la cobertura y diversidad de corales para alimentarse es mucho menor que en el resto del Pacífico.
Aunque existen diferencias notables tanto en las tallas alcanzadas por Acanthaster en distintas regiones como en las metodologías aplicadas para determinar su curva de crecimiento, los estudios llevados a cabo en Australia muestran que en el primer año de vida esta especie normalmente no alcanza los 5 cm de diámetro total, pero su crecimiento es muy rápido durante el segundo año, alcanzando entre 12.5 y 25 cm, y para el año 3 puede llegar a los 35 cm de diámetro máximo (MacNeil et al., 2017; Pratchett et al., 2014; Zann et al., 1987). Estos hallazgos presentan cierta discrepancia en relación con la talla esperada en el archipiélago Espíritu Santo a un año (fig. 5), la cual es de más de 19 cm de diámetro total, de acuerdo con la corrección sugerida por Glynn (1982). Kenchington (1977), empleando un método de progresión modal, también sugirió que Acanthaster puede alcanzar hasta 12 cm de diámetro máximo para el año 1, pero esa cifra sigue siendo baja comparada con la aquí presentada. Considerando lo anterior, es posible que, como sugieren Pratchett et al. (2014), aunque el modelo de crecimiento de von Bertalanffy es robusto en general y aplicable para describir la relación entre talla y edad de organismos adultos de Acanthaster, no es muy apropiado para determinar la edad de individuos pequeños. Esto se debe a que durante su primer año, la estrella corona de espinas tiene tasas lentas de desarrollo debido a que se alimenta principalmente de algas (Kamya et al., 2017); posteriormente, pasando los 10 cm de diámetro (año 2), los ejemplares comienzan a alimentarse de coral y aceleran notablemente su crecimiento, de acuerdo con Kettle y Lucas (1987).
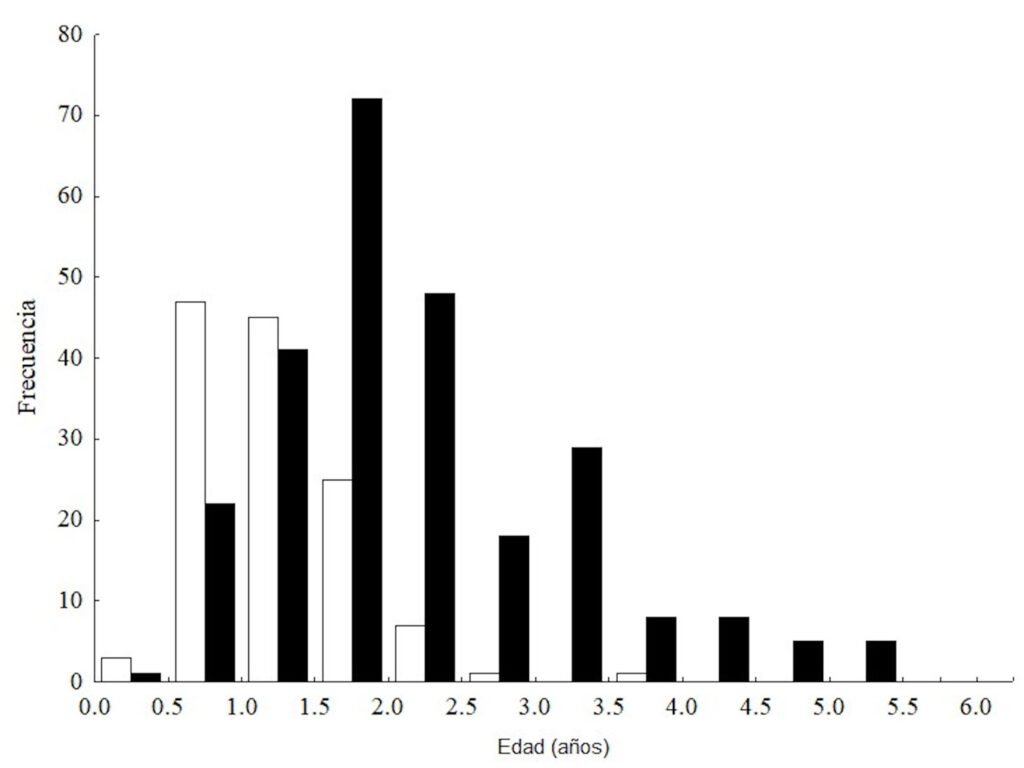
Figura 6. Estructura de edades calculada para los individuos de Acanthaster planci muestreados en 2017 y 2018 en el Parque Nacional Zona Marina de la Isla Espíritu Santo (PNZMAES).
La tasa anual de crecimiento encontrada (K) en este estudio fue de 0.429 año-1, muy similar a la reportada por MacNeil et al. (2017) de 0.54. Los valores en sí no son comparables dado que se emplearon distintas metodologías, por lo que la discusión no puede extenderse más allá de denotar la similitud. Por otra parte, la talla máxima teórica (L∞) del disco de Acanthaster en el PNZMAES fue de 30.8 cm, cercana a la presentada por MacNeil et al. (2017) de 34.9 cm a partir de un modelo bayesiano de Bertalanffy y ambas son mucho más altas que la de 20.2 cm reportada por Zann et al. (1987) en condiciones experimentales y con individuos a los que se les proporcionaron dietas de baja calidad. Usando el factor de corrección propuesto por Glynn (1982), el disco de 30.8 cm se traduce a un diámetro total de 56 cm y ello indica que teóricamente los ejemplares del golfo de California pueden alcanzar los tamaños registrados por Stump (1996) y Pan et al. (2010) en Australia y Japón (58 y 47.4 cm, respectivamente) y por Byrne et al. (2017) en la Gran Barrera Arrecifal (40 cm pero hasta 70 cm de diámetro máximo).
Además de generar el modelo de crecimiento, otro objetivo de este trabajo fue generar insumos para tratar de explicar la causa del fenómeno de explosión poblacional observado para Acanthaster en el PNZMAES durante 2017 y 2018. A este respecto y con base en la relación talla-edad, los histogramas (fig. 6) muestran que el reclutamiento de los individuos debió haber ocurrido en 2015, año durante el cual la zona se vio impactada por uno de los eventos de oscilación sureña de El Niño más fuertes en lo que va del siglo XXI y el cual afectó a los arrecifes de coral del Pacífico oriental y a las especies asociadas (Cruz-García et al., 2020; Riegl et al., 2019). La anomalía térmica alcanzada en la región de la bahía de La Paz fue superior a 2 °C (Coria-Monter et al., 2018) y alteró la ecología de todo tipo de organismos, desde mamíferos marinos hasta elementos del plancton (Elorriaga-Verplancken et al., 2016; Portner et al., 2022). Por el contrario, al año siguiente (2016-2017) la región del golfo de California estuvo influenciada por un evento de La Niña que favoreció la alta concentración de clorofila a en la columna de agua, la presencia de surgencias y aumentó la productividad (Farach-Espinosa et al., 2021).
Considerando lo anterior, es posible hipotetizar las causas del evento de explosión poblacional. Dado que las altas temperaturas aumentan la sobrevivencia larval y de los juveniles de Acanthaster (Hughes et al., 2014; Lamare et al., 2014, Pratchett et al., 2017), las anomalías térmicas de la región sur del golfo de California en 2015, combinadas con la enorme fecundidad de la estrella (más de 50 millones de huevos por individuo; Conand, 1984; Hughes et al., 2014), debieron favorecer un reclutamiento masivo. Posteriormente, las condiciones frías y productivas en el año 2016 pudieron aumentar la sobrevivencia de los juveniles al impulsar un mejor crecimiento algal en el fondo arrecifal (Wolfe et al., 2017). Así, para el año 2017 los organismos ya tenían tallas fácilmente detectables en el campo y comenzaron a realizar sus actividades de depredación, las cuales causaron notables daños a las comunidades de coral de la zona de estudio ese año (Rodríguez-Villalobos y Ayala-Bocos, 2018).
La hipótesis anterior se sustenta por los datos del modelo de edad y también por las tallas observadas en el campo. Los diámetros de disco esperados para los ejemplares (promedios de 11.43 ± 0.29 cm en 2017 y 16.96 ± 0.23 cm en 2018; tabla 1) coinciden con los reportados por Rodríguez-Villalobos y Ayala-Bocos (2021) para la zona de El Corralito en la isla Espíritu Santo (fig. 1) en 2017 (14.72 ± 2.85 cm de diámetro), lo que indica que para ese año la población de Acanthaster en la zona de estudio estaba compuesta fundamentalmente de individuos menores a 3 años, nacidos en 2015-2016 (fig. 6).
Finalmente, el modelo de sobrevivencia indica que un porcentaje muy elevado de los reclutas desaparece en el primer año de vida. Varios estudios han indicado que la tasa de mortalidad de los juveniles de Acanthaster es muy elevada (Fabricius et al., 2010; Nakamura et al., 2014; Zann et al., 1987), aunque la estimación en campo de este parámetro es notablemente difícil de obtener ya que los individuos recién reclutados de la estrella son crípticos (Fabricius, 2013). La longevidad esperada en el archipiélago Espíritu Santo fue de aproximadamente 6 años, lo cual corresponde bien a lo reportado por otros autores en Australia que indican entre 4 y 9 años de vida (Lucas, 1984; Pratchett et al., 2014). Tomando en cuenta este dato clave, es probable que la mayor parte de la cohorte de 2015 que causó el evento de mortalidad coralina masiva ya no estuviera presente en los arrecifes de la zona de estudio después del año 2021, lo cual fue confirmado a partir de datos de censos (densidades de 0.27 ind/50m2 en 2017-2018 bajó a 0.19 ind/50m2 en 2023-24). Esto implica que la población de la estrella de mar corona de espinas en el sur del golfo de California se comportó siguiendo el modelo de “aumento-caída”, típico de la especie en el Indo-Pacífico y de otros equinodermos con larvas planctotróficas (Uthicke et al., 2009).
Agradecimientos
A las autoridades y el personal del PNZMAES por las facilidades logísticas. A los miembros del staff y estudiantes asociados a la Sociedad de Historia Natural Niparajá, A.C., al personal del Laboratorio de Sistemas Arrecifales (UABCS) y a Arturo Ayala Bocos que apoyaron en las labores de campo. Las observaciones y comentarios de un revisor anónimo y del editor de la Revista Mexicana de Biodiversidad fueron clave para mejorar la presentación de las ideas y fortalecer la calidad del manuscrito.
Referencias
Babcock, R. C., Dambacher, J. M., Morello, E. B., Plagányi, É. E., Hayes, K. R., Sweatman, H. P. A. et al. (2016). Assessing different causes of Crown-of-Thorns starfish outbreaks and appropriate responses for management on the Great Barrier Reef. Plos One, 11, e0169048. https://doi.org/10.1371/journal.pone.0169048
Barham, E. G., Gowdy, R. W. y Wolfson, F. H. (1973). Acanthaster (Echinodermata, Asteroidea) in the Gulf of California. Fishery Bulletin, 71, 927–942.
Byrne, M., Rowe, F. W., Marsh, M. L. y Mah, L. C. (2017). Class Asteroidea. En: O’Hara, T. y Byrne, M. (Eds.), Australian echinoderms: biology, ecology and evolution (pp. 231–294). Melbourne: CSIRO publishing, Clayton South, Australia.
Chim, C. K. y Tan, K. S. (2013). A method for the external attachment of acoustic tags on sea stars. Journal of the Marine Biology Association of the United Kingdom, 93, 267–272. https://doi.org/10.1017/S0025315411002128
Conanp (Comisión Nacional de Áreas Naturales Protegidas). (2018). Programa de Manejo Parque Nacional exclusivamente la zona marina del Archipiélago de Espíritu Santo. Disponible en: https://www.gob.mx/publicaciones/es/articulos/parque-nacional-exclusivamente-la-zona-marina-del-archipielago-de-espiritu-santo?idiom=es
Conand, C. (1984). Distribution, reproductive cycle and morphometric relationships of Acanthaster planci (Echinodermata: Asteroidea) in New Caledonia, western tropical Pacific. Proceedings of the 5th International Echinoderm Conference, Galway, 1, 499–506.
Coria-Monter, E., Monreal-Gómez, M. A., de León, D. A. S. y Durán-Campos, E. (2018). Impact of the “Godzilla El Niño” Event of 2015-2016 on sea-surface temperature and chlorophyll-a in the southern Gulf of California, Mexico, as evidenced by satellite and in situ data. Pacific Science, 72, 411–422. https://doi.org/10.2984/72.4.2
Cruz-García, R., Rodríguez-Troncoso, A. P., Rodríguez-Zaragoza, F. A., Mayfield, A. y Cupul-Magaña, A. L. (2020). Ephemeral effects of El Niño southern oscillation events on an eastern tropical Pacific coral community. Marine Freshwater Research, 71, 1259–1268. https://doi.org/10.1071/MF18481
Dana, T. y Wolfson, A. (1970). Eastern Pacific Crown-of-thorns starfish populations in the lower Gulf of California. San Diego Society of Natural History, 16, 83–90. https://doi.org/10.5962/bhl.part.15455
De’ath G., Fabricius, K. E., Sweatman, H. y Puotinen, M. (2012). The 27-year decline of coral cover on the Great Barrier Reef and its causes. Proceedings of the National Academy of Sciences of the Unites States of America, 109, 17995–17999. https://doi.org/10.1073/pnas.1208909109
Elorriaga-Verplancken, F. R., Rosales-Nanduca, H. y Robles-Hernández, R. (2016). Unprecedented records of Guadalupe fur seals in La Paz Bay, Southern Gulf of California, Mexico, as a possible result of warming conditions in the northeastern Pacific. Aquatic Mammals, 42, 261–267. https://doi.org/10.1578/AM.42.3.2016.261
Enochs, I. C. y Glynn, P. W. (2016). Corallivory in the eastern Pacific. En Glynn, P. W., Manzello, D. y Enochs, I. C. (Eds.), Coral reefs of the Eastern Tropical Pacific: persistence and loss in a dynamic environment (pp. 315–337). Dordrecht: Springer Netherlands. https://doi.org/10.1007/978-94-017-7499-4_10
Fabricius, K. (2013). Acanthaster planci. En J. M. Lawrence (Eds.), Starfish: Biology and ecology of the Asteroidea (pp. 132–141). Baltimore: The Johns Hopkins University Press.
Fabricius, K. E., Okaji, K. y De’ath, G. (2010) Three lines of evidence to link outbreaks of the crown-of-thorns sea star Acanthaster planci to the release of larval food limitation. Coral Reefs, 29, 593–605. https://doi.org/10.1007/s00338-010-0628-z
Farach-Espinoza, E. B., López-Martínez, J., García-Morales, R., Nevárez-Martínez, M. O., Lluch-Cota, D. B. y Ortega-García, S. (2021). Temporal variability of oceanic mesoscale events in the Gulf of California. Remote Sensing, 13, 1774. https://doi.org/10.3390/rs13091774
Fisheries and aquaculture software. FISAT II – FAO-ICLARM Stock Assessment Tool. En FAO Fisheries and Aquaculture Department (online). Rome. Recuperado 20 agosto, 2025 de: https://www.fao.org/fishery
Glynn, P. W. (1982). Individual recognition and phenotypic variability in Acanthaster planci (Echinodermata: Asteroidea). Coral Reefs, 1, 89–94. https://doi.org/10.1007/BF00301690
Haddon, M. (2011). Modelling and quantitative methods in fisheries, 2° Ed. San Francisco: Chapman y Hall.
Haszprunar, G. y Spies, M. (2014). An integrative approach to the taxonomy of the crown-of-thorns starfish species group (Asteroidea: Acanthaster): a review of names and comparison to recent molecular data. Zootaxa, 3841, 271–284. https://doi.org/10.11646/zootaxa.3841.2.6
Hernández-Morales, A., Herrero-Pérezrul, M. D. y Vázquez-Arce, D. I. (2021). Variability of size and food type of Acanthaster planci (Echinodermata: Asteroidea) in the southern Gulf of California, Mexico. Revista de Biología Tropical, 69, 185–201. https://doi.org/10.15517/rbt.v69iSuppl.1.46352
Herrero-Pérezrul, M. D. y Chávez, E. A. (2005). Optimum fishing strategies for Isostichopus fuscus (Echinodermata: Holothuroidea) in the Gulf of California, México. Revista de Biología Tropical, 53 (Suppl. 3), 357–366.
Hoegh-Guldberg, O. y Pearse, J. S. (1995). Temperature, food availability, and the development of marine invertebrate larvae. American Zoologist, 35, 415–425.
Hughes, R. N., Hughes, D. J. y Smith, I. P. (2014). Limits to understanding and managing outbreaks of crown-of-thorns starfish (Acanthaster spp.). Oceanography and Marine Biology Annual Review, 52, 133–200. https://doi.org/10.1201/b17143-4
Jensen, A. L. (1997). Origin of the relation between K and Linf and synthesis of relations among life history parameters. Canadian Journal of Fisheries and Aquatic Sciences, 54,987–989. https://doi.org/10.1139/f97-007
Kamya, P. Z., Byrne, M., Mos, B., Hall, L. y Dworjanyn, S. A. (2017). Indirect effects of ocean acidification drive feeding and growth of juvenile crown-of-thorns starfish, Acanthaster planci. Proceedings of the Royal Society of Biology, 284, 20170778. https://doi.org/10.1098/rspb.2017.0778
Kayal, M., Vercelloni, J., Lison de Loma, T., Bosserelle, P., Chancerelle, Y., Geoffroy, S. et al. (2012). Predator Crown-of-Thorns starfish (Acanthaster planci) outbreak, mass mortality of corals, and cascading effects on reef fish and benthic communities. Plos One, 7, e47363. https://doi.org/10.1371/journal.pone.0047363
Kenchington, R. A. (1977). Growth and recruitment of Acanthaster planci (L.) on the Great Barrier Reef. Biological Conservation, 11, 103–118. https://doi.org/10.1016/0006-3207(77)90032-5
Kettle, B. T. y Lucas, J. S. (1987). Biometric relationships between organ indices, fecundity, oxygen consumption and body size in Acanthaster planci (L.) (Echinodermata; Asteroidea). Bulletin of Marine Science, 41, 541–551.
Lamare, M., Pecorino, D., Hardy, N., Liddy, M., Byrne, M. y Uthicke, S. (2014). The thermal tolerance of crown-of-thorns (Acanthaster planci) embryos and bipinnaria larvae: implications for spatial and temporal variation in adult populations. Coral Reefs, 33, 207–219. https://doi.org/10.1007/s00338-013-1112-3
Lucas, J. S. (1984). Growth and maturation of Acanthaster planci (L.) (Asteroidea) and hybrids in the laboratory. Journal of Experimental Marine Biology and Ecology, 79, 129–147. https://doi.org/10.1016/0022-0981(84)90214-4
MacNeil, M. A., Chong-Seng, K. M., Pratchett, D. J., Thompson, C. A., Messmer, V. y Pratchett, M. S. (2017). Age and growth of an outbreaking Acanthaster cf. solaris population within the Great Barrier Reef. Diversity, 9, 18. https://doi.org/10.3390/d9010018
MacNeil, M. A., Mellin, C., Pratchett, M. S., Hoey, J., Anthony, K. R., Cheal, A. J. et al. (2016). Joint estimation of crown of thorns (Acanthaster planci) densities on the Great Barrier Reef. PeerJ, 4, e2310. https://doi.org/10.7717/peerj.2310
Martínez-Sarabia, P. y Reyes-Bonilla, H. (2021). Damage caused by crown-of-thorns starfish (Acanthaster cf. solaris) outbreak to restored corals in the southern Gulf of California, Mexico. Bulletin of Marine Science, 97, 329–336. https://doi.org/10.5343/bms.2020.0034
Mendonça, V. M., Al Jabri, M. M., Al Ajmi, I., Al Muharrami, M., Al Areimi, M. y Al Aghbari, H. A. (2010). Persistent and expanding population outbreaks of the corallivorous starfish Acanthaster planci in the northwestern Indian Ocean: are they really a consequence of unsustainable starfish predator removal through overfishing in coral reefs, or a response to a changing environment. Zoological Studies, 49, 108–123.
Nakamura, M., Okaji, K., Higa, Y., Yamakawa, E. y Mitarai, S. (2014). Spatial and temporal population dynamics of the crown-of-thorns starfish, Acanthaster planci, over a 24-year period along the central west coast of Okinawa Island, Japan. Marine Biology, 161, 2521–2530. https://doi.org/10.1007/s00227-014-2524-5
Narváez, K. y Zapata, F. A. (2010). First record and impact of the crown-of-thorns starfish, Acanthaster planci (Spinulosida: Acanthasteridae) on corals of Malpelo Island, Colombian Pacific. Revista de Biología Tropical, 58, 139–143.
Pan, M., Hilomen, V. y Palomares, M. L. D. (2010). Size structure of Acanthaster planci populations in Tubbataha Reefs Natural Parks, Sulu Sea, Philippines. En M. L. D. Palomares y D. Pauly (Eds.), Marine biodiversity of Southeast Asian and adjacent seas (pp.70–77). Vancouver: University of British Columbia Fisheries Centre Research Reports.
Penchaszadeh, P. E. y Molinet, R. (2020). Population ecology of the sand dollar Mellita quinquiesperforata latiambulacra Clark, 1940 on the west-central coast of Venezuela. En B. David, A. Guille y J. P. Feral (Eds.), Echinoderms through time (pp. 827–834). Londres: CRC Press.
Pratchett, M. S., Caballes, C. F., Rivera-Posada, J. A. y Sweatman, H. P. A. (2014). Causes and consequences of outbreaks of crown-of-thorns starfishes (Acanthaster spp.). Oceanography and Marine Biology Annual Review, 52, 133–200. https://doi.org/10.1201/b17143-4
Pratchett, M. S., Dworjanyn, S., Mos, B., Caballes, C. F., Thompson, C. A. y Blowes, S. (2017). Larval survivorship and settlement of crown-of-thorns starfish (Acanthaster cf. solaris) at varying algal cell densities. Diversity, 9, 1–11. https://doi.org/10.3390/d9010002
Pauly, D. (1984). Length-converted catch curves: a powerful tool for fisheries research in the tropics (Part III). Fishbyte, Newsletter of the Network of Tropical Fisheries Scientists, 2, 17–19.
Portner, E. J., Benoit-Bird, K. J., Hazen, E. L., Waluk, C. M., Robinson, C. J., Gómez-Gutiérrez, J. et al. (2022). Decline and recovery of pelagic acoustic backscatter following El Niño events in the Gulf of California, Mexico. Progress in Oceanography, 206, 102823. https://doi.org/10.1016/j.pocean.2022.102823
Reyes-Bonilla, H. y Calderón-Aguilera, L. E. (1999). Population density, distribution and consumption rates of three corallivores at Cabo Pulmo Reef, Gulf of California, Mexico. Marine Ecology, 20, 344–357. https://doi.org/10.1046/j.1439-0485.1999.2034080.x
Reyes-Bonilla, H. y Herrero-Pérezrul, M. D. (2003). Population parameters of an exploited population of Isostichopus
fuscus (Holothuroidea) in the southern Gulf of California, Mexico. Fisheries Research, 59, 423–430. https://doi.org/10.1016/S0165-7836(02)00023-1
Reyes-Bonilla, H. y López-Pérez, R. A. (2009). Corals and coral-reef communities in the Gulf of California. En M. E. Johnson y J. Ledezma-Vásquez (Eds.). Atlas of coastal ecosystems in the Western Gulf of California (pp. 45–57). Tucson: University of Arizona Press.
Ricker, W. C. (1975). Computation and interpretation of biological statistics of fish populations. Bulletin of the Fisheries Research Board of Canada, 191, 1–382.
Riegl, B., Glynn, P. W., Banks, S., Keith, I., Rivera, F., Vera-Zambrano, M. et al. (2019). Heat attenuation and nutrient delivery by localized upwelling avoided coral bleaching mortality in northern Galapagos during 2015/2016 ENSO. Coral Reefs, 38, 773–785. https://doi.org/10.1007/s00338-019-01787-8
Rodríguez-Villalobos, J. C., Work, T. M., Calderón-Aguilera, L. E., Reyes-Bonilla, H. y Hernández, L. (2015). Explained and unexplained tissue loss in corals from the tropical Eastern Pacific. Diseases of Aquatic Organisms, 116, 121–131. https://doi.org/10.3354/dao02914
Rodríguez-Villalobos, J. C. y Ayala-Bocos A. (2018). Coral colonies in the eastern tropical Pacific: predation by Acanthaster cf. solaris. Pacific Conservation Biology, 24, 419–420. https://doi.org/10.1071/PC18040
Rodríguez-Villalobos, J. C. y Ayala-Bocos, A. (2021). Massive predation by Acanthaster planci in El Corralito, Gulf of California: a short-term threat. Revista de Biología Tropical, 69, 272–286. https://doi.org/10.15517/rbt.v69i
Suppl.1.46359
Rodríguez-Villalobos, J. C., Hernández-Carreón, C., Reyes-Bonilla, H., Rojas-Montiel, B. y Weaver, A. H. (2021). Temporal and spatial abundance of Acanthaster cf. solaris (Echinodermata: Asteroidea) in a national park in the Gulf of California, Mexico: 2005-2016. Pacific Science, 74, 269–282. https://doi.org/10.2984/74.3.5
Sparre, P. y Venema, S. C. (1995). Introducción a la evaluación de recursos pesqueros. FAO Documento técnico Pesca 306/1. DANIDA-FAO, Rome.
Stump, R. J. W. (1996). An investigation of the methods to describe the population dynamics of Acanthaster planci(L.) around Lizard Island, northern Cairns Section, GBR. Documento técnico No. 10. Townsville, Australia: CRC Reef Research and Great Barrier Reef Marine Park Authority.
Uthicke, S., Schaffelke, B. y Byrne, M. (2009). A boom-bust Phylum? Ecological and evolutionary consequences of density variations in echinoderms. Ecological Monographs, 79, 3–24. https://doi.org/10.1890/07-2136.1
Wolfe, K., Graba-Landry, A., Dworjanyn, S. A. y Byrne, M. (2017). Superstars: assessing nutrient thresholds for enhanced larval success of Acanthaster planci, a review of the evidence. Marine Pollution Bulletin, 116, 307–314. https://doi.org/10.1016/j.marpolbul.2016.12.079
Yamaguchi, M. (1974). Growth of juvenile Acanthaster planci (L.) in the laboratory. Pacific Science, 28, 123–138.
Zann, L., Brodie, J., Berryman, C. y Naqasima, M. (1987). Recruitment, ecology, growth and behavior of juvenile Acanthaster planci (L.) (Echinodermata: Asteroidea). Bulletin of Marine Science, 41, 561–575.