Ecological niche conservatism in sister species of Euglossa (Apidae: Euglossini) from Mexico and Central America
A. Celeste Martínez-Cervantes, Enrique Martínez-Meyer e Ismael A. Hinojosa-Díaz *
Universidad Nacional Autónoma de México, Instituto de Biología, Departamento de Zoología, Tercer Circuito Universitario s/n, Ciudad Universitaria, Coyoacán, 04510 Ciudad de México, México
*Autor para correspondencia: ihinojosa@ib.unam.mx (I.A. Hinojosa-Díaz)
Recibido: 10 enero 2025; aceptado: 30 octubre 2025
Resumen
Las abejas de la tribu Euglossini son un grupo importante de polinizadores de la región neotropical al contribuir a la reproducción de plantas por las visitas de las hembras en búsqueda de recursos florales, mientras los machos son polinizadores específicos de grupos de orquídeas en su búsqueda de químicos aromáticos, que pueden obtener de otros sustratos y que son utilizados como señales de apareamiento. El género Euglossa es el más diverso de la tribu, ocupa diversos ambientes desde el norte de México hasta el sur de la región neotropical. Se conocen las afinidades filogenéticas de muchas de las especies del género. En este estudio se describe y compara el nicho climático en 3 pares de especies hermanas del género Euglossa bajo la premisa de conservadurismo de nicho, encontrando similitud significativa solo entre las especies hermanas dentro del subgénero Euglossa, mientras que en los otros pares de especies comparadas, la similitud de nicho está más relacionada con la simpatría de las especies que con la cercanía filogenética.
Palabras clave: Abejas de orquídeas; Conservadurismo de nicho; Simpatría
Abstract
Bees of the tribe Euglossini are important pollinators in the Neotropical region contributing to the reproduction of a variety of plants visited by females in search for floral resources while males are specialized pollinators of groups of orchids in their quest for aromatic chemicals, also retrieved from other sources and later used as sexual signals. Euglossa is the most diverse genus in the tribe ranging from northern Mexico to the southern parts of the Neotropical region. General phylogenetic affinities are known for several species in the genus. Here we describe and compare the ecological niche for 3 pairs of sister species of the genus Euglossa under the premise of niche conservatism, for which we found significant similarity only between sister species in the subgenus Euglossa, whereas in the other comparisons niche similarity is explained by the sympatric distributions of the species rather than by their phylogenetic relationships.
Keywords: Orchid bees; Niche conservatism; Sympatry
Introducción
Las abejas de las orquídeas suelen exhibir colores metálicos brillantes y partes bucales alargadas, que en ciertas especies puede superar la longitud de sus propios cuerpos (Engel y Rasmussen, 2020; Roubik y Hanson, 2004). Los machos, se distinguen por una serie de caracteres sexuales secundarios relacionados con la recolección de sustancias aromáticas, sobresale la tibia posterior ancha donde se almacenan estos químicos combinados con secreciones de las glándulas labiales (Engel y Rasmussen, 2020; Roubik y Hanson, 2004). Estos compuestos funcionan como señales de atracción y estimulación de las hembras para el apareamiento (Henske et al., 2023). Los machos adquieren compuestos aromáticos principalmente de orquídeas, aunque también frecuentan otras familias de plantas y otros recursos como madera en descomposición, hongos e incluso productos químicos sintéticos (Engel y Rasmussen, 2020; Roubik y Hanson, 2004). Estas abejas representan uno de los principales polinizadores del Neotrópico al participar en la polinización de más de 60 familias de plantas, incluyendo alrededor de 700 especies de orquídeas (Roubik y Hanson, 2004).
La tribu Euglossini se originó entre hace 27 y 42 millones de años en América del Sur (Ramírez et al., 2010; Roubik y Hanson, 2004). Se han propuesto varias hipótesis con respecto a las relaciones entre los géneros, tanto con caracteres moleculares como morfológicos (Ramírez et al., 2010). Actualmente, se han registrado 249 especies de euglossinos exclusivamente neotropicales (Engel y Rasmussen, 2020), divididos en 5 géneros: Aglae, Exaerete, Eulaema, Eufriesea y Euglossa.
El género Euglossa es el más diverso dentro de la tribu, con 139 especies (Engel y Rasmussen, 2020). Su origen se remonta al Mioceno medio (Ramírez et al., 2010). Las relaciones dentro del género no están del todo resueltas y varios autores han subdividido al género en 6 subgéneros: Alloglossura, Dasystilbe, Euglossella, Euglossa, Glossurella y Glossuropoda. Recientemente, se han propuesto 4 nuevos subgéneros: Eurhytisma, Glossurodes, Parisoglossa y Trachyglossa para ayudar a resolver la parafilia de los subgéneros Glossurella y Glossuropoda (Engel, 2021).
Las relaciones evolutivas entre las especies o diferentes taxones se muestran a través de las filogenias (Eliosa et al., 2010). En los árboles filogenéticos podemos observar gráficamente estas relaciones y entender de mejor manera las conexiones entre las especies o los taxones. El conservadurismo de nicho es la tendencia de las especies a retener características ecológicas en el tiempo cuando se enfrentan a condiciones ambientales nuevas (Wiens y Donoghue, 2004; Wiens y Graham, 2005). El conservadurismo de nicho tiende a romperse con el tiempo, lo que resulta en un mayor conservadurismo entre especies que han divergido recientemente y que están estrechamente relacionadas, como es el caso de las especies hermanas (Pyron et al., 2015).
En este trabajo se describe y compara el nicho climático de especies hermanas de Euglossa, incluyendo los subgéneros Euglossa (sensu stricto), Dasystilbe y Eurhytisma para evaluar qué tan conservados son los nichos entre y dentro de estos subgéneros. Bajo la premisa del conservadurismo de nicho ecológico, esperamos que los nichos de las especies dentro de los subgéneros sean más parecidos que entre especies de subgéneros distintos.
Materiales y métodos
Especies
Subgénero Euglossa s. st. Euglossa dilemma y E. viridissima son especies hermanas distintivas dentro del subgénero Euglossa y muy afines morfológicamente que divergieron hace ~ 150,000 años (Brand et al., 2020; Eltz et al., 2011). Antes de la descripción de Euglossa dilemma (Eltz et al., 2011), E. viridissima se consideraba una especie con variación morfológica, hasta que se demostró inicialmente con evidencia morfológica y distribucional (Eltz et al., 2011), y reforzándose con evidencia genética que E. dilemma es una especie distinta (Brand et al., 2020). Ambas especies presentan poblaciones simpátricas, con áreas de traslape al sur-sureste de México y parte de Guatemala y Belice.
El subgénero Dasystilbe solo cuenta con 2 especies: E. obrima y E. villosa. Son abejas grandes que miden ~ 15 mm de longitud, presentan una coloración verde metálico con iridiscencia azul o bronce. Su cuerpo está cubierto de sedas largas y densas, especialmente en los costados (Hinojosa-Díaz et al., 2011). Los machos presentan una mandíbula bidentada, mientras que las hembras una tridentada (Hinojosa-Díaz et al., 2011).
Subgénero Eurhytisma (antes parte de Glossurella). El subgénero Glossurella era considerado un grupo parafilético (Engel, 2021); sin embargo, la relación de especies hermanas entre E. obtusa y E. dodsoni se ha mantenido a lo largo de las filogenias realizadas del género (Ghassemi-Khademi, 2018; Ramírez et al., 2010). Más tarde, se describe la especie E. williamsi, la cual no ha sido considerada en la metodología de las filogenias del género; no obstante, en el artículo donde se describe la especie se señala que ésta, muy probablemente, conforma un grupo monofilético junto con E. obtusa y E. dodsoni al presentar estructuras morfológicas similares, como la presencia de la mancha preomaular (en el mesepisterno) compartida entre las 3 especies (Hinojosa-Díaz y Engel, 2011). Partiendo de esta idea, Engel (2021) une a estas 3 especies en un nuevo subgénero llamado Eurhytisma. Lamentablemente, debido a la falta de registros de la especie E. williamsi, se decidió omitirla del presente estudio, sin embargo, la fuerte afinidad morfológica entre E. obtusa y E. dodsoni es un argumento fuerte para considerarlas más cercanas entre ellas respecto de E. williamsi (Hinojosa-Díaz y Engel, 2011).
Los datos recopilados se obtuvieron de diversas fuentes, incluyendo colecciones biológicas y acervos electrónicos: Colección Nacional de Insectos del Instituto de Biología de la Universidad Nacional Autónoma de México (CNIN); base de datos de la Colección de abejas de ECOSUR en San Cristóbal de las Casas, México; Sistema Nacional de Información sobre Biodiversidad de México (Conabio, 2021); Global Biodiversity Information Facility (GBIF); Discover Life (Ascher y Pickering, 2018) y Catalogue of Bees (Hymenoptera, Apoidea) in the Neotropical Region (Moure y Melo, 2023). Posteriormente, se depuraron los datos eliminando registros duplicados y se georreferenciaron aquellos sin coordenadas mediante el uso de Google Earth (tabla 1).
Capas ambientales
Se emplearon 33 capas con una resolución de 2.5 minutos de arco (apéndice), limitándose al área de registro de las especies que es Centroamérica y México. Las capas ambientales de precipitación y temperatura se extrajeron de la base de datos WorldClim 2.0 (Fick y Hijmans, 2017). En cuanto a la humedad (mínima, media y máxima), se utilizaron las capas de MERRAclim (Vega et al., 2018). Para simplificar las variables y mejorar el modelo, se llevó a cabo una selección basada en el coeficiente de correlación de Spearman (˃ 0.75 o ˂ -0.75) por especie y únicamente con los puntos de presencia.
Área de calibración de los modelos
Se delimitó un área de amortiguamiento de 1 grado (~ 111.1 km) alrededor del punto de registro, que abarca la máxima capacidad de dispersión conocida para machos del género Euglossa (Pokorny et al., 2015). Esta área se combinó con las provincias biogeográficas para la región neotropical donde se registraron estos puntos (Morrone et al., 2022). En cuanto a los datos de fondo, se generaron 20,000 puntos aleatorios para E. viridissima, E. dilemma y E. obrima, mientras que para el resto de las especies se utilizaron todos sus puntos de fondo debido a que eran menos que el número predeterminado (E. villosa: 11,908; E. dodsoni: 15,690; E. obtusa: 18,799).
Para desarrollar el modelo de nicho por especies, se empleó el algoritmo MAXENT (Phillips et al., 2006) a través de la plataforma Wallace (Kass et al., 2018). Para las especies con 50 registros o más, se asignó 75% de los datos para el entrenamiento y 25% para la validación. En el caso de especies con menos de 20 registros, se aplicó el método de jackknife (Pearson et al., 2007). Este procedimiento implica la generación de k repeticiones, donde k es igual al número de localidades. En cada repetición, se excluye un punto de presencia distinto para la validación, realizando así k validaciones y evaluando si se predice con precisión el punto designado para la validación; posteriormente, se realiza una prueba binomial para revisar la significancia del modelo. Este enfoque se recomienda especialmente para muestras de tamaño reducido (Pearson et al., 2007; Shcheglovitova y Anderson, 2013).
Por medio de la plataforma Wallace, que emplea los paquetes de R ENMeval (Kass et al., 2021) y dismo (Hijmans et al., 2020), se llevaron a cabo diversos modelos con variados niveles de complejidad. Estos modelos abarcan distintas combinaciones (lineal [L], lineal-cuadrático [LQ], bisagra [H], lineal-cuadrático-bisagra [LQH] y lineal-cuadrático-bisagra-producto [LQHP]) y factores de regularización, en este caso se usó desde 0.5 hasta 2 en el multiplicador de regularización con incrementos de 0.5 entre cada valor. Posteriormente, se evaluaron mediante métricas como el área bajo la curva (AUC) característica operativa del receptor (ROC) (Hanley y McNeil, 1982) por iteración y en su totalidad, la tasa de omisión (OR) para evaluar la capacidad de predicción de un clasificador binario respecto a las localidades de validación (OR = 0 es indicativo de que ninguna localidad fue omitida en la predicción y un OR = 1 de que todas fueron omitidas), y por último, el criterio de información de Akaike (AIC).
Tabla 1
Registros de las especies de Euglossa analizadas en este estudio obtenidos de las distintas fuentes citadas en el texto. Se muestran los registros totales y los registros después de depurar la base de datos.
| Subgénero | Especie | Número total de registros obtenidos | Número total de registros depurados |
| Euglossa | E. dilemma E. viridissima | 626 2,828 | 85 339 |
| Dasystilbe | E. obrima E. villosa | 134 37 | 51 13 |
| Eurhytisma | E. obtusa E. dodsoni | 61 1,514 | 15 121 |
Superposición entre especies de abejas de las orquídeas
Las variables de cada especie se combinaron en una matriz única para las comparaciones, resultando en un análisis final con 20 variables ambientales y una resolución de 2.5 minutos de arco (apéndice), con el fin de que las especies se encontraran en el mismo espacio ambiental. Con el propósito de contrastar las características de nicho, se llevó a cabo un análisis de componentes principales (PCA) para cada par de especies, utilizando la plataforma Wallace (Kass et al., 2018), que se basa en el paquete ade4 (Bougeard y Dray, 2018; Chessel et al., 2004; Dray y Dufour, 2007; Dray et al., 2007; Thioulouse et al., 2018) dentro del programa R (R Core Team, 2020).
Se calculó la densidad de presencia para cada especie siguiendo a Broennimann et al. (2012), de modo que el espacio ambiental se representa en un plano que considera los 2 primeros componentes principales (PCA) y en la gráfica generada se representan las densidades y los puntos de fondo para cada píxel utilizando un enfoque de densidad de kernel. Todo a través del paquete “ecospat” (Broennimann et al., 2021) en el entorno del programa R (R Core Team, 2020) y la plataforma Wallace. El propósito de esta acción es evaluar el espacio medioambiental disponible y corregir cualquier posible sesgo de muestreo en los registros.
Finalmente, para estimar el solapamiento de nicho, se empleó la métrica de similitud D (Schoener, 1968) del paquete “ecospat” (Broennimann et al., 2021) en el entorno del programa R (R Core Team, 2020) mediante Wallace. Esta métrica genera valores entre 0 y 1, en donde valores cercanos a 1 indican una alta similitud en las condiciones ambientales para ambas especies, mientras que valores cercanos a 0 denotan lo opuesto. Por consiguiente, la métrica D está condicionada por la delimitación de la región de estudio. Asimismo, se realizó una prueba de similitud de nicho en el espacio ambiental para evaluar si el solapamiento calculado era superior o inferior a lo esperado por azar. Para ello, se realizaron 100 simulaciones (número por defecto en Wallace) para crear la distribución de frecuencias aleatoria. Si el solapamiento observado supera 95% (p < 0.05) de los datos simulados, se puede concluir que las 2 especies son más similares de lo que se esperaría por el azar.
Resultados
De los modelos generados a través de la plataforma Wallace, se eligieron aquellos que obtuvieron menor valor según el criterio de información de Akaike (AIC), estos modelos a su vez presentaban elevados valores del AUC en una gráfica de característica operativa del receptor (ROC) y bajos índices de omisión (OR) en contraste con los otros modelos desarrollados (tabla 2).
En lo que respecta a los modelos de nicho creados por especie, los modelos creados para E. dodsoni, E. viridissima, E. dilemma, E. villosa y E. obrima también presentaron valores aceptables de AUC, aunque con tasas elevadas de omisión (tabla 2). En contraste, el modelo generado para E. obtusa mostró un mal AUC y alta tasa de omisión, posiblemente debido a la escasez de registros obtenidos (tabla 2).
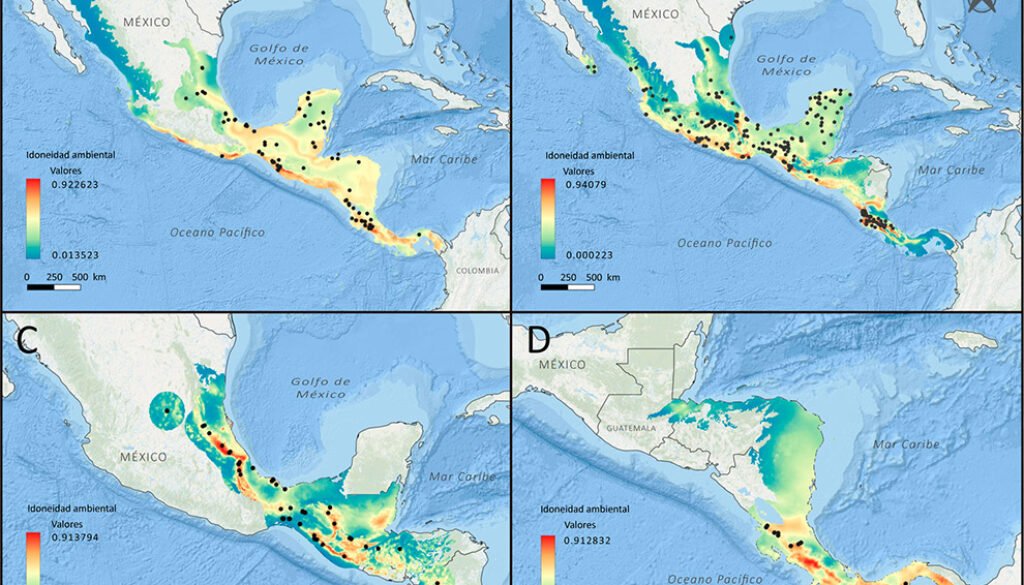
En los mapas generados por los modelos se observa una variedad de probabilidades de presencia entre las 6 especies (fig. 1). Para E. dilemma y E. viridissima se presenta una distribución potencial más extensa. En E. dilemma las zonas con mayor idoneidad ambiental se observan en la vertiente del Pacífico mexicano, península de Yucatán y principalmente en Centroamérica. En E. viridissima, entre las zonas con mayor idoneidad ambiental, destacan la franja del Pacífico (Jalisco a Chiapas), la península de Yucatán y Panamá. Por otro lado, para E. obrima las áreas de alta idoneidad se localizan en la vertiente del golfo, principalmente en el estado de Veracruz, Guatemala y parte de El Salvador y se observa un patrón más discontinuo en comparación con las especies anteriores. En E. villosa la mayor idoneidad ambiental se localiza al norte de Costa Rica del lado del Pacífico y parte de Panamá, al igual que E. obrima se observa un patrón discontinuo en las áreas de mayor idoneidad ambiental. Para E. obtusa la mayor idoneidad ambiental se localiza al sur de México y Belice. Finalmente, en el caso de E. dodsoni, las áreas de mayor idoneidad se concentran en Costa Rica y Panamá.
Tabla 2
Modelos de nicho seleccionados y su medida de evaluación para las especies de Euglossa analizadas.
| Subgénero | Especie | Modelo seleccionado | AUC | OR |
| Euglossa | E. dilemma E. viridissima | H 2 LQHP1 | 0.752 0.804 | 0.131 0.487 |
| Dasystilbe | E. obrima E. villosa | LQ 0.5 L 1.5 | 0.824 0.877 | 0.204 0.333 |
| Eurhytisma | E. obtusa E. dodsoni | LQ 2 LQH 1.5 | 0.589 0.913 | 0.214 0.260 |
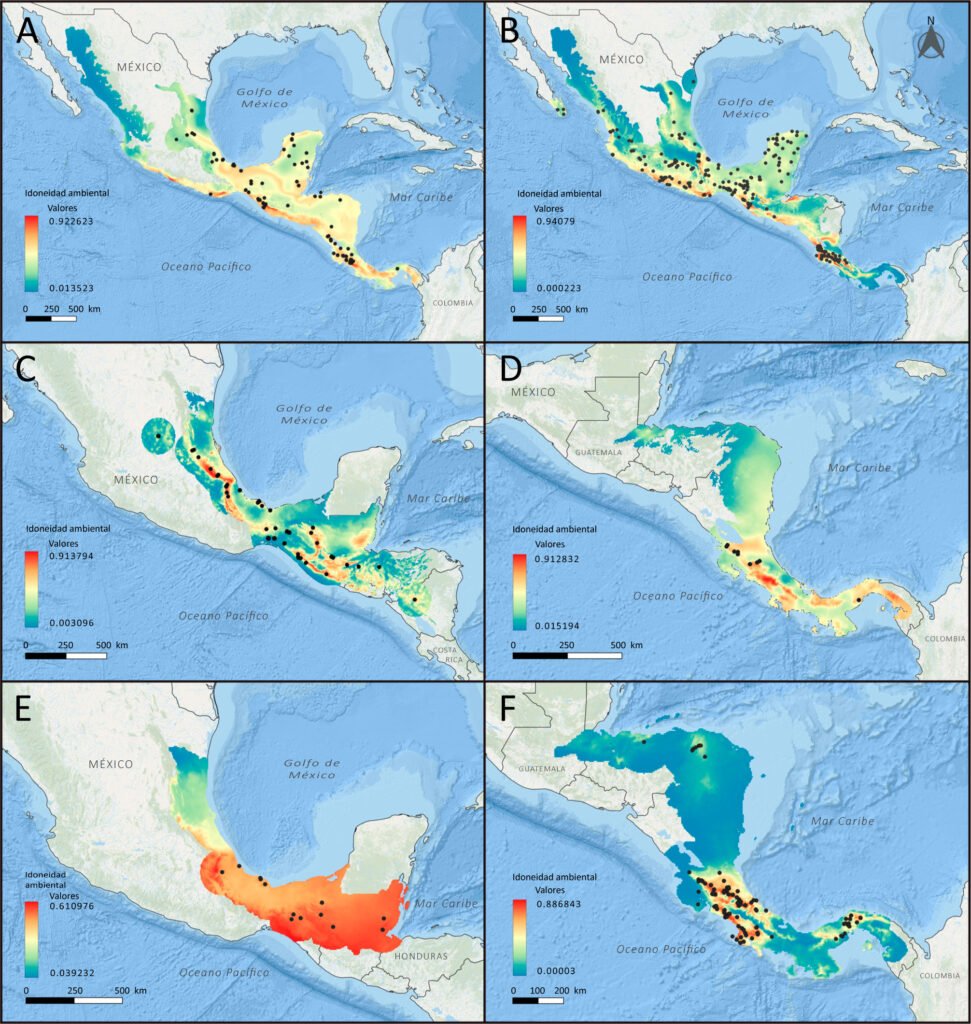
Figura 1. Mapas de los modelos de distribución generados para las especies de Euglossa. Los colores cálidos representan 0.5-1 de idoneidad ambiental de la especie, mientras que los colores fríos representan menos del 0.5 de idoneidad climática de la especie. A: Euglossa dilema; B: E. viridissima; C: E. obrima; D: E. villosa;E: E. obtusa; F: E. dodsoni.
Las 2 especies dentro del subgénero Euglossa fueron las que tuvieron mayor superposición (D = 0.51). Mientras que en las comparaciones dentro de los otros 2 subgéneros: Dasystilbe y Eurhytisma, la similitud de nicho fue baja (D = 0.01, D = 0, respectivamente) (tabla 3; fig. 2). Por lo tanto, en el subgénero Euglossa existe mayor similitud dentro del subgénero, mientras que para Dasystilbe y Eurhytisma hay mayor similitud entre subgéneros que dentro de los subgéneros (tabla 3). Para las especies alopátricas que no están estrechamente relacionadas, se observó un leve solapamiento de nicho, siendo éste el menor de todas las comparaciones (tabla 4; fig. 2). En cambio, las especies simpátricas que no están cercanamente emparentadas mostraban un amplio solapamiento de nicho (tabla 5; fig. 2).
La similitud de nichos en los subgéneros Dasystilbe (E. obrima + E. villosa) y Eurhytisma (E. obtusa + E. dodsoni) fue notablemente baja y resultó ser menor de lo esperado por el azar (p < 0.05) (tabla 3). Entre las especies alopátricas no estrechamente relacionadas, no hubo valores significativos en la prueba de similitud (p < 0.05) (tabla 4). En contraste, entre las especies simpátricas, pero no relacionadas, solo se encontraron 5 comparaciones significativas (tabla 5): E. dodsoni + E. villosa y todas las comparaciones de la especie E. viridissima.
Discusión
En este estudio se llevaron a cabo comparaciones del nicho ecológico de 3 pares de especies hermanas del género Euglossa para poner a prueba la premisa central del conservadurismo de nicho. Se encontró que el subgénero Euglossa fue el único donde se observó una mayor similitud de nicho entre sus especies hermanas y esta fue significativa. Por otro lado, los subgéneros Dasystilbe y Eurhytisma mostraron poca similitud dentro de los subgéneros, teniendo los valores más bajos en todas las comparaciones.
En relación con los modelos de nicho creados por especies, los modelos desarrollados para E. dodsoni, E. villosa, E. dilemma, E. obrima y E. viridissima mostraron un AUC aceptable pero una alta tasa de omisión (tabla 2). Por otro lado, el modelo de E. obtusa presentó tasas de omisión elevadas (tabla 2), posiblemente debido a la baja cantidad de datos disponibles (tabla 1). Para E. obtusa varios de los registros iniciales fueron excluidos por ser registros duplicados, dejando únicamente 15 registros para el modelo final, lo que representa una cantidad limitada de datos. Aunque la validación se realizó mediante el método de jackknife (Pearson et al., 2007), la cantidad de datos resulta insuficiente para garantizar la robustez del modelo.
Tabla 3
Resultados de las comparaciones de nicho entre especies hermanas de Euglossa analizadas en este estudio.
| Comparaciones entre especies hermanas | D | Similitud (p-valor) | Similitud 1→2 | Similitud 2→1 |
| E. dilemma vs. E. viridissima | 0.51 | 0.02 | 0.02 | 0.14 |
| E. obrima vs. E. villosa | 0.01 | 0.24 | 0.98 | 0.76 |
| E. dodsoni vs. E. obtusa | 0 | 0.08 | 0.79 | 0.92 |
Tabla 4
Resultados de las comparaciones de nicho entre especies alopátricas de Euglossa no cercanamente relacionadas analizadas en este estudio.
| Comparaciones entre especies alopátricas no cercanamente emparentadas | D | Similitud (p-valor) | Similitud 1→2 | Similitud 2→1 |
| E. obrima vs. E. dodsoni | 0.02 | 0.44 | 0.96 | 0.86 |
| E. villosa vs. E. obtusa | 0 | 0.27 | 0.96 | 0.99 |
Tabla 5
Resultados de las comparaciones de nicho entre especies simpátricas de Euglossa no cercanamente relacionadas analizadas en este estudio.
| Comparaciones entre especies simpátricas no cercanamente emparentadas | D | Similitud (p-valor) | Similitud 1→2 | Similitud 2→1 |
| E. dilemma vs. E. obrima | 0.24 | 0.09 | 0.20 | 0.10 |
| E. viridissima vs. E. obrima | 0.32 | 0.02 | 0.30 | 0.05 |
| E. dilemma vs. E. obtusa | 0.10 | 0.17 | 0.32 | 0 |
| E. viridissima vs. E. obtusa | 0.14 | 0.02 | 0.48 | 0 |
| E. dilemma vs. E. villosa | 0.14 | 0.09 | 0.83 | 0.04 |
| E. viridissima vs. E. villosa | 0.17 | 0.03 | 0.78 | 0 |
| E. dilemma vs. E. dodsoni | 0.22 | 0.15 | 0.64 | 0.02 |
| E. viridissima vs. E. dodsoni | 0.24 | 0.04 | 0.59 | 0.03 |
| E. obrima vs. E. obtusa | 0.17 | 0.29 | 0.48 | 0.06 |
| E. villosa vs. E. dodsoni | 0.53 | 0.02 | 0.01 | 0.42 |
En insectos, en general, existe desinformación acerca de la distribución de las especies y su taxonomía. Aunque la falta de información sobre la distribución de las especies puede tener un impacto en nuestros resultados como la fragmentación de las áreas de mayor idoneidad o la robustez de los modelos; consideramos que estos reflejan las relaciones ambientales entre las especies y pueden contribuir a comprender los patrones de especiación. A pesar de la limitada abundancia de datos, nuestros hallazgos coinciden con investigaciones previas que analizan el conservadurismo del nicho en abejas de las orquídeas (Silva et al., 2014).
Este trabajo muestra que la premisa principal del conservadurismo de nicho no se cumple en las especies hermanas en 2 de los subgéneros analizados (Dasystilbe y Eurhytisma). En el caso del subgénero Euglossa, por el contrario, se encontró la mayor similitud de entre todas las comparaciones de pares de especies hermanas en el análisis. La similitud de nicho para el par de especies puede explicarse aludiendo a varios factores y/o combinaciones de éstos, incluyendo su distribución simpátrica actual, su cercanía filogenética y su reciente divergencia estimada hace unos 150,000 años (Eltz et al., 2011), sin ser clara la influencia de ningún factor en particular. Se cree que la especiación entre ambas especies fue, principalmente, influenciada por factores ecológicos, como la preferencia química de los machos por ciertos aromas, en lugar de ser un factor geográfico (Brand et al., 2020).
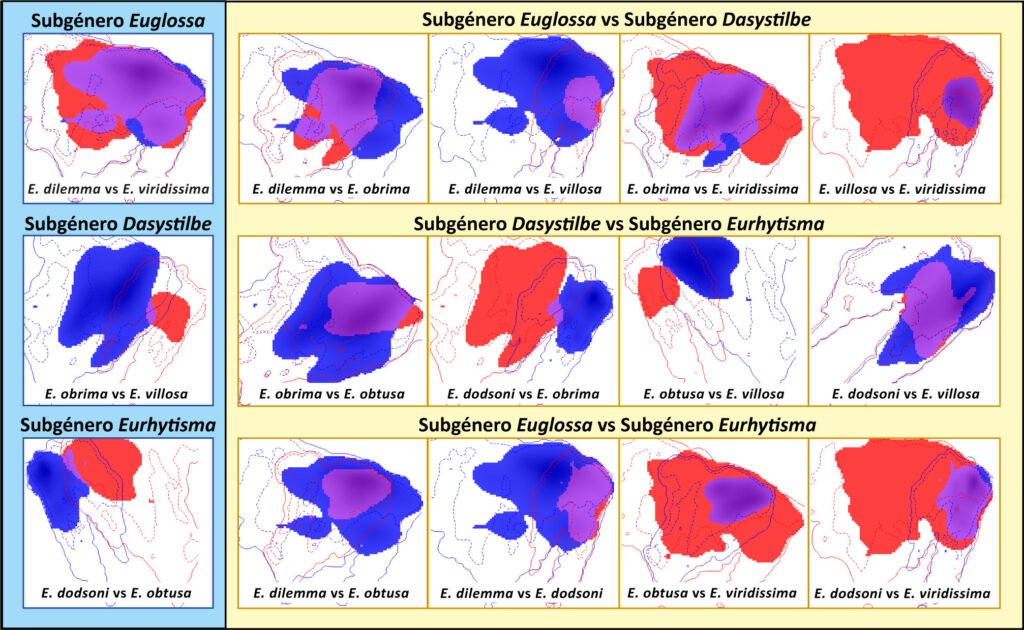
Figura 2. Comparación en el espacio ambiental de las combinaciones de pares de las especies de Euglossa analizadas. Del lado izquierdo, con fondo azul claro se encuentran las comparaciones para especies dentro del mismo subgénero. Mientras que, del lado derecho en amarillo, se muestran las comparaciones para especies de distintos subgéneros. Dentro de cada comparación, en azul rey se muestran las condiciones ambientales cubiertas por el nicho de la primera especie, en rojo las condiciones ambientales cubiertas por la segunda especie y en morado las condiciones ambientales cubiertas por ambas especies.
En cuanto a la comparación entre las especies del subgénero Euglossa y las especies de los otros 2 subgéneros, se observaron altos niveles de superposición. Resaltan las comparaciones que involucran a E. viridissima con el resto de las especies analizadas, todas con valores significativos. Euglossa viridissima tiene una distribución relativamente amplia, con reportes que sugieren posibles extensiones de rango recientes (Falcón-Brindis et al., 2018), algo similar a lo documentado para E. dilemma (Genaro et al., 2020; Skov y Wiley, 2005). La presencia y capacidad de ocupación de sitios con un amplio rango de condiciones en el caso de E. viridissima explican las similitudes significativas con las demás especies consideradas en este estudio.
Silva et al. (2014) analizaron el conservadurismo del nicho en 2 géneros de la tribu Euglossini (Eulaema y Eufriesea). Concluyeron que las especies simpátricas muestran un mayor traslape de nicho independientemente de su parentesco, a diferencia de las especies alopátricas que, aunque están más cercanamente relacionadas, presentan un menor grado de similitud de nicho. Este fenómeno no solo se observó en abejas, sino también en investigaciones con ranas de la familia Dendrobatidae (Graham et al., 2004), lagartijas del género Anolis (Losos et al., 2003) y aves del género Sylvia (Böhning-Gaese et al., 2003).
Por otro lado, existen investigaciones que respaldan la hipótesis de conservadurismo de nicho, como es el caso de ciertos grupos de plantas (Guo et al., 2013; Kolanowska, 2013; Prinzig et al., 2001), otros insectos (Peterson et al., 1999; Zhao et al., 2019), reptiles (Dowell y Hekkala, 2016; Schulte et al., 2012), anfibios (Kozak y Wiens, 2006; Muñoz-Ortiz et al., 2015), aves (Navarro-Sigüenza et al., 2020; Trujillo-Arias et al., 2018; Wang et al., 2017) y mamíferos (Peterson et al., 1999).
De acuerdo con Wiens y Graham (2005), el conservadurismo de nicho puede surgir de 4 factores clave: la selección natural, el flujo genético, la pleiotropía y la falta de variabilidad. Sin embargo, los rasgos fisiológicos (adaptaciones) que subyacen al conservadurismo de nicho están poco estudiados y pueden ser relativamente específicos de cada especie. Ellos sugieren que el estudio del conservadurismo de nicho debería centrarse en los factores que lo generan, en lugar de un debate sobre su existencia.
Los resultados obtenidos en este estudio son consistentes con investigaciones previas y refuerzan la conclusión planteada por Silva et al. (2014). En este sentido, los pares de especies hermanas en los subgéneros Dasystilbe (E. obrima + E. villosa) y Eurhytisma (E. obtusa + E. dodsoni) mostraron una menor similitud de nicho, lo cual concuerda con los estudios arriba mencionados, ya que dichas especies son actualmente alopátricas. En las comparaciones entre subgéneros. las especies alopátricas y no relacionadas mostraron baja similitud y traslape, mientras que las especies que no están cercanamente emparentadas, pero son simpátricas presentaron una mayor similitud y traslape de nicho. Un caso interesante es la similitud encontrada entre E. villosa y E. dodsoni, especies simpátricas que no están estrechamente relacionadas, en donde se observa un alto grado de similitud de nicho, aunque no fue significativo. El tamaño de la muestra puede influir en este resultado, especialmente en el caso de E. villosa, que cuenta con muy pocos registros.
Aunque se considera que la similitud de nichos encontrada en 2 de los subgéneros depende principalmente de una historia biogeográfica similar en lugar de una relación de parentesco, no se descarta que algunos factores ecológicos, como las preferencias de aroma de los machos, las tasas de competencia o las diferencias de microhábitat (Silva et al., 2014), también impacten en la dinámica temporal y espacial del nicho ecológico de las especies. Sin embargo, debido al enfoque y escala del estudio, no se puede determinar su influencia. Además, la cantidad limitada de datos utilizados, especialmente en 2 especies (E. villosa y E. obtusa) y el método empleado pudieron haber influido en los resultados obtenidos (Peterson, 2011; Warren et al., 2008).
Agradecimientos
Este proyecto fue desarrollado gracias al apoyo del programa UNAM DGAPA-PAPIIT, proyecto IN211121 y formó parte de los estudios dirigidos a la obtención del grado de Maestra en Ciencias Biológicas (Posgrado en Ciencias Biológicas, UNAM) de la primera autora, para lo cual recibió una beca de posgrado de Secihti (antes Conahcyt).
Apéndice. Capas ambientales obtenidas en diferentes bases de datos, las capas con asterisco (*) corresponden a las utilizadas en las comparaciones de superposición de pares de especies.
| Clave | Capa | Unidades | Origen |
| Bio 1* | Temperatura media anual | °C*10 | WorldClim |
| Bio 2* | Rango diurno medio (media mensual* [temp. máx.-temp. min.]) | °C*10 | WorldClim |
| Bio 3* | Isotermalidad ([BIO2 / BIO7] [100]) | °C*10 | WorldClim |
| Bio 4* | Estacionalidad de la temperatura (desv. estándar*100) | °C*10 | WorldClim |
| Bio 5* | Temperatura máxima del mes más cálido | °C*10 | WorldClim |
| Apéndice. Continúa | |||
| Clave | Capa | Unidades | Origen |
| Bio 6* | Temperatura mínima del mes más frío | °C*10 | WorldClim |
| Bio 7* | Rango anual de temperatura (Bio 5-Bio 6) | °C*10 | WorldClim |
| Bio 8* | Temperatura media del trimestre más cálido | °C*10 | WorldClim |
| Bio 9* | Temperatura media del trimestre más frío | °C*10 | WorldClim |
| Bio 10* | Precipitación anual | mm | WorldClim |
| Bio 11* | Precipitación del mes más húmedo | mm | WorldClim |
| Bio 12* | Precipitación del mes más seco | mm | WorldClim |
| Bio 13* | Estacionalidad de la precipitación (coef. var.) | mm | WorldClim |
| Bio 14 | Precipitación del trimestre más húmedo | mm | WorldClim |
| Bio 15 | Precipitación del trimestre más seco | mm | WorldClim |
| Bio 16* | Humedad específica máxima anual | kg agua/kg aire | MERRAclim |
| Bio 17* | Humedad específica máxima del mes más húmedo | kg agua/kg aire | MERRAclim |
| Bio 18* | Humedad específica máxima del mes menos húmedo | kg agua/kg aire | MERRAclim |
| Bio 19 | Estacionalidad de la humedad específica máxima (coef. var.) | kg agua/kg aire | MERRAclim |
| Bio 20 | Humedad específica máxima del trimestre más húmedo | kg agua/kg aire | MERRAclim |
| Bio 21 | Humedad específica máxima del trimestre menos húmedo | kg agua/kg aire | MERRAclim |
| Bio 22 | Humedad específica media anual | kg agua/kg aire | MERRAclim |
| Bio 23* | Humedad específica media del mes más húmedo | kg agua/kg aire | MERRAclim |
| Bio 24 | Humedad específica media del mes menos húmedo | kg agua/kg aire | MERRAclim |
| Bio 25* | Estacionalidad de la humedad específica media (coef. var.) | kg agua/kg aire | MERRAclim |
| Bio 26 | Humedad específica media del trimestre más húmedo | kg agua/kg aire | MERRAclim |
| Bio 27* | Humedad específica media del trimestre menos húmedo | kg agua/kg aire | MERRAclim |
| Bio 28 | Humedad específica mínima anual | kg agua/kg aire | MERRAclim |
| Bio 29 | Humedad específica mínima del mes más húmedo | kg agua/kg aire | MERRAclim |
| Bio 30 | Humedad específica mínima del mes menos húmedo | kg agua/kg aire | MERRAclim |
| Bio 31* | Estacionalidad de la humedad específica mínima (coef. var.) | kg agua/kg aire | MERRAclim |
| Bio 32 | Humedad específica mínima del trimestre más húmedo | kg agua/kg aire | MERRAclim |
| Bio 33 | Humedad específica mínima del trimestre menos húmedo | kg agua/kg aire | MERRAclim |
Referencias
Ascher, J. S. y Pickering, J. (2018). Discover life bee species guide and world checklist (Hymenoptera: Apoidea: Anthophila). Recuperado el 11 noviembre, 2022 de: http://www.discoverlife.org/mp/20q?guide=Apoidea_species
Böhning-Gaese, K., Schuda, M. D. y Helbig, A. J. (2003). Weak phylogenetic effects on ecological niches of Sylvia warblers. Journal of Evolutionary Biology, 16, 956–965. https://doi.org/10.1046/j.1420-9101.2003.00605.x
Bougeard, S. y Dray, S. (2018). Supervised multiblock analysis in R with the ade4 Package. Journal of Statistical Software, 86, 1–17. https://doi.org/10.18637/jss.v086.i01
Brand, P., Hinojosa-Díaz, I. A., Ayala, R., Daigle, M. Yurrita, C. L., Eltz, T. et al. (2020). The evolution of sexual signaling is linked to odorant receptor tuning in perfume-collecting orchid bees. Nature Communications, 11, 1–11. https://doi.org/10.1038/s41467-019-14162-6
Broennimann, O., Di Cola, V. y Guisan, A. (2021). ecospat: Spatial Ecology Miscellaneous Methods. R package version 3.2. https://CRAN.R–project.org/package=ecospat
Broennimann, O., Fitzpatrick, M. C., Pearman, P. B., Petitpierre, B., Pellissier, L., Yoccoz, N. G. et al. (2012). Measuring ecological niche overlap from occurrence and spatial environmental data. Global Ecology and Biogeography, 21, 481–497. https://doi.org/10.1111/j.1466-8238.2011.00698.x
Chessel, D., Dufour, A. y Thioulouse, J. (2004). The ade4 Package – I: One–Table Methods. R News, 4, 5–10.
Conabio (Comisión Nacional para el Conocimiento y Uso de la Biodiversidad). (2021). Sistema Nacional de Información sobre Biodiversidad. Registros de ejemplares. Ciudad de México, México. Recuperado el 27 febrero, 2021 de: https://www.snib.mx/
Dowell, R. y Hekkala, S. (2016). Divergent lineages and conserved niches using ecological niche modeling to examine the evolutionary patterns of the Nile monitor (Varanus niloticulus). Evolutionary Ecology, 30, 471–485. https://doi.org/10.1007/s10682-016-9818-7
Dray, S. y Dufour, A. (2007). The ade4 Package: implementing the duality diagram for ecologists. Journal of Statistical Software, 22, 1–20. https://doi.org/10.18637/jss.v022.i04
Dray, S., Dufour, A. y Chessel, D. (2007). The ade4 Package – II: Two–Table and K–Table Methods. R News, 7, 47–52.
Eliosa, H. R., Nieto, A. y Navarro, M. C. (2010). Conservadurismo filogenético del nicho ecológico un enfoque integral de la evolución. Ciencias, 98, 64–69.
Eltz, T., Fritzsch, F., Zimmermann, Y., Pech, J., Ramírez, S. R., Quezada-Euan, J. J. G. et al. (2011). Characterization of the orchid bee Euglossa viridissima (Apidae: Euglossini) and a novel cryptic sibling species, by morphological, chemical, and genetic characters. Zoological Journal of the Linnean Society, 163, 1064–1076. https://doi.org/10.1111/j.1096-3642.2011.00740.x
Engel, M. S. (2021). A key to the subgenera of the orchid bee genus Euglossa (Hymenoptera: Apidae). Entomologist’s Monthly Magazine, 157, 225–241. https://doi.org/10.31184/M00138908.1574.4093
Engel, M. S. y Rasmussen, C. (2020). Corbiculate Bees. En C. K. Starr (Ed.), Encyclopedia of Social Insects (pp. 1–9). Berlín: Springer. https://doi.org/10.1007/978-3-319-90306-4_30-1
Falcón-Brindis, A., Ayala, R., Jiménez, M. L. e Hinojosa-Díaz, I. A. (2018). A missing piece in the puzzle: the presence of Euglossa viridissima in the Baja California Peninsula (Hymenoptera, Apidae). Zookeys, 726, 15–23. https://doi.org/10.3897/zookeys.726.19876
Fick, S. E. y Hijmans, R. J. (2017). WorldClim 2: new 1 km spatial resolution climate surfaces for global land areas. International Journal of Climatology, 37, 4302–4315. https://doi.org/10.1002/joc.5086
GBIF.org (2021). Euglossa dilemma. Euglossa obrima. Euglossa dodsoni. Euglossa obtusa. Euglossa villosa. Euglossa viridissima. Recuperados el 20 julio, 2021 de: https://doi.org/10.15468/dl.xdqhq4; https://doi.org/10.15468/dl.2r57f4; https://doi.org/10.15468/dl.t6k4r6; https://doi.org/10.15468/dl.ubgt7v; https://doi.org/10.15468/dl.4xv2t2; https://doi.org/10.15468/dl.7fa7qr
Genaro, J. A., Hinojosa-Díaz, I. A. y McDowell, A. (2020). First record of the orchid bee Euglossa dilemma (Hymenoptera: Apidae) in Hispaniola, the Antilles. Insecta Mundi, 0779, 1–5.
Ghassemi-Khademi, T. (2018). New insight into the phylogeny of the orchid bees (Apidae: Euglossini). Journal of Wildlife and Biodiversity, 2, 19–35. https://doi.org/10.22120/jwb.2018.30117
Graham, C. H., Ron, S. R., Santos, J. C., Schneider, C. J. y Moritz, C. (2004). Integrating phylogenetics and environmental niche models to explore speciation mechanisms in Dendrobatid frogs. Evolution, 58, 1781–1793. https://doi.org/10.1111/j.0014-3820.2004.tb00461.x
Guo, W. Y., Lambertini, C., Li, X. Z., Meyerson, L. A. y Brix, H. (2013). Invasion of old world Phragmites australis in the new world: precipitation and temperature patterns combined with human influences redesign the invasive niche. Global Change Biology, 19, 3406–3422. https://doi.org/10.1111/gcb.12295
Hanley, J. A. y McNeil, B. J. (1982). The meaning and use of the area under a Receiver Operating Characteristic Curve (ROC). Diagnostic Radiology, 143, 29–36. https://doi.org/10.1148/radiology.143.1.7063747
Henske, J., Saleh, N. W., Chouvenc, T., Ramírez, S. R. y Eltz, T. (2023). Function of environment-derived male perfumes in orchid bees. Current Biology, 33, 2075–2080. https://doi.org/10.1016/j.cub.2023.03.060
Hijmans, R. J., Phillips, S., Leathwick, J. y Elith, J. (2020). Dismo: species distribution modeling. R package version 1.3-3. https://CRAN.R-project.org/package=dismo
Hinojosa-Díaz, I. A. y Engel, M. S. (2011). Euglossa williamsi, a new species of orchid bee from the Amazon Basin of Ecuador and Peru, with notes on its taxonomic association and biogeography (Hymenoptera, Apidae). Zookeys, 159, 49–63. https://doi.org/10.3897/zookeys.159.2239
Hinojosa-Díaz I. A., Melo G. y Engel, M. (2011). Euglossa obrima, a new species of orchid bee from Mesoamerica, with notes on the subgenus Dasystilbe Dressler (Hymenoptera, Apidae). Zookeys, 97, 11–29. https://doi.org/10.3897/zookeys.97.1106
Kass, J. M., Vilela, B., Aiello-Lammens, M. E., Muscarella, R., Merow, C. y Anderson, R. P. (2018). Wallace: a flexible platform for reproducible modeling of species niches and distributions built for community expansion. Methods in Ecology and Evolution, 9, 1151–1156. https://doi.org/10.1111/2041-210X.12945
Kass, J. M., Muscarella, R., Galante, P. J., Bohl, C. L., Pinilla-Buitrago, G. E., Boria, R. A. et al. (2021). ENMeval 2.0: redesigned for customizable and reproducible modeling of species’ niches and distributions. Methods in Ecology and Evolution, 12, 1602–1608. https://doi.org/10.1111/2041-210X.13628
Kolanowska, M. (2013). Niche conservatism and the future potential range of Epipactis helleborine (Orchidaceae). Plos One, 8, 1–8. https://doi.org/10.1371/journal.pone.0077352
Kozak, K. H. y Wiens, J. J. (2006). Does niche conservatism promote speciation? A case study in North American salamanders. Evolution, 60, 2604–2621. https://doi.org/
10.1111/j.0014-3820.2006.tb01893.x
Losos, J. B., Jackman, T. R., Larson, A., de Queiroz, K. y Rodríguez-Schettino, L. (1998). Contingency and determinism in replicated adaptive radiations of island lizards. Science, 279, 2115–2118. http://www.jstor.org/stable/2896277
Morrone, J. J., Escalante, T., Rodríguez-Tapia, G., Carmona, A., Arana, M. y Mercado-Gómez, J. D. (2022). Biogeographic regionalization of the neotropical region: new map and shapefile. Anais da Academia Brasileira de Ciencias, 94, e20211167. https://doi.org/10.1590/0001-3765202220211167
Moure, J. S. y Melo, G. A. R. (2023). Euglossini Latreille, 1802. En Moure, J. S., Urban, D. & Melo, G. A. R. (Orgs). Catalogue of Bees (Hymenoptera, Apoidea) in the Neotropical Region – online version. Disponible en: https://www.moure.cria.org.br/catalogue
Muñoz-Ortiz, A., Velásquez-Álvarez, Á. A., Guarnizo, C. E. y Crawford, A. J. (2015). Of peaks and valleys: testing the roles of orogeny and habitat heterogeneity in driving allopatry in mid-elevation frogs (Aromobatidae: Rheobates) of the northern Andes. Journal of Biogeography, 42, 193–205. https://doi.org/10.1111/JBI.12409
Navarro-Sigüenza, A. G., Almazán-Núñez, R. C., Sánchez-Ramos, L. E., Rebón-Gallardo, M. F. y Arbeláez-Cortés, E. (2020). Relict humid tropical forest in Mexico promotes differentiation in barred woodcreepers Dendrocolaptes (Aves: Furnariidae). Zootaxa, 4780, 307–323. https://doi.org/10.11646/zootaxa.4780.2.5
Pearson, R. G., Raxworthy, C. J., Nakamura, M. y Peterson, A. T. (2007). Predicting species distributions from small numbers of occurrence records: a test case using cryptic geckos in Madagascar. Journal of Biogeography, 34, 102–117. https://doi.org/10.1111/j.1365-2699.2006.01594.x
Peterson, A. T. (2011). Ecological niche conservatism: a time-structured review evidence. Journal of Biogeography, 38, 817–827. https://doi.org/10.1111/j.1365-2699.2010.02456.x
Peterson, A. T., Soberón, J. y Sánchez-Cordero, V. (1999). Conservatism of ecological niches in evolutionary time. Science, 285, 1265–1267. https://doi.org/10.1126/science.285.5431.1265
Phillips, S. J., Anderson, R. P. y Schapire, R. E. (2006). Maximum entropy modeling of species geographic distributions. Ecological Modelling, 190, 231–259. https://doi.org/10.1016/j.ecolmodel.2005.03.026
Pokorny, T., Loose, D., Dyker, G., Quezada-Euán, J. J. G. y Eltz, T. (2015). Dispersal ability of male orchid bees and direct evidence for long-range flights. Apidologie, 46, 224–237. https://doi.org/10.1007/s13592-014-0317-y
Prinzig, A., Durka, W., Klotz, S. y Brandl, F. (2001). The niche of higher plants: evidence for phylogenetic conservatism. Proceedings: Biological Sciences, 268, 2383–2389. https://doi.org/10.1098/rspb.2001.1801
Pyron, R. A., Costa, G. C., Patten, M. A. y Burbrink, F. T. (2015), Phylogenetic niche conservatism and the evolutionary
basis of ecological speciation. Biological Reviews, 90, 1248–1262. https://doi.org/10.1111/brv.12154
R Core Team (2020). R: a language and environment for statistical computing. R Foundation for Statistical Computing, Vienna, Austria. https://www.R–project.org/.
Ramírez, S. R., Roubik, D. W., Skov, C. y Pierce, N. E. (2010). Phylogeny, diversification patterns and historical biogeography of euglossine orchid bees (Hymenoptera: Apidae). Biological Journal of the Linnean Society, 100, 552–572. https://doi.org/10.1111/j.1095-8312.2010.01440.x
Roubik, D. W. y Hanson, P. (2004). Orchid bees: biology and field guide. Heredia, Costa Rica: INBio.
Schoener, T. W. (1968). The Anolis lizards of Bimini: resource partitioning in a complex fauna. Ecology, 49, 704–726. https://doi.org/10.2307/1935534
Schulte, U., Hochkirch, A., Lötters, S., Rödder, D., Schweiger, S., Weimann, T. et al. (2012). Cryptic niche conservatism among evolutionary lineages of an invasive lizard. Global Ecology and Biogeography, 21, 198–211. https://doi.org/10.1111/j.1466-8238.2011.00665.x
Shcheglovitova, M. y Anderson, R. P. (2013). Estimating optimal complexity for ecological niche models: a jackknife approach for species with small sample sizes. Ecological Modelling, 269, 9–17. https://doi.org/10.1016/j.ecolmodel.2013.08.011
Silva, D. P., Vilela, B., De Marco, P. y Nemésio, A. (2014). Using ecological niche models and niche analyses to understand speciation patterns: the case of sister neotropical orchid bees. Plos One, 9, e113246. https://doi.org/10.1371/journal.pone.0113246
Skov, C. y Wiley, J. (2005). Establishment of the neotropical orchid bee Euglossa viridissima (Hymenoptera: Apidae) in Florida. Florida Entomologist, 88, 225–227. https://doi.org/10.1653/0015-4040(2005)088[0225:EOTNOB]2.0.CO;2
Thioulouse, J., Dray, S., Dufour, A., Siberchicot, A., Jombart, T. y Pavoine, S. (2018). Multivariate Analysis of Ecological Data with ade4. Nueva York: Springer. https://doi.org/10.1007/978-1-4939-8850-1
Trujillo-Arias, N., Calderón, L., Santos, F. R., Miyaki, C. Y., Aleixo, A., Witt, C. C. et al. (2018). Forest corridors between the central Andes and the southern Atlantic Forest enabled dispersal and peripatric diversification without niche divergence in a passerine. Molecular Phylogenetics and Evolution, 128, 221–232. https://doi.org/10.1016/j.ympev.2018.08.005
Vega, G. C., Pertierra, L. R. y Olalla-Tárraga, M. A. (2018). MERRAclim, a high-resolution global dataset of remotely sensed bioclimatic variables for ecological modelling. Scientific Data, 4, 170078. https://doi.org/10.1038/sdata.2017.78
Wang, P., Liu, Y., Liu, Y., Chang, Y., Wang, N. y Zhang, Z. (2017). The role of niche divergence and geographic arrangement in the speciation of Eared Pheasants (Crossoptilon, Hodgson 1938). Molecular Phylogenetics and Evolution, 113, 1–8. https://doi.org/10.1016/j.ympev.2017.05.003
Warren, D. J., Glor, R. E. y Turelli, M. (2008). Environmental niche equivalency versus conservatism: quantitative approaches to niche evolution. Evolution, 62, 2868–2883. https://doi.org/10.1111/j.1558-5646.2008.00482.x
Wiens, J. J. y Donoghue, M. J. (2004). Historical biogeography, ecology and species richness. Trends in Ecology and Evolution, 19, 639–644. https:/doi.org/10.1016/j.tree.
2004.09.011
Wiens, J. J. y Graham, C. H. (2005). Niche conservatism: integrating evolution, ecology, and conservation biology. Annual Review of Ecology, Evolution, and Systematics, 36, 519–539. https://doi.org/10.1146/annurev.ecolsys.36.102803.095431
Zhao, Q., Zhang, H. y Wei, J. (2019). Climatic niche comparison across a cryptic species complex. PeerJ, 2019, 1–18. https://doi.org/10.7717/peerj.7042