Morfología del huevo y comportamientos de oviposición en Pseudosermyle (Phasmatodea: Diapheromeridae)
Egg morphology and oviposition techniques in Pseudosermyle (Phasmatodea: Diapheromeridae)
Ulises López-Mora a, b, *, Enrique González-Soriano a, A. Celeste Martínez-Cervantes a, b, Jorge Llorente-Bousquets c
a Universidad Nacional Autónoma de México, Instituto de Biología, Departamento de Zoología, Tercer Circuito Universitario s/n, Ciudad Universitaria, Coyoacán, 04510 Ciudad de México, México
b Universidad Nacional Autónoma de México, Posgrado en Ciencias Biológicas, Instituto de Biología, Departamento de Zoología, Tercer Circuito Universitario s/n, Ciudad Universitaria, Coyoacán, 04510 Ciudad de México, México
c Universidad Nacional Autónoma de México, Facultad de Ciencias, Departamento de Biología Evolutiva, Museo de Zoología Alfonso L. Herrera, Circuito Exterior s/n, Ciudad Universitaria, Coyoacán, 04510 Ciudad de México, México
* Autor para correspondencia: nxitl00@gmail.com (U. López-Mora)
Recibido: 30 julio 2025; aceptado: 04 octubre 2025
Resumen
Pseudosermyle es el género de insectos palo con mayor riqueza en América del Norte; muestra una distribución desde el sur de los EUA hasta América Central, desafortunadamente ha sido poco estudiado. En el presente trabajo se realiza la primera aproximación en extenso a la morfología del huevo en Pseudosermyle respecto a su microestructura, con el empleo de microscopía electrónica de barrido (MEB), así como el análisis de componentes principales para determinar la utilidad de las medidas estandarizadas que se utilizan en la descripción de huevos, además de su ornamentación. Se encontraron 4 patrones en el huevo de Pseudosermyle, entre los que se incluyen 3 tipos de oviposición: liberación, adheridos al sustrato y formación de ooteca. Esto sugiere que podría tratarse de géneros distintos bajo una posible subtribu. Además, la ornamentación del huevo es lo suficientemente distinta para reconocer diferentes especies. Por lo tanto, se debe analizar la importancia de estos caracteres en la descripción de especies de Pseudosermyle.
Palabras clave: Diapheromerinae; Diapheromerini; Phasmida; MEB; Insectos palo
Abstract
Pseudosermyle is the genus of stick insects with the greatest diversity in North America, with a range extending from the southern USA to Central America; unfortunately, it has been poorly studied. In this work, we present the first comprehensive analysis of the egg morphology in Pseudosermyle in relation to ultrastructure, using scanning electron microscopy, along with principal component analysis to evaluate the effectiveness of the standardized measurements used in the egg descriptions, as well as the ornamentation. We identified 4 general patterns in Pseudosermyle eggs corresponding to 3 different oviposition techniques: dropping, attaching to substrate and forming oothecae. These patterns suggest the possibility of recognizing different genera within a putative subtribe. Additionally, the ornamentation is sufficiently distinct to differentiate among species. Thus, we emphasize the importance of these characters in the description of species of Pseudosermyle.
Keywords: Diapheromerinae; Diapheromerini; Phasmida; SEM; Stick insects
Introducción
El orden Phasmatodea comprende organismos denominados insectos palo, hoja o corteza. Por lo general se reconocen por su cuerpo alargado y cilíndrico o deprimido; es menos frecuente encontrar formas más robustas (Bradler y Buckley, 2018). Su coloración varía en distintos matices del castaño al verde, aunque existen algunos con coloraciones aposemáticas (rojo, amarillo o azul). En la etapa adulta ninguno de estos insectos mide menos de 2 cm de longitud (Seiler et al., 2006). Una característica notoria es su cripsis con la vegetación, que en conjunto con comportamientos especializados, como la catalepsia e imitación del balanceo de las hojas y el follaje durante el día (Bradler y Buckley, 2018), les permiten pasar inadvertidos frente a sus depredadores. Sus huevos se asemejan a semillas de las plantas donde habitan (Severin, 1910).
La ootaxonomía de Phasmatodea se estandarizó con los trabajos de Clark (1976a, b, 1979) y Sellick (1994, 1997a, b, 1998). A partir de entonces, el huevo se ha incluido en las descripciones de sus especies (Allred et al., 1986; Conle et al., 2007; López-Mora y Llorente-Bousquets, 2023) y también se han efectuado trabajos utilizando el microscopio electrónico de barrido (MEB) para el análisis de las microestructuras y la textura de la cápsula en especies pertenecientes a los géneros Agathemera Stål, 1875, Anisomorpha Gray, 1835, Bacillus Berthold, 1827, Burria Brunner von Wattenwyl, 1900, Carausius Stål, 1875, Clonopsis Pantel, 1915, Heteronemia Gray, 1835, Lonchodes Gray, 1835, Megaphasma Caudell, 1903, Orxines Stål, 1875, Paraprisopus Redtenbacher, 1906, Ramulus Saussure, 1862, Sipyloidea Brunner von Wattenwyl, 1893, Timema Scudder, 1895 y Xeropsis Redtenbacher, 1906 (Allred et al., 1986; Camousseight y Bustamante, 1991; Jintsuet al., 2010; Mazzini y Scali, 1977, 1980, 1983; Mazzini et al., 1982, 1984, 1992; Scali y Mazzini, 1977, 1981, 1982, 1983; Stark y Lentz, 1986). En particular, la textura de la cápsula y la ornamentación del opérculo han resultado ser muy útiles en la diferenciación de especies cercanamente relacionadas (Mazzini et al., 1982, 1992; Scali y Mazzini, 1981), incluso para diferenciar híbridos (Mazzini et al., 1984). En suma, los trabajos previos han concluido en la importancia de los estudios con MEB y microscopia óptica para la diferenciación entre especies cercanamente relacionadas en Phasmatodea y posibles híbridos.
Pseudosermyle Caudell, 1903 es el género más diverso en México y América del Norte, con 26 especies en total (de Luna, 2022; López-Mora y Llorente-Bousquets, 2018). Sin embargo, solo se conocen 4 ilustraciones, que no son de microestructura del huevo, para 3 especies: Pseudosermyle tridens (Burmeister, 1838), ilustrada por Kaup (1871) y Zompro (2001); P. truncata Caudell, 1903, por Caudell (1914) y P. phalangiphora Conle, Hennemann et Fontana, 2007, por ellos mismos. Al observar las imágenes de estas 3 especies se advierten diferencias significativas en las formas de la cápsula y la lámina micropilar, que no han sido evaluadas en su microestructura y son relevantes para distinguir especies.
Nuestro objetivo fue realizar una exploración más extensa sobre la morfología coriónica a nivel de microestructura utilizando MEB, incorporando 11 especies más de Pseudosermyle, así como analizar su empleo a nivel genérico y específico al reconocer jerarquías entre los caracteres que se utilizan para describir a las especies.
Materiales y métodos
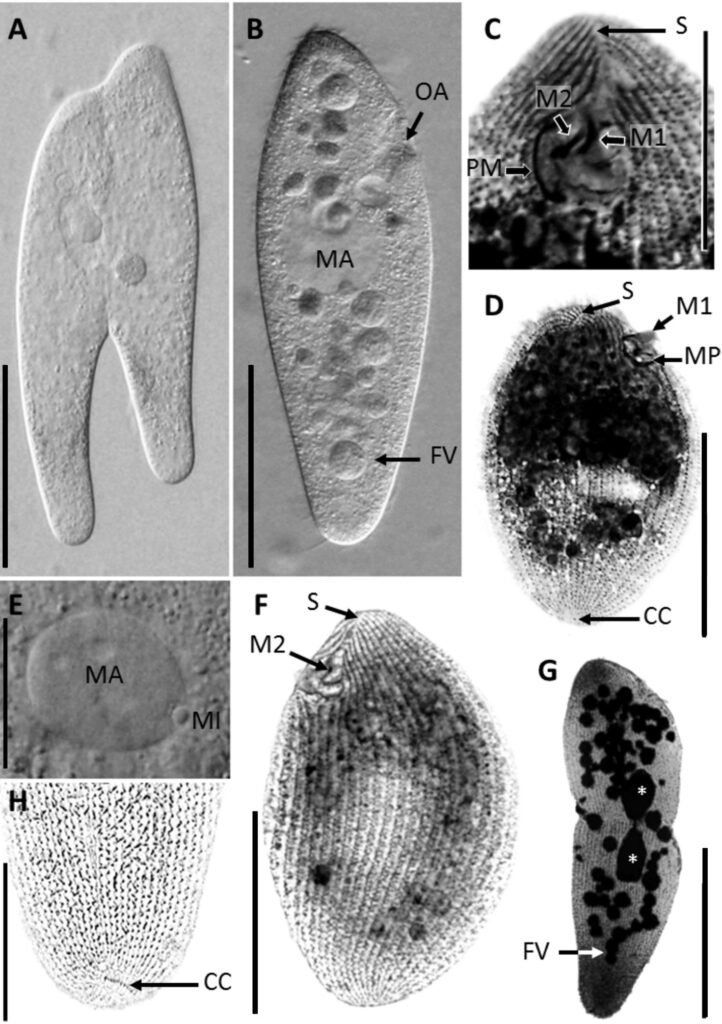
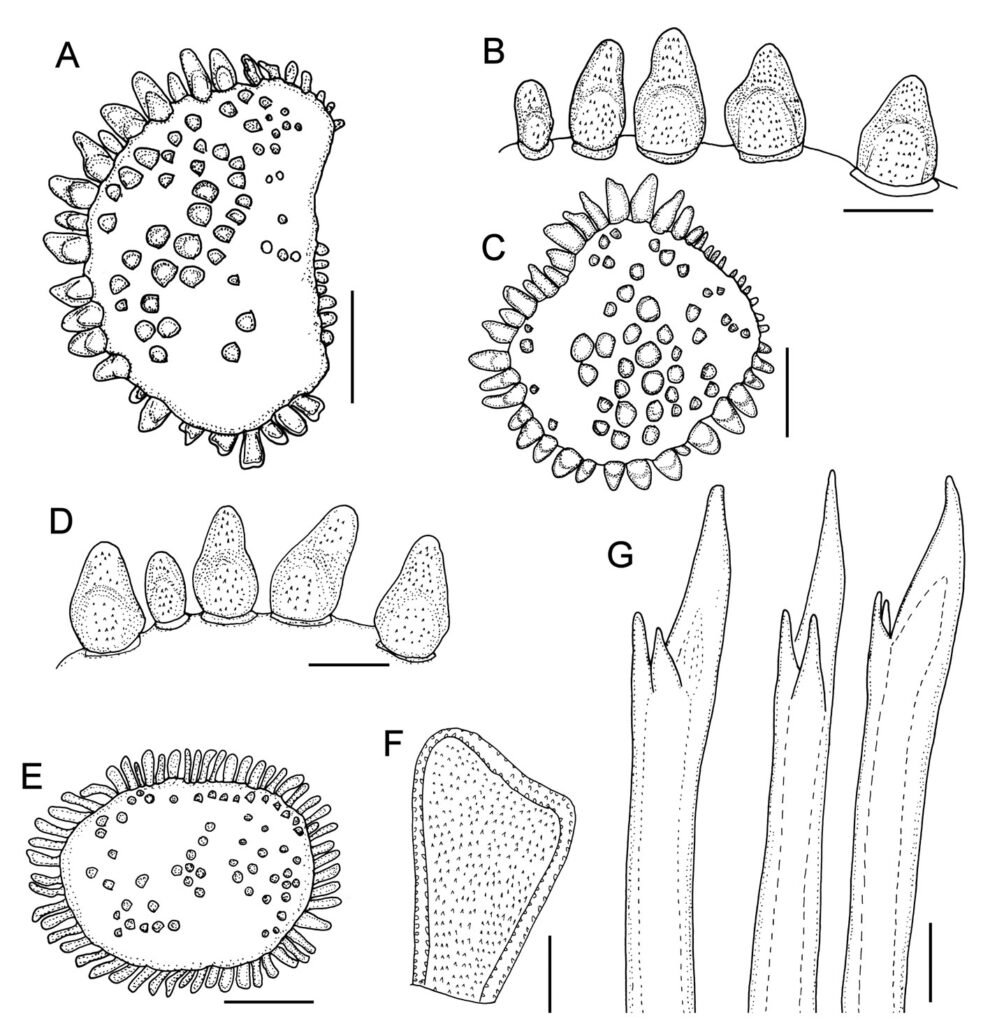
Los acrónimos y abreviaturas de las colecciones son: CNIN = Colección Nacional de Insectos, Instituto de Biología, UNAM; MZFC = Museo de Zoología Alfonso L. Herrera, Facultad de Ciencias, UNAM. Estructuras coriónicas: H = altitud de la cápsula; L = longitud de la cápsula; mpi = lámina micropilar interna; mpl = longitud de la lámina micropilar; mpw = amplitud de la lámina micropilar, NM = lámina micropilar interna abierta con línea media; oph = altura del opérculo, opw = amplitud del opérculo; PO = lámina micropilar interna paralela sin línea media; W = amplitud de cápsula; %h/l = índice de elongación, %w/h = índice de compresión.
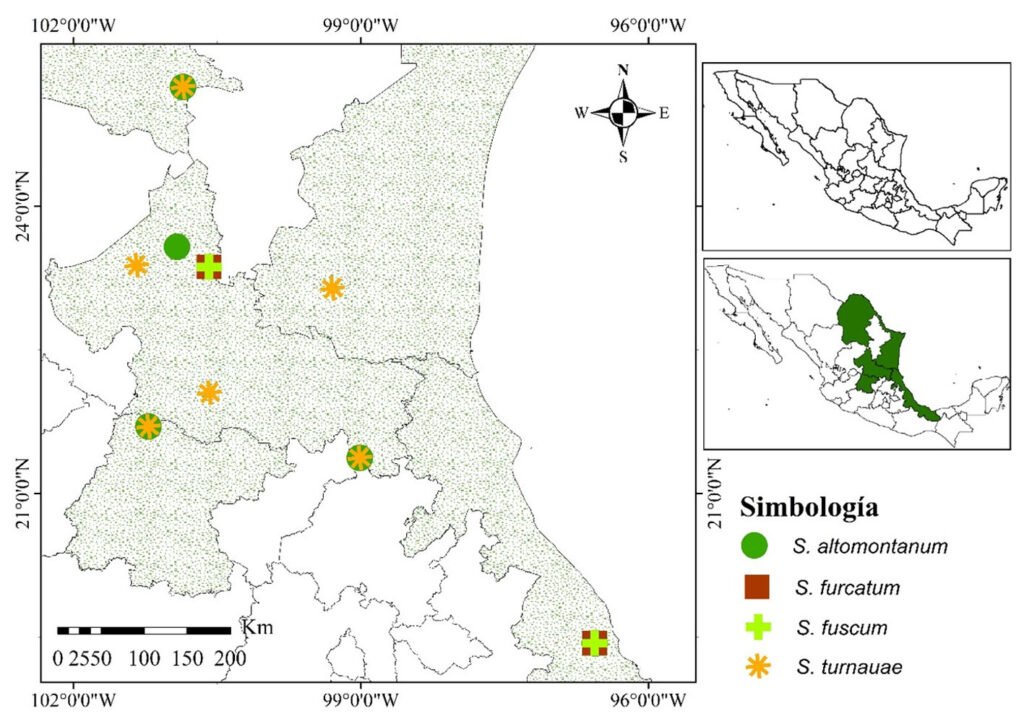
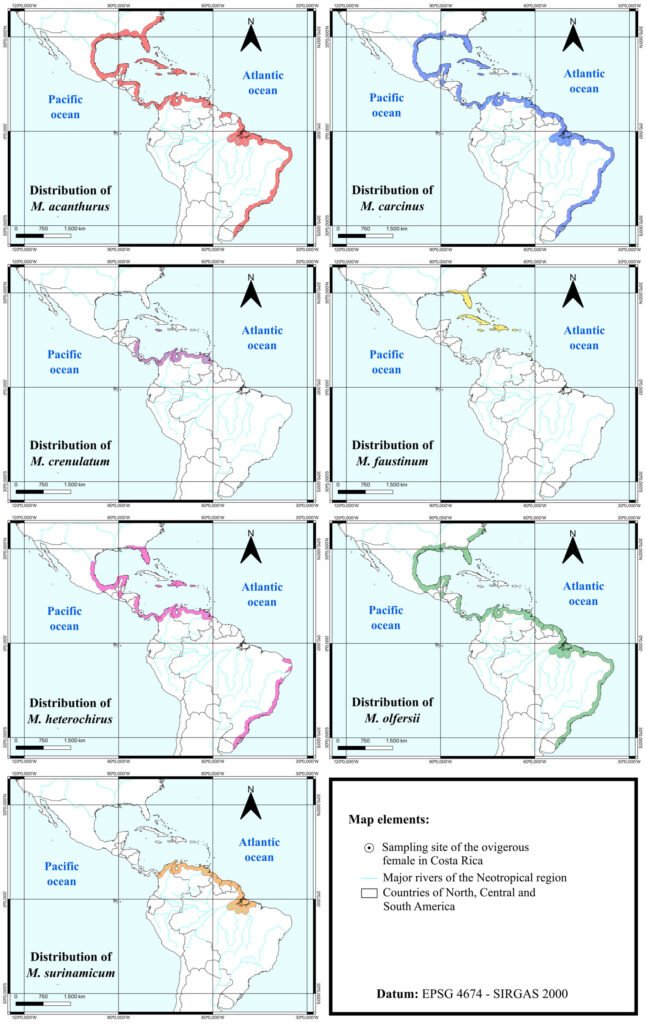
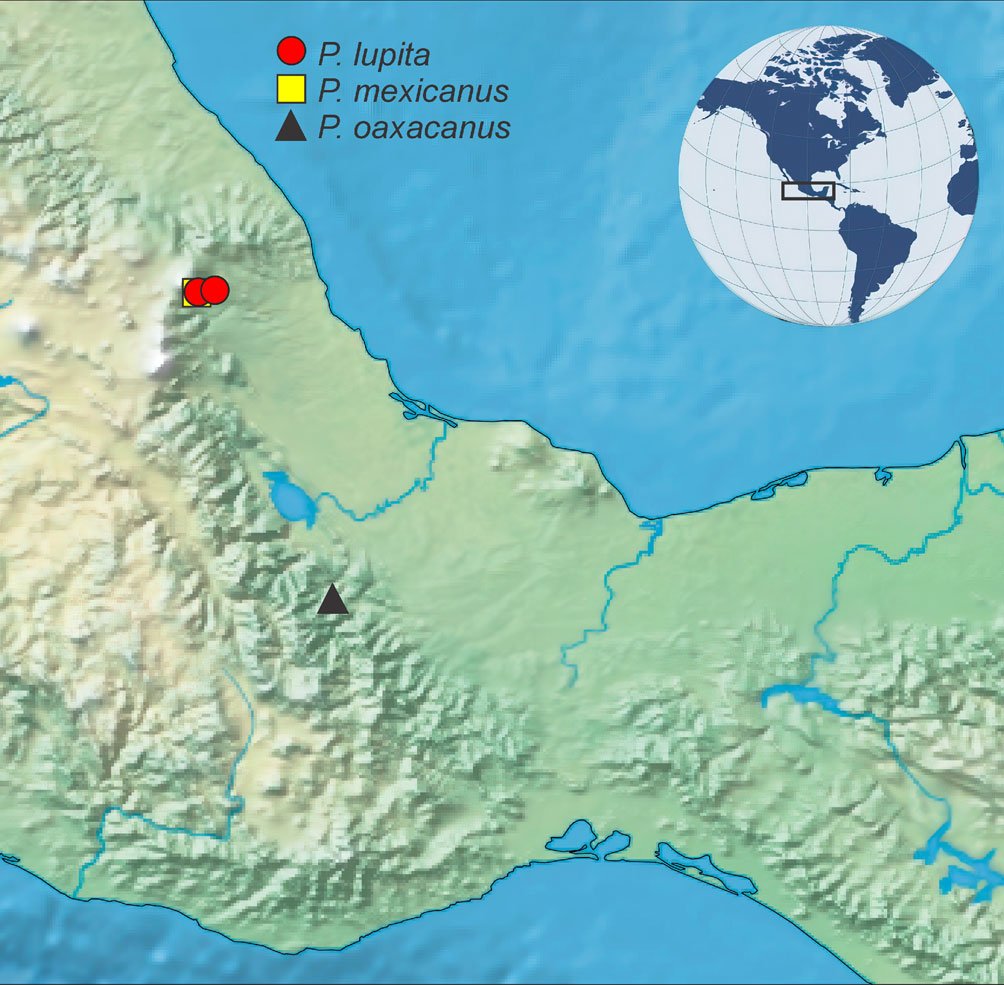
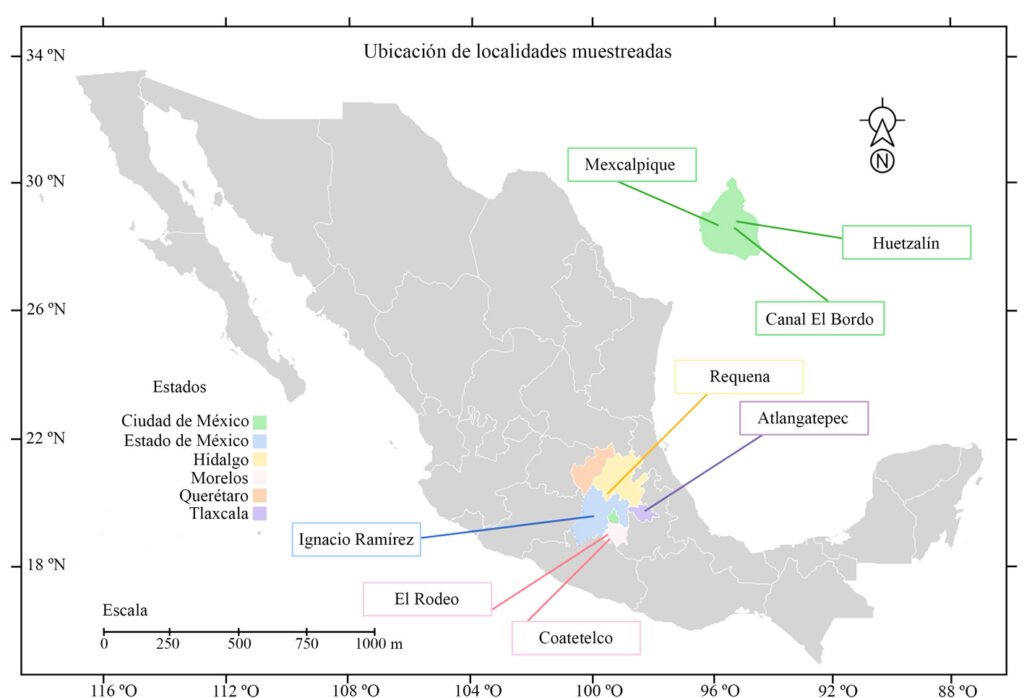
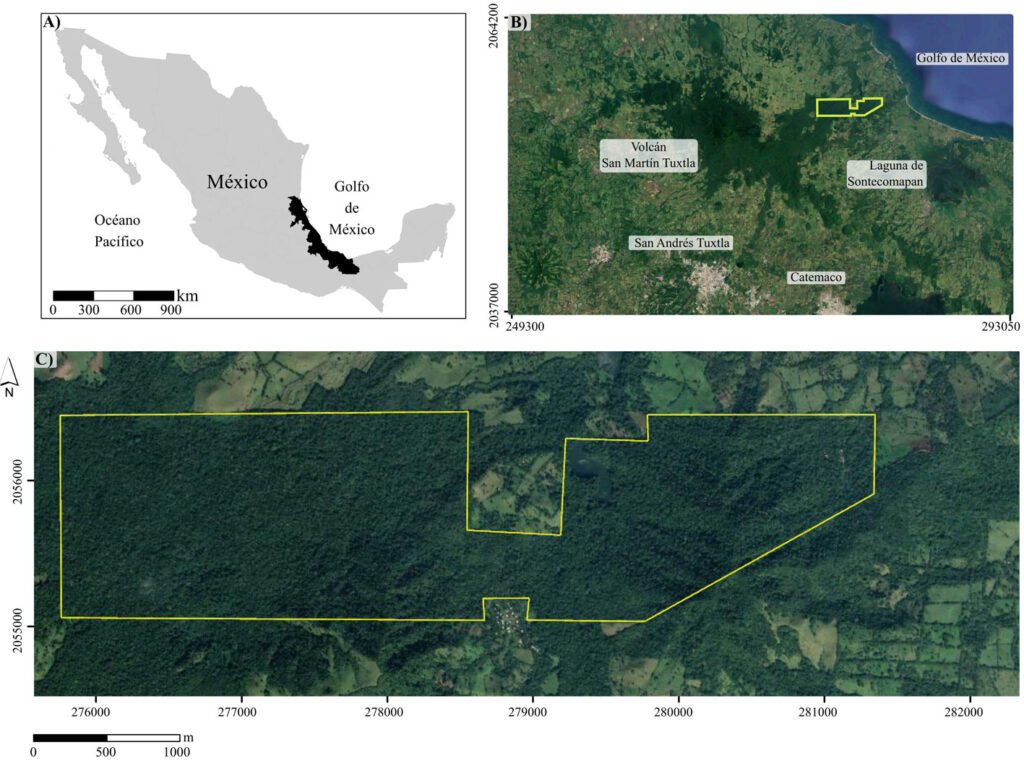
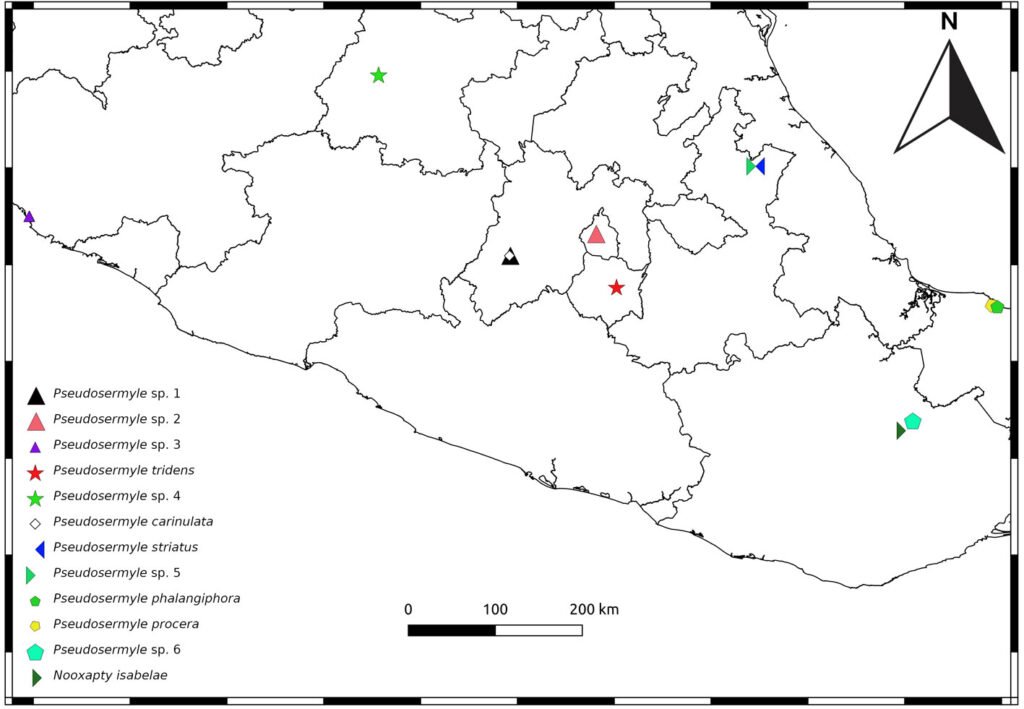
Se recolectaron 44 machos y 61 hembras en distintas localidades (fig. 1, tabla 1) y se depositaron en la CNIN y MZFC (tabla 2), Nooxapty isabelae se revisó de los ejemplares tipos depositados en las colecciones por López-Mora y Llorente-Bousquets (2023) (tabla 2). Los ejemplares que se obtuvieron de crianza aún no se depositan en colección alguna, pues se están utilizando para otro tipo de estudios. Los puntos de recolecta se muestran en un mapa (fig. 1) obtenido con QGIS 3.8.1-Zanzibar (QGIS, 2019). Para obtener los huevos, se seleccionaron 22 hembras de distintas especies (tabla 3), el número de hembra varió entre las especies pues algunas no sobrevivieron al traslado, se mantuvieron en cautiverio y aisladas entre sí (dentro de diferentes contenedores) con las siguientes condiciones: temperatura de 20-22 °C, humedad relativa 60-80%, alimentación con base en Galinsoga sp. (Asteraceae) que se colocó en frascos con agua. Estuvieron bajo ciclos de luz y oscuridad correspondientes a los presentados en la CDMX durante el lapso que estuvieron cautivas; se intentaron replicar las condiciones de temperatura y humedad tomadas en campo con un termohigrómetro digital PEAKMETER PM6508. Los organismos se identificaron comparando la morfología de adultos (machos y hembras) y el tipo de oviposición, en particular con las fotografías e ilustraciones de Brock et al. (2019), estos datos fueron cualitativos y no se incluyeron en el análisis de componentes principales (PCA). Para Nooxapty isabelae López-Mora et Llorente-Bousquets, 2023 se examinaron los huevos de la serie tipo y se usó como grupo externo. Se observaron y midieron en total 255 huevos de 22 hembras de 12 especies (tabla 3) bajo un microscopio Olympus SZX12, con ocular de reglilla micrométrica y un objetivo Olympus DF PL 1.5 X-4. Se efectuaron las mediciones de los huevos acorde con Sellick (1997b); los datos se presentan en las tablas 4-9 y en las diagnosis se expresan las cifras bajo los siguientes parámetros estadísticos: n = tamaño de la muestra, promedio ± desviación estándar (valor mínimo-valor máximo) en las descripciones.
Tabla 1
Localidades de recolecta de las distintas especies de insectos palo, el orden es alfabético por estado.
| Localidad | Longitud | Latitud | Especies |
| REPSA, Coyoacán, Ciudad de México, México | 19.317634 | -99.184854 | Pseudosermyle sp. 2 |
| Arriba cueva, Valle de Bravo, Estado de México | 19.09248 | -100.07218 | Pseudosermyle sp. 1 |
| Bajo mesa, Valle de Bravo, Estado de México, México | 19.0861 | -100.07665 | Pseudosermyle carinulata |
| Villa Esmeralda, Silao, Guanajuato, México | 20.95367 | -101.43361 | Pseudosermyle sp. 4 |
| EBCH, La Huerta, Jalisco, México | 19.49931 | -105.04484 | Pseudosermyle sp. 3 |
| Cruz Verde, Ayala, Morelos, México | 18.760174 | -98.976098 | Pseudosermyle tridens |
| Curva Choápam-Latani, Santiago Choápam, Oaxaca, México | 17.377754 | -95.916254 | Pseudosermyle sp. 6 |
| Curva 1 Amatepec-Chinantequilla, Totontepec Villa de Morelos, Oaxaca, México | 17.28485 | -95.988362 | Nooxapty isabelae |
| Camino a Tzinacapan, Cuetzalan, Puebla, México | 20.016558 | -97.53983 | Pseudosermyle striatus Psudosermyle sp. 5 |
| EBTLT, San Andrés Tuxtla, Veracruz, México | 18.5860833 | -95.0755 | Pseudosermyle phalangiphora Pseudosermyle procera |
Tabla 2
Organismos revisados y depositados en las colecciones por especie, sexo y huevos indicando el voucher. Para Nooxapty isabelae se indican los ejemplares revisados. En Núm. de especímenes se separan los ejemplares depositados y revisados (primera cifra) de los revisados (segunda cifra) por un símbolo de más “+”.
| Especie | CNIN | MZFC | ||||
| Machos | Hembras | Huevos | Machos | Hembras | Huevos | |
| Pseudosermyle sp. 1 | PHMX351-354, 356-358 | PHMX26 | PHMX125 | PHMX349-350, 355, 426 | ||
| Tabla 2. Continúa | ||||||
| Especie | CNIN | MZFC | ||||
| Machos | Hembras | Huevos | Machos | Hembras | Huevos | |
| Pseudosermyle sp. 2 | PHMX307-308, 311, 314-322 | PHMX72-75, 78-79 | PHMX76-77, 80 | PHMX304-306, 309-310, 312-313 | ||
| Pseudosermyle sp. 3 | PHMX467-468 | PHMX469-471 | PHMX324, 327-328 | PHMX323, 325-326 | ||
| P. tridens | PHMX678 | PHMX679-680 | PHMX332-337, 341, 343-348, 616-618 | PHMX329-331, 338-340, 342 | ||
| Pseudosermyle sp. 4 | PHMX91, 93 | PHMX94-100 | PHMX362-365, 367-373, 423-425 | PHMX54-56, 90, 92 | PHMX57-62 | PHMX359-361, 366 |
| P. carinulata | PHMX160-163 | PHMX164-165, 168, 653 | PHMX420-421 | PHMX416-419, 422 | ||
| P. striata | PHMX81-85 | PHMX86-89 | PHMX262-270, 272-273, 277-288, 292-300, 302-303 | PHMX463 | PHMX462, PHMX464-465 | PHMX259-261, 271, 274-276, 289-291, 301 |
| Pseudosermyle sp. 5 | PHMX27 | PHMX378-388 | PHMX1-2, 11-12 | PHMX4-6, 13 | PHMX374-377 | |
| P. phalangiphora | PHMX101-102, 135, 148, 155 | PHMX103-107, 146-147, 149 | PHMX172-183, 188-198, 203-213 | PHMX169-171, 184-187, 199-202 | ||
| P. procera | PHMX108-110, 136-137, 151, 156-157 | PHMX111-114, 150, 152-154, | PHMX217-228, 232-243, 248-258 | PHMX214-216, 229-231, 244-247 | ||
| Pseudosermyle sp. 6 | PHMX681 | PHMX405-415 | PHMX401-404 | |||
| Nooxapty isabelae | PHMX117, 119 | PHMX115 | PHMX389-393, 399-400 | PHMX118 | PHMX116 | PHMX394-398 |
| Núm. especímenes | 27+2 | 38+1 | 179+7 | 17+1 | 23+1 | 70+5 |
Tabla 3
Especies de Phasmatodea revisadas, número de hembras por especie tentativamente bajo el género Pseudosermyle y número de huevos por hembra revisados.
| Especies de Phasmatodea revisadas | Clave | Huevos por hembra | ||
| Nombre | Clave de ♀ | Núm. de ♀ | ||
| Pseudosermyle sp. 1 | PtgVB | U | 1 | 11 |
| Pseudosermyle sp. 2 | PtgDF | G1 G2 | 1 2 | 5 14 |
| Pseudosermyle sp. 3 | Pch | F1 F2 | 1 2 | 3 3 |
| P. tridens | PtrMor | T1 T2 | 1 2 | 10 10 |
| Tabla 3. Continúa | ||||
| Especies de Phasmatodea revisadas | Clave | Huevos por hembra | ||
| Nombre | Clave de ♀ | Núm. de ♀ | ||
| Pseudosermyle sp. 4 | PtrGto | U | 1 | 15 |
| P. carinulata | Pca | C1 C2 | 1 2 | 5 2 |
| P. striata | Pst | S1 S2 S3 | 1 2 3 | 15 15 15 |
| Pseudosermyle sp. 5 | PspF | U | 1 | 15 |
| P. phalangiphora | Pph | H1 H2 H3 | 1 2 3 | 15 15 15 |
| P. procera | Ppr | P1 P2 P3 | 1 2 3 | 15 15 15 |
| Pseudosermyle sp. 6 | Poax | U | 1 | 15 |
| N. isabelae | Nisa | U | 1 | 12 |
| Total: 12 spp. | — | — | 22 | 255 |
Para asociar machos con hembras que no se encontraban en cópula en el campo, se realizaron los siguientes pasos: a) se observaron los machos con los cuales copulaban las hembras en cautiverio; b) se separaron los huevos por morfología y hembra; c) éstos se incubaron por separado; d) cuando eclosionaron, las ninfas se mantuvieron en terrarios separados; e) se obtuvieron adultos y se comparó la morfología con la presentada por los parentales; f) cuando se obtienen machos y hembras de la misma hembra se corrobora si la morfología que presentan es similar a la de los parentales y se deduce qué machos parentales coinciden; g) se observa que los machos copulen con las hembras correspondientes con la morfología materna; y h) se compara la morfología coriónica de los huevos de las hembras hijas con las parentales para corroborar la correspondencia. Estos pasos permiten discernir cuando hay especies del mismo género que se encuentran en el mismo sitio, o cuando desconocemos la correspondencia entre sexos en los insectos palo de una localidad.
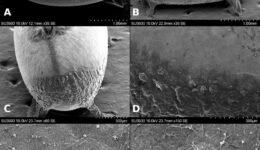
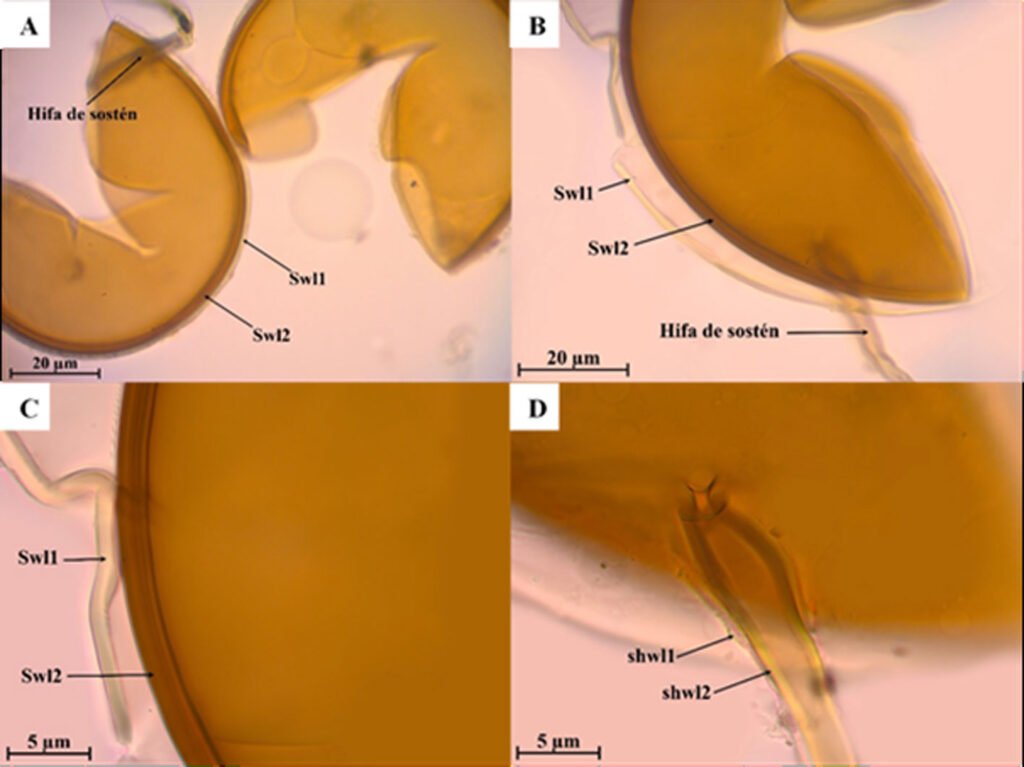
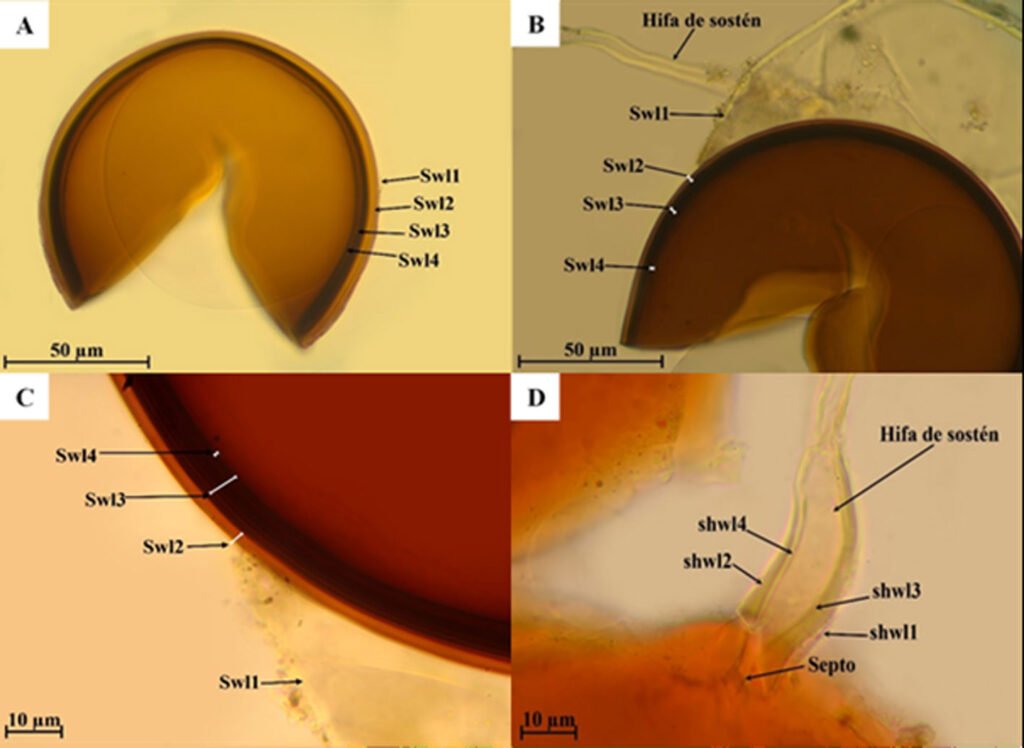
Se tomaron micrografías con una cámara de 8MP LEICA DFC490 adaptada a un microscopio LEICA Z16 AP0A y obtenidas con Leica Application Suite. Éstas se procesaron con GIMP 2.8.22 (GNU). Se llevaron a cabo observaciones bajo el MEB, los huevos se procesaron modificando el método de Nieves-Uribe et al. (2021) de la siguiente manera: serie descendente de etanol, 10 min en cada uno (96% → 70% → 50% → 30% → 10%) → H2O destilada (10 min) → jabón biológico (agitación manual constante) → Sonicar por 10 seg en 2 lapsos de 5 seg (con un sonicador modelo: Bronson 200) → enjuagar en agua destilada → agua destilada (10 min) → serie ascendente de etanol, 10 min en cada uno (10% → 30% → 50% → 70% → 96%) → dejar evaporar el alcohol (30 min. aprox.) → montar la muestra → dejar secar por 2 días en un recipiente hermético con una bolsita de silica gel (2 días). Las muestras se cubrieron en la ionizadora 19Quorum 150R ES en 2 ciclos de 20 min cada uno y se observaron bajo un microscopio Hitachi SU3500. Las abreviaturas en las medidas del huevo siguen la nomenclatura de Sellick (1997b, c, 1998). Las estructuras descritas y propuestas para el huevo se ilustran en la figura 2. Se siguió la nomenclatura de texturas de Harris (1979) para las descripciones de microestructura, en este caso solo se midieron las estructuras de 1 huevo por especie por el costo elevado de la técnica; éste corresponde con el huevo ilustrado en las micrografías obtenidas con el microscopio estereoscópico Leica. Es importante señalar que el nivel de detalle que obtuvimos permite documentar que las estructuras (v. gr. arrugas, espinas, gránulos) presentan textura, que se describe en ocasiones con frases que parecen contradictorias (v. gr. arrugas lisas, gránulos con espinas), pero se acompañan de imágenes.
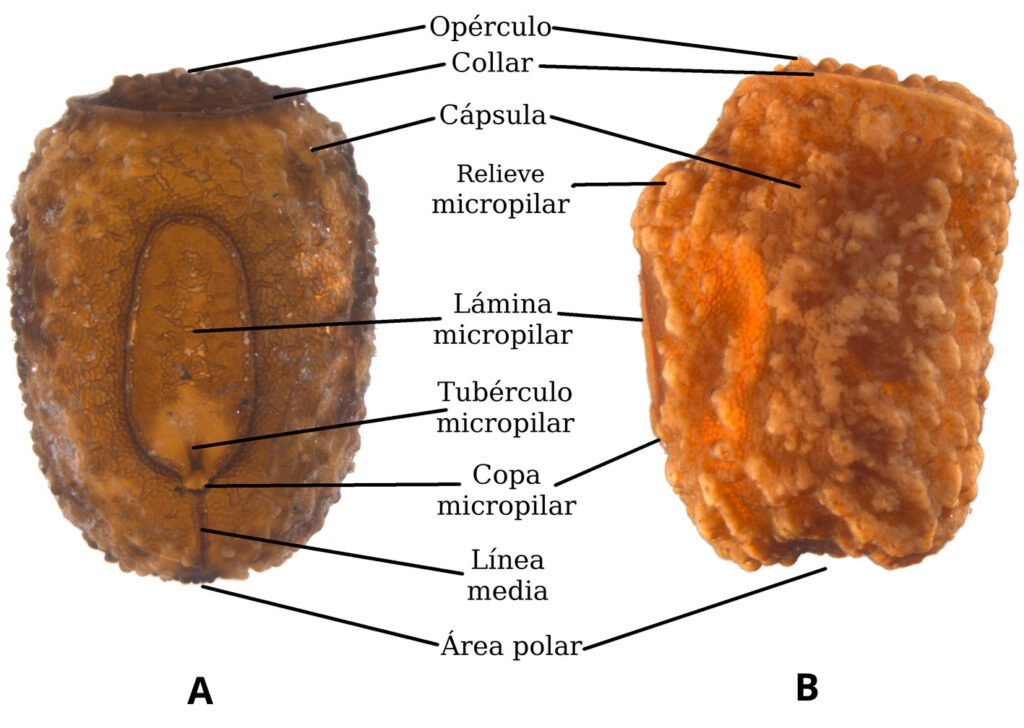
Tabla 4
Medidas en micras (μm) de cada huevo de P. phalangiphora utilizadas para el PCA.
| Clave | Medidas de huevo | ||||||
| L | W | H | mpl | mpw | oph | opw | |
| PphH1-1 | 2,774 | 1,752 | 1,971 | 876 | 474.5 | 1,423.5 | 1,131.5 |
| PphH1-2 | 2,737.5 | 1,752 | 1,898 | 912.5 | 474.5 | 1,350.5 | 1,058.5 |
| PphH1-3 | 2,664.5 | 1,533 | 1,788.5 | 912.5 | 511 | 1,350.5 | 1,095 |
| PphH1-4 | 2,701 | 1,715.5 | 1,898 | 876 | 474.5 | 1,460 | 1,131.5 |
| PphH1-5 | 2,628 | 1,679 | 1,861.5 | 949 | 511 | 1,460 | 1,095 |
| PphH1-6 | 2,847 | 1,715.5 | 1,898 | 766.5 | 511 | 1,460 | 1,204.5 |
| PphH1-7 | 2,737.5 | 1,679 | 1,861.5 | 766.5 | 511 | 1,496.5 | 1,095 |
| PphH1-8 | 2,847 | 1,788.5 | 1,861.5 | 912.5 | 438 | 1,423.5 | 1,168 |
| PphH1-9 | 2,774 | 1,642.5 | 1,861.5 | 803 | 511 | 1,460 | 1,204.5 |
| PphH1-10 | 2,774 | 1,679 | 1,861.5 | 876 | 547.5 | 1,350.5 | 1,095 |
| PphH1-11 | 2,810.5 | 1,679 | 1,934.5 | 839.5 | 438 | 1,460 | 1,168 |
| PphH1-12 | 2,847 | 1,752 | 1,861.5 | 803 | 474.5 | 1,460 | 1,168 |
| PphH1-13 | 2,737.5 | 1,715.5 | 1,861.5 | 766.5 | 474.5 | 1,460 | 1,131.5 |
| PphH1-14 | 2,664.5 | 1,642.5 | 1,861.5 | 839.5 | 474.5 | 1,387 | 1,058.5 |
| PphH1-15 | 2,920 | 1,788.5 | 1,934.5 | 912.5 | 511 | 1,496.5 | 1,168 |
| PphH2-1 | 2,372.5 | 1,387 | 1,496.5 | 839.5 | 474.5 | 1,350.5 | 1,058.5 |
| PphH2-2 | 2,555 | 1,679 | 1,752 | 803 | 438 | 1,715.5 | 1,387 |
| PphH2-3 | 2,555 | 1,569.5 | 1,642.5 | 912.5 | 438 | 1,533 | 1,314 |
| PphH2-4 | 2,591.5 | 1,898 | 1,861.5 | 766.5 | 438 | 1,752 | 1,387 |
| PphH2-5 | 2,555 | 1,606 | 1,825 | 766.5 | 401.5 | 1,606 | 1,277.5 |
| PphH2-6 | 2,591.5 | 1,606 | 1,825 | 766.5 | 438 | 1,642.5 | 1,387 |
| PphH2-7 | 2,664.5 | 1,642.5 | 1,825 | 766.5 | 438 | 1,642.5 | 1,387 |
| PphH2-8 | 2,555 | 1,679 | 1,861.5 | 803 | 438 | 1,642.5 | 1,277.5 |
| PphH2-9 | 2,591.5 | 1,642.5 | 1,825 | 949 | 547.5 | 1,606 | 1,241 |
| PphH2-10 | 2,628 | 1,642.5 | 1,788.5 | 693.5 | 438 | 1,533 | 1,314 |
| PphH2-11 | 2,628 | 1,496.5 | 1,679 | 839.5 | 511 | 1,460 | 1,168 |
| PphH2-12 | 2,591.5 | 1,606 | 1,752 | 839.5 | 438 | 1,606 | 1,314 |
| PphH2-13 | 2,591.5 | 1,496.5 | 1,715.5 | 839.5 | 401.5 | 1,460 | 1,277.5 |
| PphH2-14 | 2,591.5 | 1,679 | 1,788.5 | 730 | 438 | 1,423.5 | 1,350.5 |
| PphH2-15 | 2,664.5 | 1,715.5 | 2,007.5 | 912.5 | 438 | 1,715.5 | 1,423.5 |
| PphH3-1 | 2,774 | 1,642.5 | 1,898 | 803 | 474.5 | 1,387 | 1,095 |
| PphH3-2 | 2,664.5 | 1,642.5 | 1,825 | 803 | 474.5 | 1,387 | 1,095 |
| PphH3-3 | 2,664.5 | 1,642.5 | 1,788.5 | 839.5 | 511 | 1,314 | 1,058.5 |
| PphH3-4 | 2,737.5 | 1,642.5 | 1,825 | 766.5 | 547.5 | 1,387 | 1,095 |
| PphH3-5 | 2,628 | 1,679 | 1,788.5 | 803 | 511 | 1,350.5 | 1,058.5 |
| PphH3-6 | 2,737.5 | 1,642.5 | 1,788.5 | 803 | 511 | 1,314 | 1,095 |
| PphH3-7 | 2,774 | 1,642.5 | 1,825 | 803 | 511 | 1,387 | 1,095 |
| Tabla 4. Continúa | |||||||
| Clave | Medidas de huevo | ||||||
| L | W | H | mpl | mpw | oph | opw | |
| PphH3-8 | 2,737.5 | 1,679 | 1,825 | 876 | 511 | 1,460 | 1,095 |
| PphH3-9 | 2,701 | 1,679 | 1,861.5 | 803 | 547.5 | 1,350.5 | 1,022 |
| PphH3-10 | 2,701 | 1,642.5 | 1,788.5 | 766.5 | 438 | 1,350.5 | 1,095 |
| PphH3-11 | 2,701 | 1,606 | 1,898 | 839.5 | 547.5 | 1,496.5 | 1,131.5 |
| PphH3-12 | 2,701 | 1,642.5 | 1,861.5 | 876 | 547.5 | 1,496.5 | 1,095 |
| PphH3-13 | 2,664.5 | 1,606 | 1,825 | 839.5 | 438 | 1,350.5 | 1,204.5 |
| PphH3-14 | 2,737.5 | 1,642.5 | 1,752 | 803 | 474.5 | 1,350.5 | 1,095 |
| PphH3-15 | 2,774 | 1,679 | 1,788.5 | 876 | 438 | 1,168 | 1,058.5 |
Tabla 5
Medidas en μm de cada huevo de Pseudosermyle procera utilizadas para el PCA.
| Clave | Medidas de huevo | ||||||
| L | W | H | mpl | mpw | oph | opw | |
| PprP1-1 | 2,737.5 | 1,825 | 1,934.5 | 693.5 | 292 | 1,496.5 | 1,241 |
| PprP1-2 | 2,774 | 1,788.5 | 1,934.5 | 730 | 292 | 1,460 | 1,241 |
| PprP1-3 | 2,737.5 | 1,788.5 | 1,934.5 | 657 | 255.5 | 1,423.5 | 1,168 |
| PprP1-4 | 2,737.5 | 1,679 | 1,861.5 | 693.5 | 292 | 1,423.5 | 1,168 |
| PprP1-5 | 2,555 | 1,606 | 1,788.5 | 730 | 328.5 | 1,314 | 1,095 |
| PprP1-6 | 2,664.5 | 1,642.5 | 1,861.5 | 657 | 292 | 1,350.5 | 1,204.5 |
| PprP1-7 | 2,737.5 | 1,752 | 1,934.5 | 730 | 255.5 | 1,387 | 1,131.5 |
| PprP1-8 | 2,737.5 | 1,788.5 | 1,934.5 | 730 | 292 | 1,314 | 1,131.5 |
| PprP1-9 | 2,737.5 | 1,715.5 | 1,934.5 | 730 | 292 | 1,460 | 1,204.5 |
| PprP1-10 | 2,737.5 | 1,752 | 1,971 | 693.5 | 255.5 | 1,387 | 1,131.5 |
| PprP1-11 | 2,664.5 | 1,715.5 | 1,898 | 693.5 | 255.5 | 1,387 | 1,095 |
| PprP1-12 | 2,810.5 | 1,788.5 | 1,898 | 693.5 | 292 | 1,387 | 1,095 |
| PprP1-13 | 2,701 | 1,752 | 1,934.5 | 657 | 255.5 | 1,350.5 | 1,095 |
| PprP1-14 | 2,810.5 | 1,752 | 1,934.5 | 766.5 | 292 | 1,460 | 1,168 |
| PprP1-15 | 2,810.5 | 1,679 | 1,934.5 | 693.5 | 292 | 1,460 | 1,131.5 |
| PprP2-1 | 2,774 | 1,715.5 | 1,861.5 | 693.5 | 365 | 1,350.5 | 1,204.5 |
| PprP2-2 | 2,664.5 | 1,788.5 | 2,044 | 657 | 365 | 1,423.5 | 1,095 |
| PprP2-3 | 2,737.5 | 1,679 | 1,971 | 584 | 328.5 | 1,569.5 | 1,131.5 |
| PprP2-4 | 2,737.5 | 1,715.5 | 1,898 | 620.5 | 365 | 1,387 | 1,131.5 |
| PprP2-5 | 2,737.5 | 1,752 | 1,898 | 693.5 | 365 | 1,496.5 | 1,131.5 |
| PprP2-6 | 2,701 | 1,679 | 1,861.5 | 693.5 | 328.5 | 1,387 | 1,204.5 |
| PprP2-7 | 2,774 | 1,715.5 | 1,898 | 620.5 | 365 | 1,460 | 1,095 |
| PprP2-8 | 2,737.5 | 1,715.5 | 1,934.5 | 730 | 365 | 1,460 | 1,168 |
| Tabla 5. Continúa | |||||||
| Clave | Medidas de huevo | ||||||
| L | W | H | mpl | mpw | oph | opw | |
| PprP2-9 | 2,701 | 1,715.5 | 1,934.5 | 657 | 328.5 | 1,460 | 1,168 |
| PprP2-10 | 2,774 | 1,752 | 1,934.5 | 657 | 365 | 1,423.5 | 1,241 |
| PprP2-11 | 2,737.5 | 1,715.5 | 1,898 | 730 | 401.5 | 1,460 | 1,168 |
| PprP2-12 | 2,810.5 | 1,715.5 | 1,898 | 730 | 328.5 | 1,423.5 | 1,131.5 |
| PprP2-13 | 2,664.5 | 1,679 | 1,861.5 | 620.5 | 292 | 1,460 | 1,131.5 |
| PprP2-14 | 2,664.5 | 1,679 | 1,861.5 | 657 | 365 | 1,387 | 1,131.5 |
| PprP2-15 | 2,810.5 | 1,679 | 1,898 | 693.5 | 365 | 1,387 | 1,168 |
| PprP3-1 | 2,737.5 | 1,788.5 | 2,007.5 | 730 | 401.5 | 1,569.5 | 1,241 |
| PprP3-2 | 2,628 | 1,788.5 | 1,898 | 730 | 401.5 | 1,460 | 1,204.5 |
| PprP3-3 | 2,737.5 | 1,825 | 2,007.5 | 657 | 438 | 1,569.5 | 1,277.5 |
| PprP3-4 | 2,701 | 1,788.5 | 1,971 | 730 | 401.5 | 1,533 | 1,241 |
| PprP3-5 | 2,628 | 1,825 | 2,007.5 | 657 | 365 | 1,569.5 | 1,241 |
| PprP3-6 | 2,701 | 1,788.5 | 1,934.5 | 657 | 401.5 | 1,496.5 | 1,204.5 |
| PprP3-7 | 2,701 | 1,788.5 | 1,934.5 | 657 | 401.5 | 1,533 | 1,241 |
| PprP3-8 | 2,591.5 | 1,788.5 | 1,971 | 620.5 | 365 | 1,496.5 | 1,168 |
| PprP3-9 | 2,701 | 1,788.5 | 1,971 | 693.5 | 438 | 1,569.5 | 1,168 |
| PprP3-10 | 2,591.5 | 1,788.5 | 1,971 | 620.5 | 401.5 | 1,642.5 | 1,241 |
| PprP3-11 | 2,737.5 | 1,752 | 1,934.5 | 657 | 438 | 1,569.5 | 1,241 |
| PprP3-12 | 2,774 | 1,825 | 2,007.5 | 730 | 401.5 | 1,569.5 | 1,277.5 |
| PprP3-13 | 2,701 | 1,715.5 | 2,044 | 620.5 | 401.5 | 1,533 | 1,277.5 |
| PprP3-14 | 2,628 | 1,825 | 2,007.5 | 693.5 | 401.5 | 1,533 | 1,204.5 |
| PprP3-15 | 2,664.5 | 1,825 | 2,007.5 | 657 | 401.5 | 1,642.5 | 1,277.5 |
Tabla 6
Medidas en μm de cada huevo de Pseudosermyle striata utilizadas para el PCA.
| Clave | Medidas de huevo | ||||||
| L | W | H | mpl | mpw | oph | opw | |
| PstS1-1 | 2,263.8 | 1,470 | 1,675.8 | 1,234.8 | 529.2 | 1,029 | 882 |
| PstS1-2 | 2,352 | 1,587.6 | 1,734.6 | 1,234.8 | 529.2 | 1,146.6 | 1,029 |
| PstS1-3 | 2,293.2 | 1,528.8 | 1,705.2 | 1,205.4 | 529.2 | 1,087.8 | 940.8 |
| PstS1-4 | 2,352 | 1,558.2 | 1,646.4 | 1,205.4 | 529.2 | 1,087.8 | 1,029 |
| PstS1-5 | 2,116.8 | 1,528.8 | 1,705.2 | 1,058.4 | 529.2 | 1,176 | 999.6 |
| PstS1-6 | 2,175.6 | 1,499.4 | 1,705.2 | 1,087.8 | 588 | 1,117.2 | 970.2 |
| PstS1-7 | 2,234.4 | 1,470 | 1,646.4 | 1,117.2 | 558.6 | 1,146.6 | 970.2 |
| PstS1-8 | 2,263.8 | 1,528.8 | 1,646.4 | 1,058.4 | 558.6 | 1,176 | 1029 |
| Tabla 6. Continúa | |||||||
| Clave | Medidas de huevo | ||||||
| L | W | H | mpl | mpw | oph | opw | |
| PstS1-9 | 2,175.6 | 1,470 | 1,675.8 | 1,087.8 | 588 | 1,146.6 | 999.6 |
| PstS1-10 | 2,087.4 | 1,499.4 | 1,705.2 | 1,029 | 558.6 | 1,117.2 | 999.6 |
| PstS1-11 | 2,175.6 | 1,440.6 | 1,646.4 | 1,058.4 | 529.2 | 1,146.6 | 970.2 |
| PstS1-12 | 2,116.8 | 1,470 | 1,705.2 | 1,087.8 | 529.2 | 1,117.2 | 911.4 |
| PstS1-13 | 2,116.8 | 1,499.4 | 1,675.8 | 1,176 | 529.2 | 1,117.2 | 940.8 |
| PstS1-14 | 2,146.2 | 1,558.2 | 1,675.8 | 1,117.2 | 529.2 | 1,058.4 | 940.8 |
| PstS1-15 | 2,205 | 1,499.4 | 1,646.4 | 1,087.8 | 588 | 1,087.8 | 911.4 |
| PstS2-1 | 2,322.6 | 1,558.2 | 1,705.2 | 1,029 | 529.2 | 1,087.8 | 940.8 |
| PstS2-2 | 2,293.2 | 1,558.2 | 1,705.2 | 1,117.2 | 588 | 1,058.4 | 970.2 |
| PstS2-3 | 2,263.8 | 1,528.8 | 1,646.4 | 999.6 | 529.2 | 1,087.8 | 940.8 |
| PstS2-4 | 2,263.8 | 1,352.4 | 1,528.8 | 1,058.4 | 558.6 | 999.6 | 911.4 |
| PstS2-5 | 2,175.6 | 1,499.4 | 1,646.4 | 911.4 | 529.2 | 1,087.8 | 940.8 |
| PstS2-6 | 2,322.6 | 1,558.2 | 1,734.6 | 1,058.4 | 529.2 | 1,087.8 | 940.8 |
| PstS2-7 | 2,263.8 | 1,411.2 | 1,734.6 | 1,058.4 | 558.6 | 1,117.2 | 970.2 |
| PstS2-8 | 2,205 | 1,558.2 | 1,675.8 | 1,029 | 558.6 | 1,087.8 | 940.8 |
| PstS2-9 | 2,352 | 1,558.2 | 1,734.6 | 1,205.4 | 499.8 | 1,087.8 | 970.2 |
| PstS2-10 | 2,381.4 | 1,558.2 | 1,675.8 | 1,087.8 | 558.6 | 1,029 | 940.8 |
| PstS2-11 | 2,263.8 | 1,499.4 | 1,617 | 970.2 | 558.6 | 1,058.4 | 911.4 |
| PstS2-12 | 2,234.4 | 1,499.4 | 1,675.8 | 1,087.8 | 558.6 | 1,029 | 911.4 |
| PstS2-13 | 2,293.2 | 1,470 | 1,646.4 | 1,176 | 529.2 | 1,058.4 | 911.4 |
| PstS2-14 | 2,175.6 | 1,411.2 | 1,558.2 | 970.2 | 529.2 | 1,029 | 882 |
| PstS2-15 | 2,116.8 | 1,323 | 1,499.4 | 999.6 | 558.6 | 970.2 | 852.6 |
| PstS3-1 | 2,146.2 | 1,440.6 | 1,587.6 | 999.6 | 470.4 | 999.6 | 911.4 |
| PstS3-2 | 2,116.8 | 1,440.6 | 1,675.8 | 940.8 | 441 | 1,058.4 | 793.8 |
| PstS3-3 | 2,175.6 | 1,352.4 | 1,528.8 | 940.8 | 558.6 | 940.8 | 852.6 |
| PstS3-4 | 2,175.6 | 1,470 | 1,499.4 | 970.2 | 470.4 | 999.6 | 911.4 |
| PstS3-5 | 2,146.2 | 1,440.6 | 1,587.6 | 999.6 | 529.2 | 999.6 | 940.8 |
| PstS3-6 | 2,028.6 | 1,440.6 | 1,587.6 | 999.6 | 470.4 | 1,058.4 | 911.4 |
| PstS3-7 | 2,146.2 | 1,440.6 | 1,617 | 940.8 | 441 | 1,029 | 911.4 |
| PstS3-8 | 2,205 | 1,528.8 | 1,617 | 911.4 | 470.4 | 1,058.4 | 970.2 |
| PstS3-9 | 2,116.8 | 1,470 | 1,558.2 | 970.2 | 470.4 | 1,029 | 911.4 |
| PstS3-10 | 2,175.6 | 1,499.4 | 1,646.4 | 911.4 | 499.8 | 1,029 | 940.8 |
| PstS3-11 | 2,087.4 | 1,411.2 | 1,470 | 852.6 | 529.2 | 999.6 | 882 |
| PstS3-12 | 2,087.4 | 1,470 | 1,528.8 | 911.4 | 499.8 | 999.6 | 911.4 |
| PstS3-13 | 2,175.6 | 1,470 | 1,528.8 | 940.8 | 529.2 | 1,029 | 911.4 |
| PstS3-14 | 2,352 | 1,558.2 | 1,764 | 1,146.6 | 529.2 | 1,146.6 | 999.6 |
| PstS3-15 | 2,410.8 | 1,528.8 | 1,705.2 | 1,264.2 | 529.2 | 1,117.2 | 1,058.4 |
Tabla 7
Medidas en μm de cada huevo de Pseudosermyle carinulata, Pseudosermyle tridens, Pseudosermyle sp. 4, Pseudosermyle sp. 5 utilizadas para el PCA.
| Clave | Medidas de huevo | ||||||
| L | W | H | mpl | mpw | oph | opw | |
| PtrGtoU-1 | 3,580.2 | 1,285.2 | 1,514.7 | 642.6 | 596.7 | 872.1 | 688.5 |
| PtrGtoU-2 | 3,626.1 | 1,239.3 | 1,560.6 | 642.6 | 550.8 | 872.1 | 688.5 |
| PtrGtoU-3 | 3,626.1 | 1,377 | 1,606.5 | 642.6 | 596.7 | 872.1 | 688.5 |
| PtrGtoU-4 | 3,626.1 | 1,377 | 1,468.8 | 688.5 | 596.7 | 872.1 | 688.5 |
| PtrGtoU-5 | 3,580.2 | 1,285.2 | 1,560.6 | 734.4 | 550.8 | 826.2 | 734.4 |
| PtrGtoU-6 | 3,580.2 | 1,331.1 | 1,560.6 | 688.5 | 550.8 | 872.1 | 688.5 |
| PtrGtoU-7 | 3,672 | 1,331.1 | 1,514.7 | 688.5 | 596.7 | 826.2 | 734.4 |
| PtrGtoU-8 | 3,672 | 1,377 | 1,422.9 | 688.5 | 550.8 | 872.1 | 642.6 |
| PtrGtoU-9 | 3,672 | 1,377 | 1,514.7 | 688.5 | 550.8 | 872.1 | 688.5 |
| PtrGtoU-10 | 3,580.2 | 1,377 | 1,377 | 459 | 459 | 872.1 | 642.6 |
| PtrGtoU-11 | 3,580.2 | 1,285.2 | 1,422.9 | 321.3 | 229.5 | 872.1 | 688.5 |
| PtrGtoU-12 | 3,672 | 1,331.1 | 1,422.9 | 596.7 | 459 | 826.2 | 688.5 |
| PtrGtoU-13 | 3,580.2 | 1,239.3 | 1,422.9 | 688.5 | 550.8 | 872.1 | 734.4 |
| PtrGtoU-14 | 3,534.3 | 1,331.1 | 1,514.7 | 642.6 | 596.7 | 826.2 | 688.5 |
| PtrGtoU-15 | 3,488.4 | 1,331.1 | 1,606.5 | 688.5 | 596.7 | 872.1 | 734.4 |
| PtrMorT1-1 | 3,488.4 | 1,285.2 | 1,422.9 | 596.7 | 504.9 | 734.4 | 780.3 |
| PtrMorT1-2 | 3,626.1 | 1,331.1 | 1,514.7 | 504.9 | 504.9 | 734.4 | 780.3 |
| PtrMorT1-3 | 3,717.9 | 1,377 | 1,514.7 | 550.8 | 504.9 | 734.4 | 780.3 |
| PtrMorT1-4 | 3,580.2 | 1,331.1 | 1,468.8 | 504.9 | 504.9 | 780.3 | 780.3 |
| PtrMorT1-5 | 3,534.3 | 1,377 | 1,468.8 | 550.8 | 504.9 | 780.3 | 826.2 |
| PtrMorT1-6 | 3,672 | 1,331.1 | 1,468.8 | 550.8 | 504.9 | 734.4 | 780.3 |
| PtrMorT1-7 | 3,580.2 | 1,331.1 | 1,377 | 459 | 504.9 | 734.4 | 734.4 |
| PtrMorT1-8 | 3,580.2 | 1,377 | 1,377 | 596.7 | 504.9 | 642.6 | 734.4 |
| PtrMorT1-9 | 3,442.5 | 1,331.1 | 1,422.9 | 550.8 | 550.8 | 780.3 | 826.2 |
| PtrMorT1-10 | 3,442.5 | 1,239.3 | 1,377 | 550.8 | 550.8 | 780.3 | 826.2 |
| PtrMorT2-1 | 3,549.6 | 1,326 | 1,433.1 | 540.6 | 515.1 | 744.6 | 785.4 |
| PtrMorT2-2 | 3,488.4 | 1,239.3 | 1,422.9 | 688.5 | 550.8 | 734.4 | 780.3 |
| PtrMorT2-3 | 3,626.1 | 1,147.5 | 1,468.8 | 642.6 | 367.2 | 734.4 | 734.4 |
| PtrMorT2-4 | 3,442.5 | 1,147.5 | 1,331.1 | 688.5 | 550.8 | 734.4 | 780.3 |
| PtrMorT2-5 | 3,717.9 | 1,285.2 | 1,514.7 | 688.5 | 550.8 | 734.4 | 780.3 |
| PtrMorT2-6 | 3,717.9 | 1,239.3 | 1,468.8 | 688.5 | 550.8 | 734.4 | 734.4 |
| PtrMorT2-7 | 3,626.1 | 1,239.3 | 1,422.9 | 688.5 | 596.7 | 688.5 | 780.3 |
| PtrMorT2-8 | 3,717.9 | 1,285.2 | 1,468.8 | 642.6 | 550.8 | 826.2 | 780.3 |
| PtrMorT2-9 | 3,717.9 | 1,239.3 | 1,422.9 | 688.5 | 596.7 | 734.4 | 780.3 |
| PtrMorT2-10 | 3,672 | 1,193.4 | 1,514.7 | 642.6 | 596.7 | 734.4 | 780.3 |
| PcaC1-1 | 1,999.2 | 1,381.8 | 1,587.6 | 1,029 | 382.2 | 940.8 | 823.2 |
| Tabla 7. Continúa | |||||||
| Clave | Medidas de huevo | ||||||
| L | W | H | mpl | mpw | oph | opw | |
| PcaC1-2 | 1,999.2 | 1,411.2 | 1,587.6 | 999.6 | 382.2 | 970.2 | 823.2 |
| PcaC1-3 | 2,028.6 | 1,381.8 | 1,587.6 | 1,029 | 411.6 | 940.8 | 823.2 |
| PcaC1-4 | 2,058 | 1,352.4 | 1,558.2 | 940.8 | 382.2 | 940.8 | 852.6 |
| PcaC1-5 | 1,969.8 | 1,323 | 1,558.2 | 940.8 | 382.2 | 940.8 | 823.2 |
| PcaC2-1 | 1,852.2 | 1,176 | 1,381.8 | 940.8 | 441 | 823.2 | 735 |
| PcaC2-2 | 1,822.8 | 1,264.2 | 1,440.6 | 911.4 | 411.6 | 882 | 764.4 |
| PspFU-1 | 2,058 | 1,323 | 1,558.2 | 1,117.2 | 411.6 | 999.6 | 823.2 |
| PspFU-2 | 2,028.6 | 1,323 | 1,499.4 | 1,234.8 | 382.2 | 999.6 | 793.8 |
| PspFU-3 | 2,087.4 | 1,352.4 | 1,587.6 | 1,146.6 | 382.2 | 911.4 | 735 |
Tabla 8
Medidas en μm de cada huevo de N. isabelae, Pseudosermyle sp. 1, Pseudosermyle sp. 2. Pseudosermyle sp. 5 utilizadas para el PCA.
| Clave | Medidas de huevo | ||||||
| L | W | H | mpl | mpw | oph | opw | |
| PspFU-4 | 1,822.8 | 1,146.6 | 1,440.6 | 940.8 | 411.6 | 970.2 | 676.2 |
| PspFU-5 | 1,940.4 | 1,264.2 | 1,499.4 | 970.2 | 382.2 | 911.4 | 676.2 |
| PspFU-6 | 1,881.6 | 1,234.8 | 1,470 | 1,029 | 411.6 | 940.8 | 705.6 |
| PspFU-7 | 1,940.4 | 1,293.6 | 1,470 | 940.8 | 411.6 | 911.4 | 705.6 |
| PspFU-8 | 1,911 | 1,205.4 | 1,499.4 | 911.4 | 382.2 | 970.2 | 764.4 |
| PspFU-9 | 1,852.2 | 1,205.4 | 1,470 | 940.8 | 382.2 | 970.2 | 764.4 |
| PspFU-10 | 2,058 | 1,323 | 1,499.4 | 1,087.8 | 382.2 | 999.6 | 735 |
| PspFU-11 | 2,087.4 | 1,323 | 1,499.4 | 1,058.4 | 382.2 | 999.6 | 793.8 |
| PspFU-12 | 1,999.2 | 1,323 | 1,470 | 1,205.4 | 382.2 | 970.2 | 764.4 |
| PspFU-13 | 1,881.6 | 1,234.8 | 1,440.6 | 1,058.4 | 411.6 | 911.4 | 793.8 |
| PspFU-14 | 2,058 | 1,323 | 1,528.8 | 1,087.8 | 382.2 | 1,029 | 764.4 |
| PspFU-15 | 1,940.4 | 1,293.6 | 1,499.4 | 999.6 | 382.2 | 999.6 | 705.6 |
| NisaU-1 | 2,263.8 | 1,499.4 | 1,764 | 1,029 | 617.4 | 1,293.6 | 970.2 |
| NisaU-2 | 2,293.2 | 1,470 | 1,705.2 | 999.6 | 588 | 1,146.6 | 882 |
| NisaU-3 | 2,293.2 | 1,646.4 | 1,793.4 | 1,029 | 617.4 | 1,234.8 | 1,029 |
| NisaU-4 | 2,175.6 | 1,558.2 | 1,705.2 | 999.6 | 558.6 | 1,205.4 | 1,029 |
| NisaU-5 | 2,263.8 | 1,646.4 | 1,793.4 | 999.6 | 588 | 1,234.8 | 1,029 |
| NisaU-6 | 2,146.2 | 1,470 | 1,558.2 | 1,087.8 | 558.6 | 1,117.2 | 940.8 |
| NisaU-7 | 2,293.2 | 1,558.2 | 1,793.4 | 1,029 | 588 | 1,234.8 | 1,029 |
| NisaU-8 | 2,146.2 | 1,440.6 | 1,617 | 999.6 | 558.6 | 1,087.8 | 940.8 |
| NisaU-9 | 2,175.6 | 1,528.8 | 1,617 | 1,087.8 | 558.6 | 1,146.6 | 911.4 |
| NisaU-10 | 2,293.2 | 1,587.6 | 1,793.4 | 970.2 | 588 | 1,176 | 911.4 |
| Tabla 8. Continúa | |||||||
| Clave | Medidas de huevo | ||||||
| L | W | H | mpl | mpw | oph | opw | |
| NisaU-11 | 2,116.8 | 1,558.2 | 1,793.4 | 970.2 | 617.4 | 1,234.8 | 1,058.4 |
| NisaU-12 | 2,352 | 1,499.4 | 1,764 | 1,058.4 | 646.8 | 1,293.6 | 1,029 |
| PtgVBU-1 | 3,394.5 | 1,569.5 | 1,715.5 | 1,533 | 657 | 1,277.5 | 912.5 |
| PtgVBU-2 | 3,029.5 | 1,350.5 | 1,606 | 1,350.5 | 511 | 912.5 | 620.5 |
| PtgVBU-3 | 3,467.5 | 1,533 | 1,752 | 1,496.5 | 730 | 1,204.5 | 803 |
| PtgVBU-4 | 3,394.5 | 1,533 | 1,606 | 1,496.5 | 657 | 1,095 | 803 |
| PtgVBU-5 | 3,321.5 | 1,496.5 | 1,642.5 | 1,533 | 620.5 | 1,204.5 | 912.5 |
| PtgVBU-6 | 3,431 | 1,460 | 1,642.5 | 1,460 | 584 | 1,095 | 803 |
| PtgVBU-7 | 3,431 | 1,460 | 1,642.5 | 1,460 | 657 | 1,241 | 839.5 |
| PtgVBU-8 | 3,394.5 | 1,533 | 1,569.5 | 1,533 | 693.5 | 1,095 | 839.5 |
| PtgVBU-9 | 3,467.5 | 1,533 | 1,715.5 | 1,460 | 620.5 | 1,095 | 766.5 |
| PtgVBU-10 | 3,394.5 | 1,533 | 1,715.5 | 1,496.5 | 730 | 1,168 | 912.5 |
| PtgVBU-11 | 3,285 | 1,606 | 1,679 | 1,460 | 620.5 | 1,204.5 | 876 |
| PtgDFG1-1 | 3,321.5 | 1,533 | 1,715.5 | 1,095 | 730 | 985.5 | 766.5 |
| PtgDFG1-2 | 3,102.5 | 1,533 | 1,606 | 1,131.5 | 693.5 | 839.5 | 693.5 |
| PtgDFG1-3 | 3,285 | 1,533 | 1,642.5 | 1,204.5 | 730 | 912.5 | 766.5 |
| PtgDFG1-4 | 3,102.5 | 1,460 | 1,533 | 1,204.5 | 693.5 | 949 | 766.5 |
| PtgDFG1-5 | 3,248.5 | 1,569.5 | 1,569.5 | 1,168 | 766.5 | 803 | 657 |
| PtgDFG2-1 | 3,248.5 | 1,533 | 1,642.5 | 1,241 | 657 | 949 | 620.5 |
| PtgDFG2-2 | 3,285 | 1,496.5 | 1,606 | 1,095 | 620.5 | 949 | 730 |
| PtgDFG2-3 | 3,248.5 | 1,496.5 | 1,569.5 | 1,350.5 | 730 | 949 | 803 |
| PtgDFG2-4 | 3,285 | 1,606 | 1,715.5 | 1,314 | 876 | 912.5 | 730 |
| PtgDFG2-5 | 3,102.5 | 1,606 | 1,752 | 1,241 | 876 | 949 | 730 |
Tabla 9
Medidas en μm de cada huevo de Pseudosermyle sp. 2. Pseudosermyle sp. 3, Pseudosermyle sp. 6 utilizadas para el PCA.
| Clave | Medidas de huevo | ||||||
| L | W | H | mpl | mpw | oph | opw | |
| PtgDFG2-6 | 3,285 | 1,496.5 | 1,606 | 1,314 | 620.5 | 912.5 | 657 |
| PtgDFG2-7 | 3,212 | 1,460 | 1,569.5 | 1,277.5 | 620.5 | 912.5 | 657 |
| PtgDFG2-8 | 3,321.5 | 1,533 | 1,679 | 1,277.5 | 657 | 985.5 | 693.5 |
| PtgDFG2-9 | 3,212 | 1,569.5 | 1,679 | 1,314 | 876 | 912.5 | 766.5 |
| PtgDFG2-10 | 3,175.5 | 1,606 | 1,752 | 1,387 | 657 | 876 | 657 |
| PtgDFG2-11 | 3,467.5 | 1,606 | 1,715.5 | 1,241 | 657 | 949 | 657 |
| PtgDFG2-12 | 3,248.5 | 1,606 | 1,642.5 | 1,277.5 | 693.5 | 985.5 | 839.5 |
| PtgDFG2-13 | 3,248.5 | 1,606 | 1,642.5 | 1,241 | 693.5 | 985.5 | 657 |
| Tabla 9. Continúa | |||||||
| Clave | Medidas de huevo | ||||||
| L | W | H | mpl | mpw | oph | opw | |
| PtgDFG2-14 | 3,285 | 1,496.5 | 1,642.5 | 1,460 | 730 | 949 | 803 |
| PchF1-1 | 3,626.1 | 1,147.5 | 1,422.9 | 1,239.3 | 688.5 | 918 | 780.3 |
| PchF1-2 | 3,993.3 | 1,468.8 | 1,652.4 | 1,422.9 | 734.4 | 1,055.7 | 826.2 |
| PchF1-3 | 3,947.4 | 1,514.7 | 1,606.5 | 1,468.8 | 826.2 | 1,101.6 | 872.1 |
| PchF2-1 | 3,947.4 | 1,377 | 1,698.3 | 1,377 | 688.5 | 918 | 780.3 |
| PchF2-2 | 3,672 | 1,377 | 1,560.6 | 1,377 | 780.3 | 872.1 | 688.5 |
| PchF2-3 | 3,672 | 1,422.9 | 1,606.5 | 1,422.9 | 780.3 | 872.1 | 688.5 |
| PoaxU-1 | 2,701 | 1,642.5 | 1,898 | 693.5 | 328.5 | 1,314 | 1,131.5 |
| PoaxU-2 | 2,518.5 | 1,569.5 | 1,825 | 693.5 | 365 | 1,277.5 | 1,095 |
| PoaxU-3 | 2,664.5 | 1,642.5 | 1,861.5 | 657 | 328.5 | 1,277.5 | 1,058.5 |
| PoaxU-4 | 2,664.5 | 1,679 | 1,825 | 657 | 365 | 1,277.5 | 1,131.5 |
| PoaxU-5 | 2,664.5 | 1,642.5 | 1,861.5 | 730 | 365 | 1,277.5 | 1,131.5 |
| PoaxU-6 | 2,518.5 | 1,606 | 1,788.5 | 693.5 | 365 | 1,241 | 1,095 |
| PoaxU-7 | 2,555 | 1,606 | 1,861.5 | 657 | 365 | 1,350.5 | 1,131.5 |
| PoaxU-8 | 2,591.5 | 1,642.5 | 1,861.5 | 766.5 | 328.5 | 1,277.5 | 1,131.5 |
| PoaxU-9 | 2,482 | 1,569.5 | 1,752 | 657 | 365 | 1,168 | 949 |
| PoaxU-10 | 2,591.5 | 1,569.5 | 1,861.5 | 657 | 365 | 1,241 | 1,095 |
| PoaxU-11 | 2,482 | 1,679 | 1,788.5 | 693.5 | 365 | 1,277.5 | 1,058.5 |
| PoaxU-12 | 2,518.5 | 1,569.5 | 1,788.5 | 693.5 | 328.5 | 1,277.5 | 1,095 |
| PoaxU-13 | 2,555 | 1,606 | 1,861.5 | 693.5 | 328.5 | 1,241 | 1,022 |
| PoaxU-14 | 2,555 | 1,679 | 1,788.5 | 693.5 | 365 | 1,241 | 1,022 |
| PoaxU-15 | 2,701 | 1,679 | 1,898 | 657 | 292 | 1,314 | 1,131.5 |
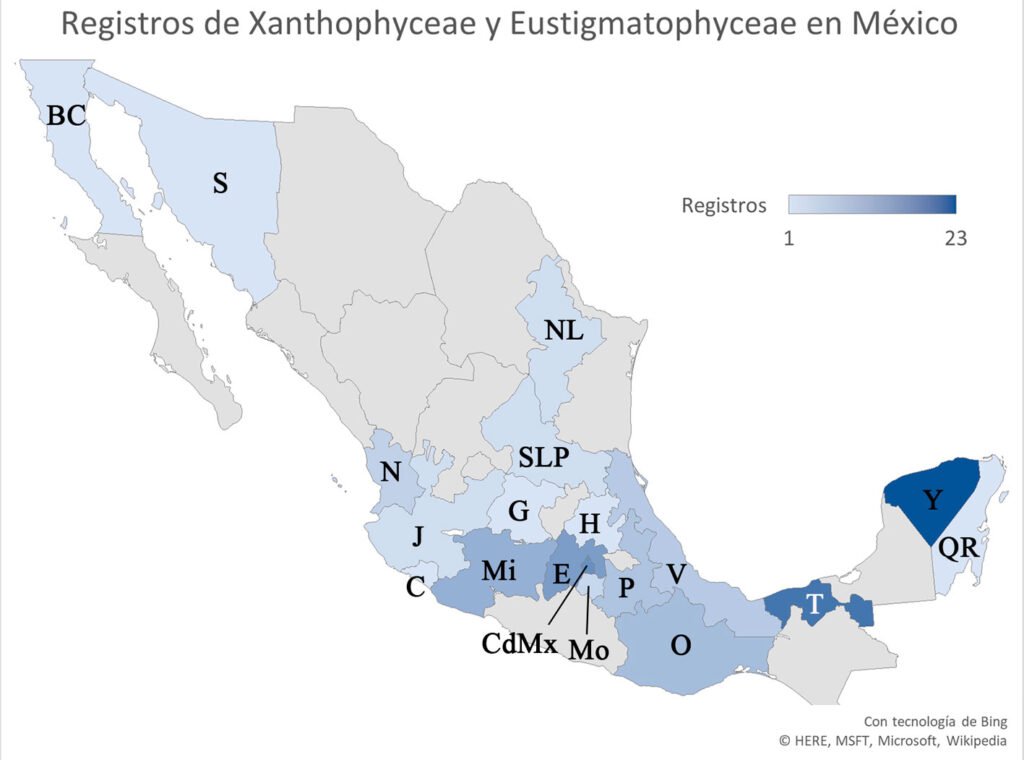
Se llevó a cabo un análisis de componentes principales (PCA) para examinar si las medidas —en micras— de los huevos eran relevantes al reconocer grupos. Las medidas utilizadas fueron: longitud de la cápsula (L), amplitud de la cápsula (W), altitud de la cápsula (H), longitud de la lámina micropilar (mpl), amplitud de la lámina micropilar (mpw), altitud del opérculo (oph) y amplitud del opérculo (opw) (tablas 4-9). Se incluyeron todos los huevos con el propósito de graficar estas mediciones y agruparlos según dichas medidas. Se empleó R (R Core Team, 2013) mediante la interfaz de Rstudio (Rstudio Team, 2015); las paqueterías utilizadas fueron: ggplot2 (Wickham, 2016), ggfortify (Horikoshi y Tang, 2016), rgl (Adler et al., 2018), pca3d (Weiner, 2017) y magick (Ooms, 2018). Cada huevo fue caracterizado de manera individual siguiendo un código que incluye los nombres de las columnas: nombre, clave de hembra de la tabla 3, más el número ascendente correspondiente (tablas 4-9). Para la descripción de los grupos, las medidas se convirtieron a milímetros (mm), mientras que para cada especie se mantuvieron en micras (μm).
Resultados
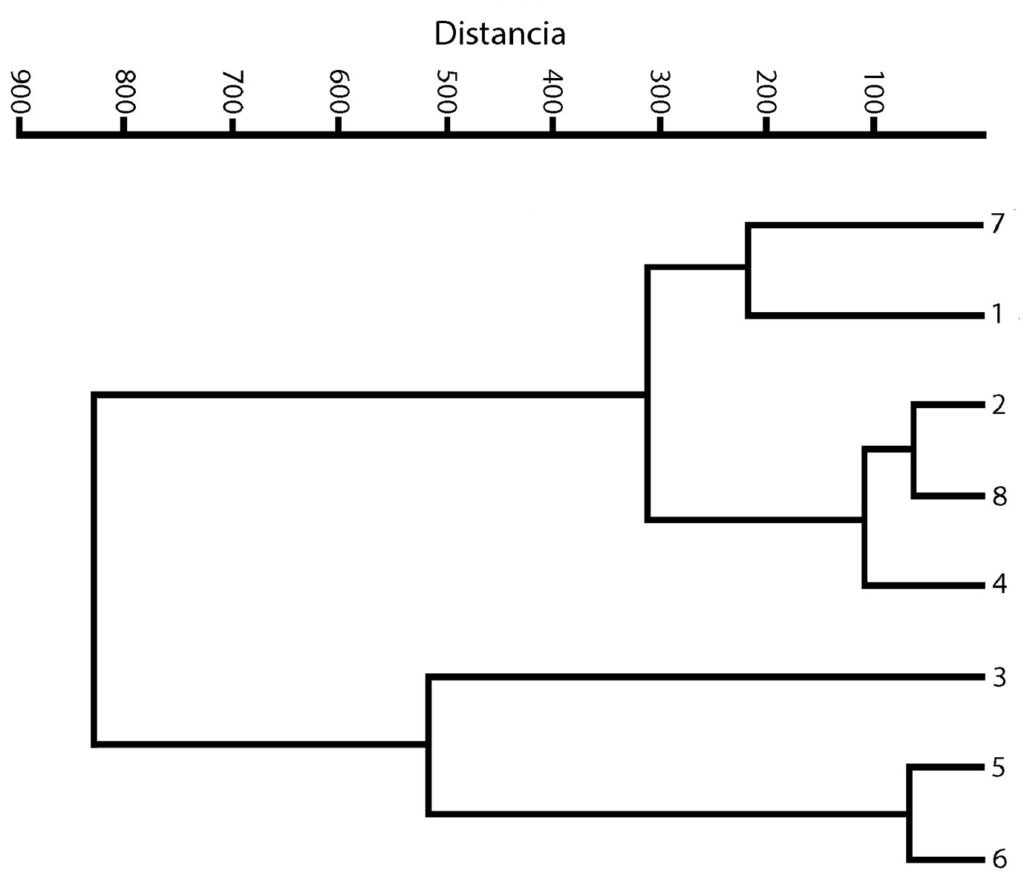
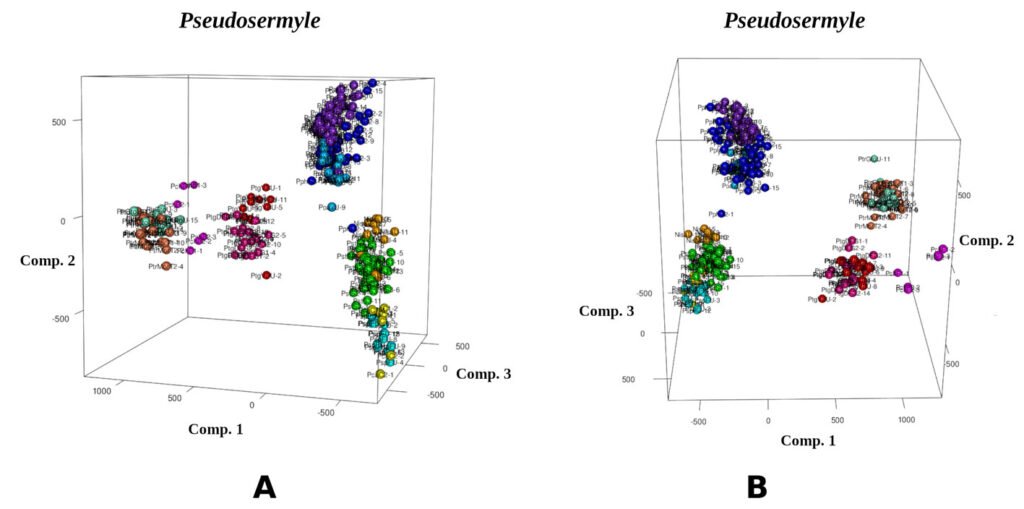
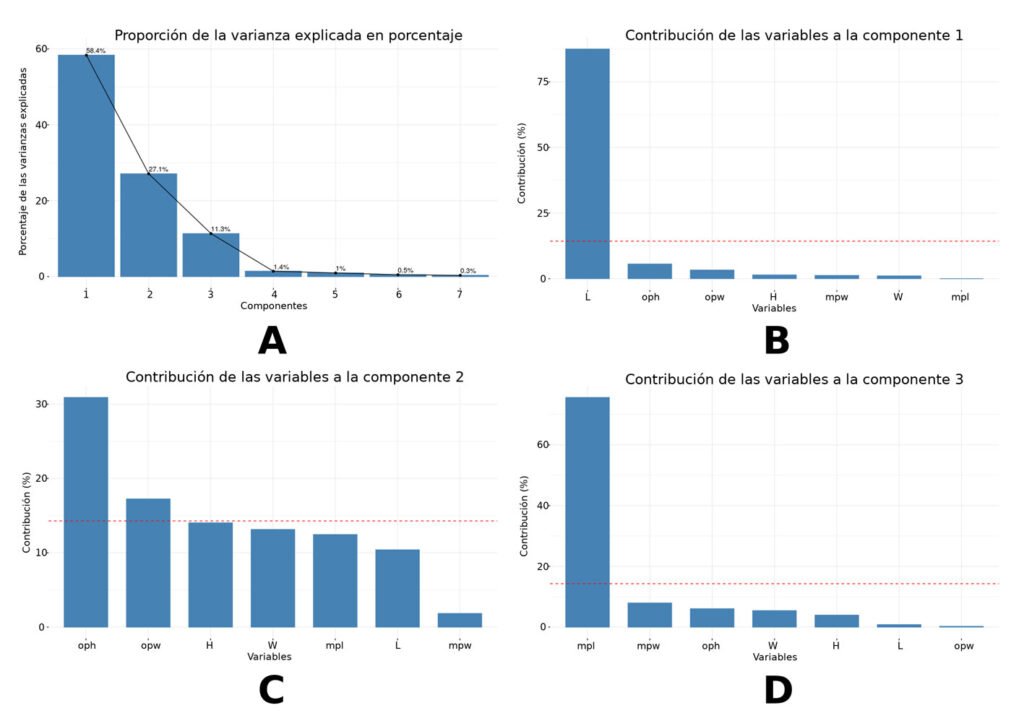
El análisis de componentes principales (PCA) muestra la formación de 4 grupos (fig. 3) explicados en detalle posteriormente, que coinciden con los patrones de morfología externa mostrada por los adultos (machos y hembras) y el tipo de oviposición. En el gráfico del PCA cada eje representa un componente; por lo tanto, se representan 2 gráficos del PCA, uno con rotación en el eje del primer componente (fig. 3A) y otro con rotación en el eje del segundo componente (fig. 3B), para una apreciación mejor de los 4 grupos. Los primeros 3 componentes explican 96.76% de la varianza (fig. 4A). El primer componente presenta mayor contribución de L (fig. 4B), mientras que el segundo presenta mayor homogeneidad en la contribución que recibe de las variables; sin embargo, la oph es la variable que más contribuye (fig. 4C). Finalmente, el tercer componente presenta mayor contribución de mpl (fig. 4D).
A continuación, se da una descripción breve de la microestructura coriónica general de cada grupo, así como para cada una de las especies incluidas en este trabajo. También se incluye una comparación de las distintas estructuras coriónicas entre los grupos y las especies, como se observa en las tablas 10-12. Muchas de estas especies no están descritas y pueden representar especies aún inéditas e innominadas, en consecuencia, se dejaron como morfoespecies y solo se enumeraron.
Tabla 10
Comparación entre estructuras coriónicas entre especies y grupos. Longitud de cápsula (L), amplitud de cápsula (W), altitud de cápsula (H).
| Grupos | General | Cápsula | ||||||
| Tipo de huevo | Oviposición | Forma | Textura | Microestructura | L promedio (mm) | W promedio (mm) | H promedio (mm) | |
| Grupo 1 | adhesivo | Adheridos | Fusiforme | Gránulos | Basamentos piramidales | 3.37 ±0.23 | 1.5 ±0.09 | 1.64 ±0.07 |
| Pseudosermyle sp. 1 | adhesivo | Adheridos | Fusiforme | Gránulos | Basamentos piramidales | 3.36 ±0.12 | 1.5 ±0.06 | 1.66 ±0.05 |
| Pseudosermyle sp. 2 | adhesivo | Adheridos | Fusiforme | Gránulos | Basamentos piramidales | 3.24 ±0.08 | 1.54 ±0.05 | 1.64 ±0.06 |
| Pseudosermyle sp. 3 | adhesivo | Adheridos | Fusiforme | Gránulos | Basamentos piramidales | 3.8 ±0.16 | 1.38 ±0.12 | 1.59 ±0.09 |
| Grupo 2 | adhesivo | Ooteca | Fusiforme | Paralelepípedos | Liso | 3.6 ±0.08 | 1.3 ±0.06 | 1.46 ±0.06 |
| Pseudosermyle tridens | adhesivo | Ooteca | Fusiforme | Paralelepípedos | Liso | 3.59 ±0.09 | 1.28 ±0.07 | 1.44 ±0.05 |
| Pseudosermyle sp. 4 | Adhesivo | Ooteca | Fusiforme | Paralelepípedos | Liso | 3.6 ±0.05 | 1.32 ±0.04 | 1.49 ±0.07 |
| Grupo 3 | Alveolada | Por caída | Doliforme | Variable | Variable | 2.14 ±0.14 | 1.44 ±0.11 | 1.61 ±0.1 |
| Pseudosermyle carinulata | Alveolada | Por caída | Doliforme | Gránulos | Proyecciones digitiformes | 1.96 ±0.08 | 1.32 ±0.08 | 1.52 ±0.08 |
| Pseudosermyle striata | Alveolada | Por caída | Doliforme | Arrugas | Proyecciones digitiformes | 2.21 ±0.09 | 1.48 ±0.06 | 1.64 ±0.07 |
| Pseudosermyle sp. 5 | Alveolada | Por caída | Doliforme | Arrugas | Rugulosa | 1.96 ±0.08 | 1.27 ±0.05 | 1.49 ±0.03 |
| Nooxapty isabelae | Alveolada | Por caída | Doliforme | Espinas | Proyecciones digitiformes | 2.23 ±0.07 | 1.53 ±0.06 | 1.72 ±0.08 |
| Grupo 4 | Alveolada | Por caída | Doliforme | Variable | Variable | 2.68 ±0.09 | 1.69 ±0.08 | 1.87 ±0.08 |
| Pseudosermyle phalangiphora | Alveolada | Por caída | Doliforme | Gibas con espinas umbeliformes | Punteada | 2.68 ±0.1 | 1.65 ±0.08 | 1.82 ±0.08 |
| Pseudosermyle procera | Alveolada | Por caída | Doliforme | Verrugosa con fóveas | Verrugosa | 2.71 ±0.06 | 1.74 ±0.05 | 1.93 ±0.05 |
| Pseudosermyle sp. 6 | Alveolar | Por caída | Doliforme | Coliculada con espinas umbeliformes | Verrugosa | 2.58 ±0.07 | 1.62 ±0.04 | 1.83 ±0.04 |
Tabla 11
Comparación entre estructuras coriónicas entre especies y grupos. Porcentaje de cobertura de la longitud de lámina micropilar en la longitud de la cápsula (% de mpl/L).
| Grupos | Opérculo | Lámina micropilar (mp) | ||||||
| Ornamentación | Ángulo opercular | Capas | Forma | Ornamentación | % de mpl/L | Relieve micropilar | Forma lámina micropilar interna | |
| Grupo 1 | Variable | + 55° | 1 | Lemniscata | Similar a la cápsula | 40 | Variable | Abierta con línea media |
| Pseudosermyle sp. 1 | Estructura solitaria | + 55° | 1 | Lemniscata | Similar a la cápsula | 43.98 | Presen-te | Abierta con línea media |
| Pseudosermyle sp. 2 | Similar a la cápsula | + 55° | 1 | Lemniscata | Similar a la cápsula | 38.63 | Ausente | Abierta con línea media |
| Pseudosermyle sp. 3 | Disposición radial | + 55° | 1 | Lemniscata | Similar a la cápsula | 36.34 | Presen-te | Abierta con línea media |
| Grupo 2 | Similar a la cápsula | + 40° | 2 | Variable | Distinta a la cápsula | 17 | Ausente | Paralela sin línea media |
| Pseudosermyle tridens | Similar a la cápsula | + 40° | 2 | Triangular | Distinta a la cápsula | 16.7 | Ausente | Paralela sin línea media |
| Pseudosermyle sp. 4 | Similar a la cápsula | + 40° | 2 | Circular | Distinta a la cápsula | 17.57 | Ausente | Paralela sin línea media |
| Grupo 3 | Similar a la cápsula | ≈ 0° | 1 | Oblonga | Similar a la cápsula | 50 | Ausente | Abierta con línea media |
| Pseudosermyle carinulata | Similar a la cápsula | ≈ 0° | 1 | Oblonga | Similar a la cápsula | 49.46 | Ausente | Abierta con línea media |
| Pseudosermyle striata | Similar a la cápsula | ≈ 0° | 1 | Oblonga | Similar a la cápsula | 47.51 | Ausente | Abierta con línea media |
| Pseudosermyle sp. 5 | Similar a la cápsula | ≈ 0° | 1 | Oblonga | Similar a la cápsula | 53.23 | Ausente | Abierta con línea media |
| Nooxapty isabelae | Similar a la cápsula | ≈ 0° | 1 | Oblonga | Similar a la cápsula | 45.72 | Ausente | Abierta con línea media |
| Grupo 4 | Acomodo de estructuras | ≈ 0° | 1 | Variable | Variable | 30 | Varia-ble | Abierta con línea media |
| Pseudosermyle phalangiphora | Estructura solitaria | ≈ 0° | 1 | Oblonga | Distinta a la cápsula | 30.885 | Ausente | Abierta con línea media |
| Pseudosermyle procera | Anillo | ≈ 0° | 1 | Elíptica | Distinta a la cápsula | 25.11 | Presen-te | Abierta con línea media |
| Pseudosermyle sp. 6 | Anillo | ≈ 0° | 1 | Oblonga | Similar a la cápsula | 26.55 | Ausente | Abierta con línea media |
Tabla 12
Comparación entre estructuras coriónicas entre especies y grupos. Lámina micropilar (mp).
| Grupos | Borde | Tubérculo micropilar | Copa micropilar | Línea media externa | |||
| Forma | Posición | Forma | Posición | Presencia | Ornamentación | Longitud | |
| Grupo 1 | Carina que se ensancha hacia la parte posterior | Hacia la copa micropilar | Variable | Fusionada al borde de mp | Presente | Variable | Corta (no llega al área polar) |
| Pseudosermyle sp. 1 | Carina que se ensancha hacia la parte posterior | Hacia la copa micropilar | Triángulo invertido | Fusionada al borde de mp | Presente | Carina | Corta (no llega al área polar) |
| Pseudosermyle sp. 2 | Carina que se ensancha hacia la parte posterior | Hacia la copa micropilar | Triángulo invertido | Fusionada al borde de mp | Presente | Cambio de textura | Corta (no llega al área polar) |
| Pseudosermyle sp. 3 | Carina que se ensancha hacia la parte posterior | Hacia la copa micropilar | Matraz invertido | Fusionada al borde de mp | Presente | Sucesión de estructuras | Corta (no llega al área polar) |
| Grupo 2 | Variable | En la mitad de la copa micropilar | Carina | Ausente | Ausente | No aplica | No aplica |
| Pseudosermyle tridens | Cambio de textura | En la mitad de la copa micropilar | Carina | Ausente | Ausente | No aplica | No aplica |
| Pseudosermyle sp. 4 | Ligera elevación | En la mitad de la copa micropilar | Carina | Ausente | Ausente | No aplica | No aplica |
| Grupo 3 | Variable | Hacia la copa micropilar | Variable | Separada del borde de mp | Presente | Variable | Variable |
| Pseudosermyle carinulata | Surco | Hacia la copa micropilar | Rectangular | Separada del borde de mp | Presente | Carina | Larga (llega al área polar) |
| Pseudosermyle striata | Carina | Hacia la copa micropilar | Triángulo invertido | Separada del borde de mp | Presente | Carina | Larga (llega al centro del área polar) |
| Pseudosermyle sp. 5 | Superficie lisa | Hacia la copa micropilar | Rectangular | Separada del borde de mp | Presente | Carina | Larga (llega al área polar) |
| Nooxapty isabelae | Carina | Hacia la copa micropilar | Forma de y | Separada del borde de mp | Presente | Sucesión de estructuras | Larga (llega al centro del área polar) |
| Grupo 4 | Carina | Hacia la copa micropilar | Variable | Fusionada al borde de mp | Variable | Variable | Variable |
| Tabla 12. Continúa | |||||||
| Grupos | Borde | Tubérculo micropilar | Copa micropilar | Línea media externa | |||
| Forma | Posición | Forma | Posición | Presencia | Ornamentación | Longitud | |
| Pseudosermyle phalangiphora | Carina | Hacia la copa micropilar | Semiesfera | Fusionada al borde de mp | Presente | Carina | Larga (llega al área polar) |
| Pseudosermyle procera | Carina | Hacia la copa micropilar | Semiesfera | Fusionada al borde de mp | Ausente | No aplica | No aplica |
| Pseudosermyle sp. 6 | Carina | Hacia la copa micropilar | Triángulo invertido | Fusionada al borde de mp | Presente | Sucesión de estructuras | Larga (llega al área polar) |
Pseudosermyle grupo 1
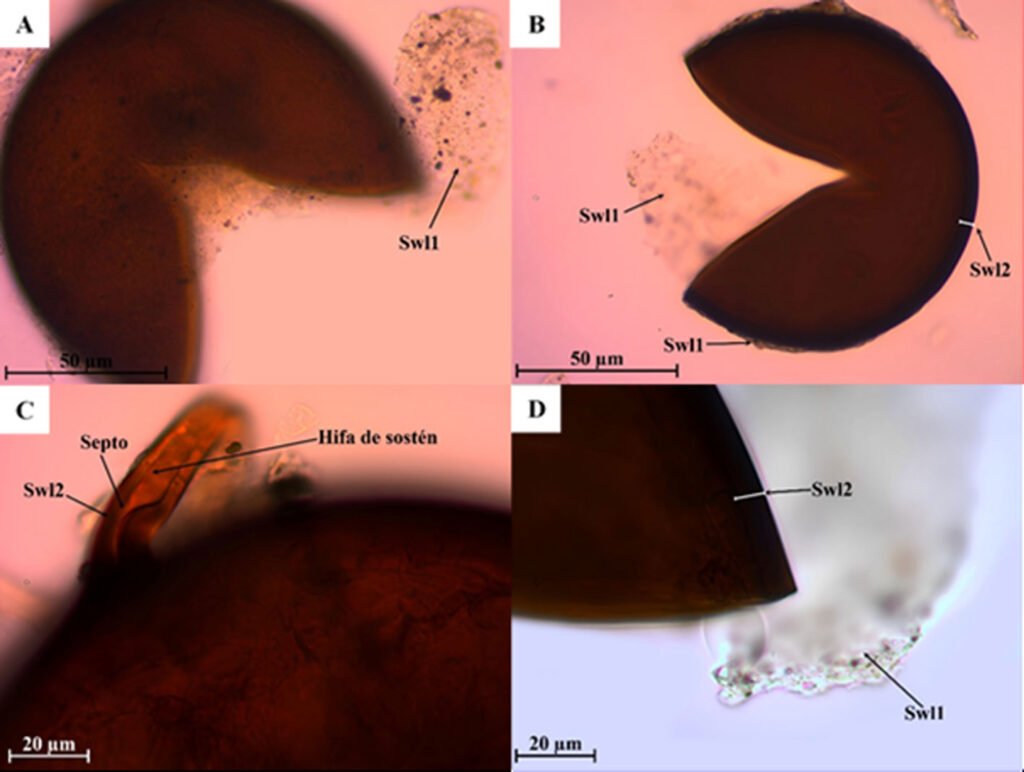
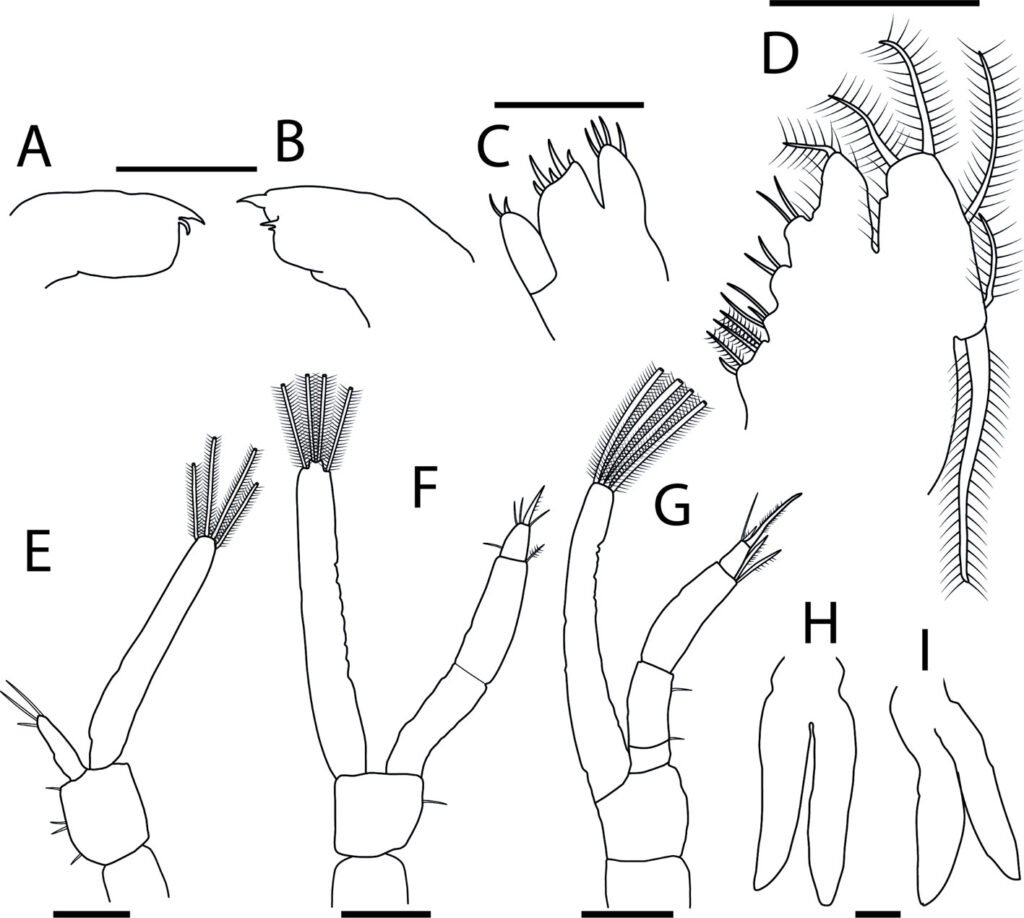
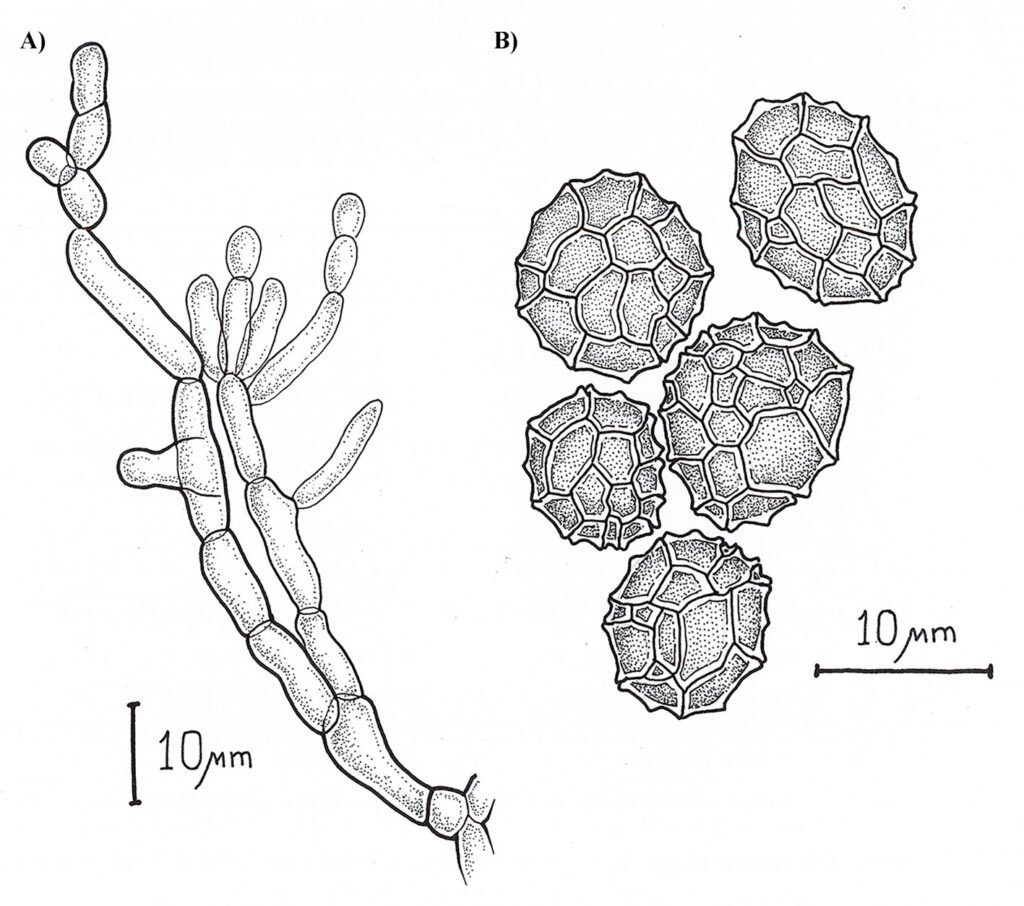
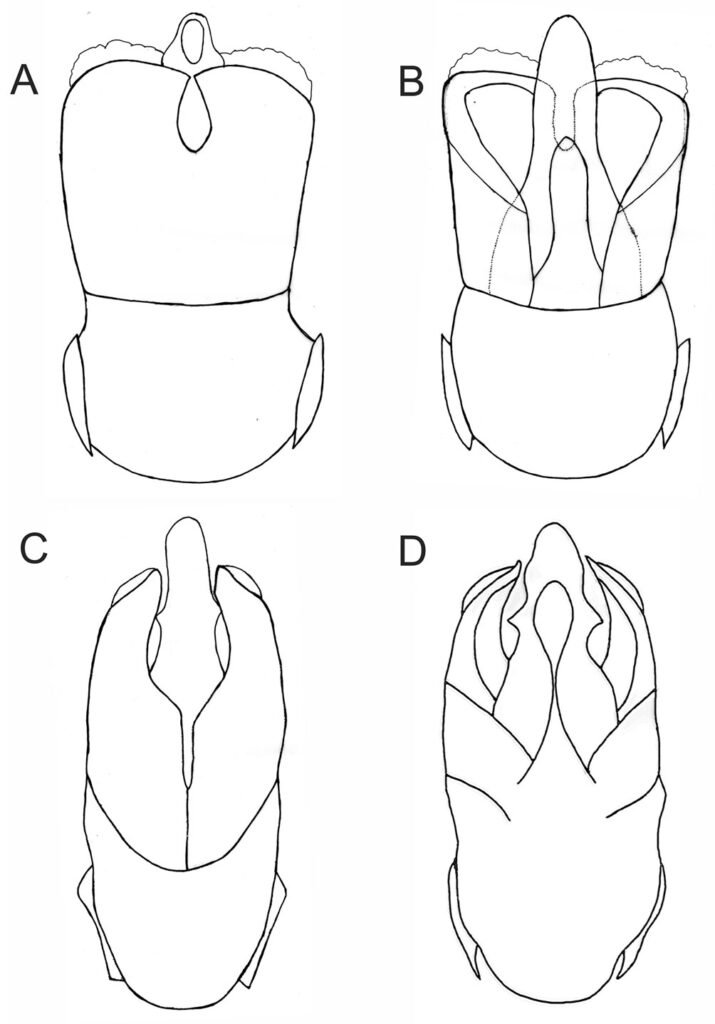
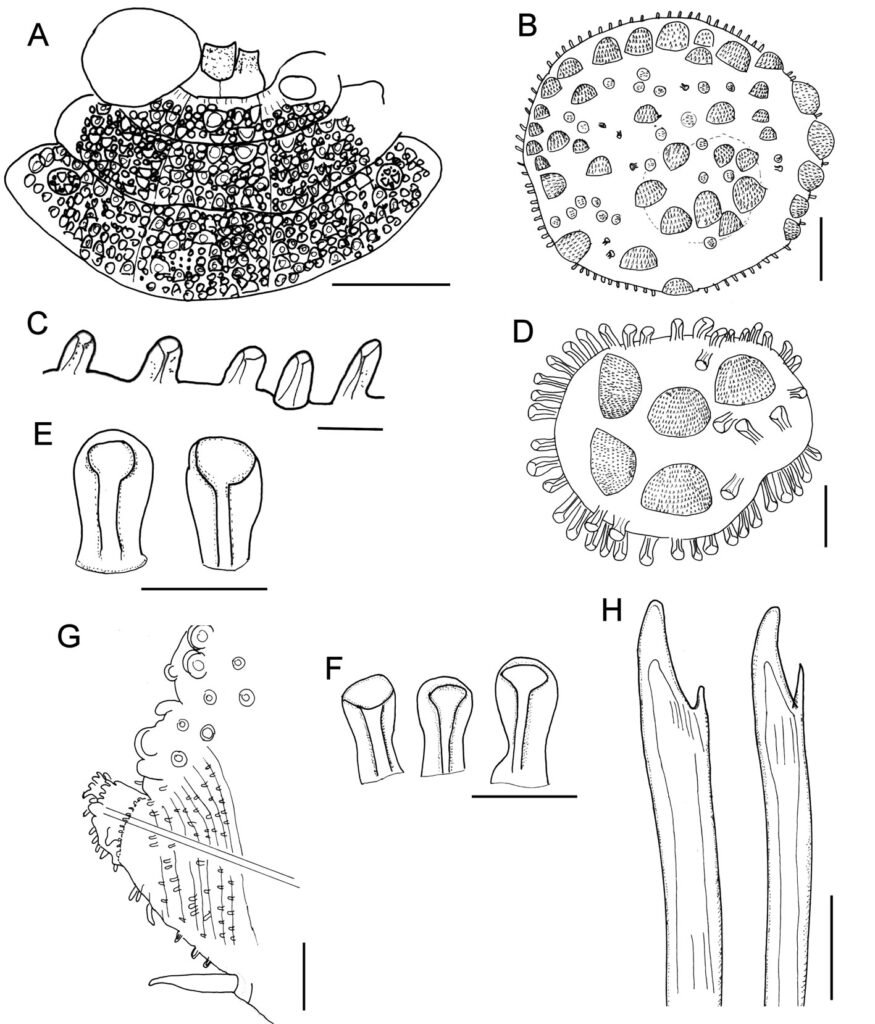
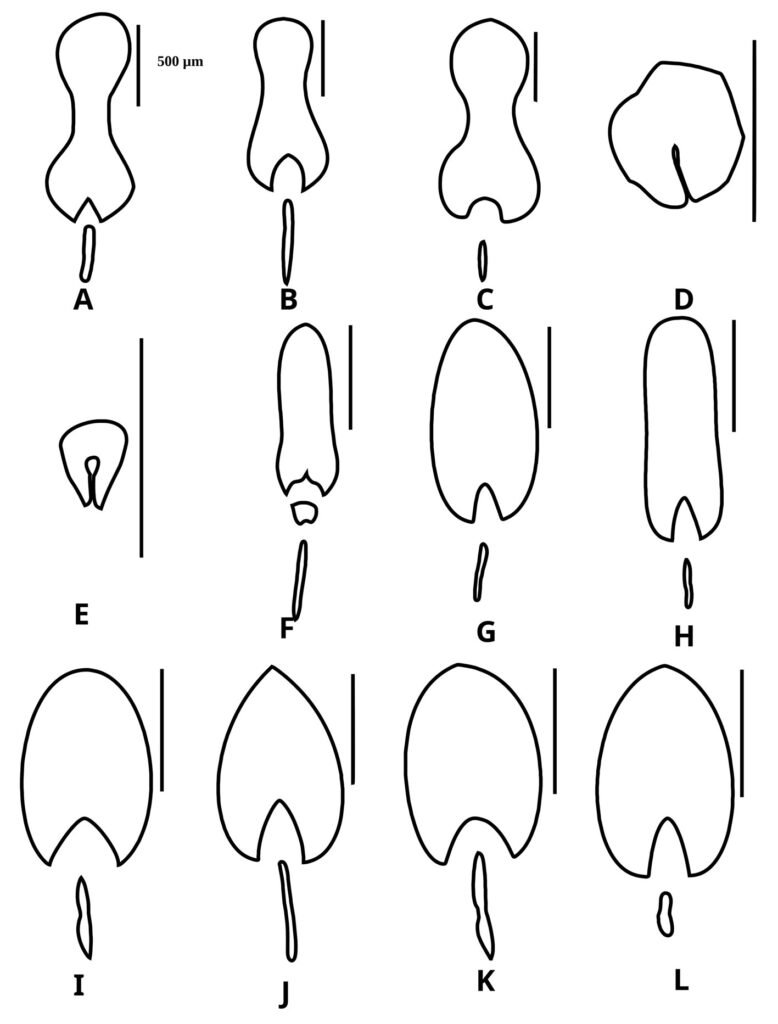
Huevo: adhesivo, adherido individualmente sobre una superficie (fig. 5B). Medidas en mm (n = 36): L = 3.37 ± 0.23 (3.02-3.99), W = 1.5 ± 0.09 (1.14-1.6), H = 1.64 ± 0.07 (1.42-1.75), mpl = 1.34 ± 0.12 (1.09-1.53), mpw = 0.69 ± 0.08 (0.51-0.87), oph = 0.99 ± 0.12 (0.8-1.27) y opw = 0.76 ± 0.08 (0.62-0.91). Opérculo orientado en + 55° aproximadamente. Lámina micropilar en forma de lemniscata u oblonga con el centro constreñido; con una longitud aproximada entre más de un tercio y menos de la mitad de la longitud de la cápsula. Lámina micropilar interna abierta con línea media (fig. 6A-C).
Especies incluidas: Pseudosermyle sp. 1, Pseudo-
sermyle sp. 2 y Pseudosermyle sp. 3.
Pseudosermyle sp. 1 (figs. 1, 6A, 7A, 8, 9)
Material examinado: 11 huevos. México. Edo. de México, Valle de Bravo, Arriba cueva, 19°5’32.928” N, 100°4’19.848” O, 2,260 m snm [voucher: PHMX 349-358 depositados en CNIN y MZFC].

Medidas en μm: (n = 11) L= 3364.63 ± 124.11 (3029.5-3467.5), W = 1509.77 ± 67.84 (1350.5-1606), H = 1662.4 ± 57.39 (1569.5-1752), mpl = 1479.9 ± 52.54 (1350.5-1533), mpw = 643.72 ± 63.79 (511-730), oph = 1144.77 ± 100.98 (912.5-1277.5), opw = 826.22 ± 85.24 (620.5-912.5), %h/l (elongación) = 49.44 ± 1.97 (46.23-53.01), %w/h (compresión) = 90.86 ± 4 (84.09-97.67).

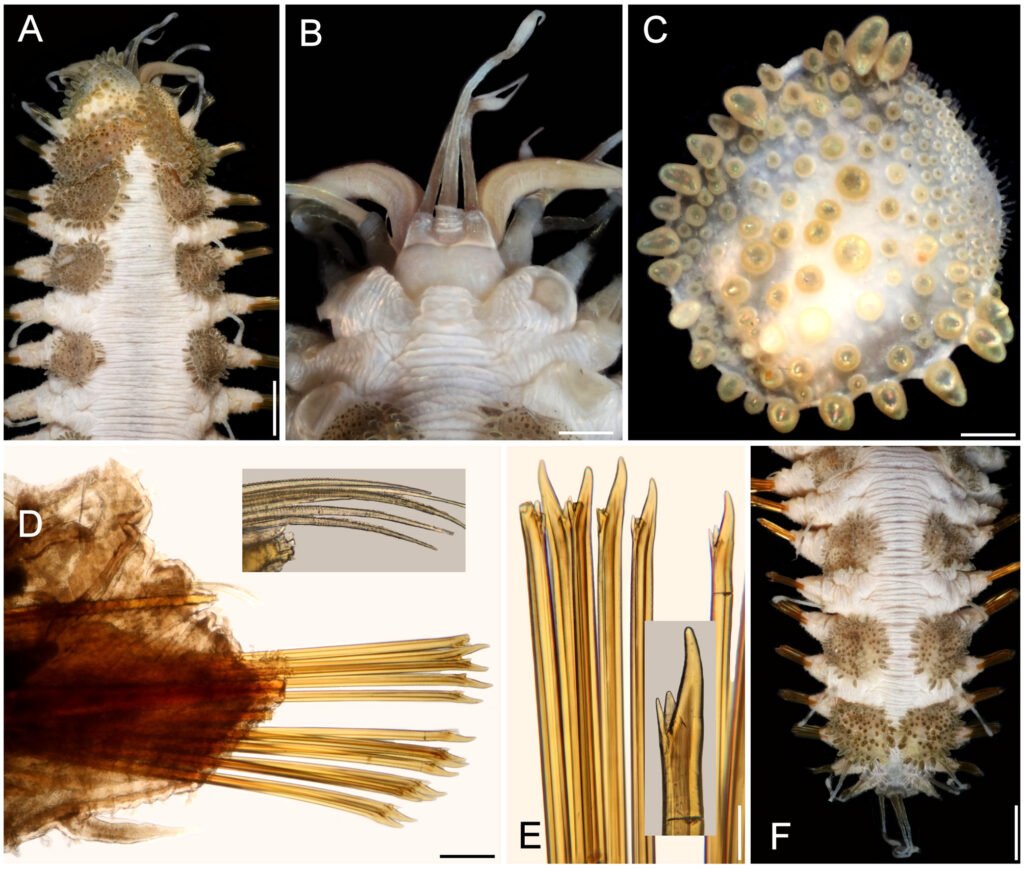
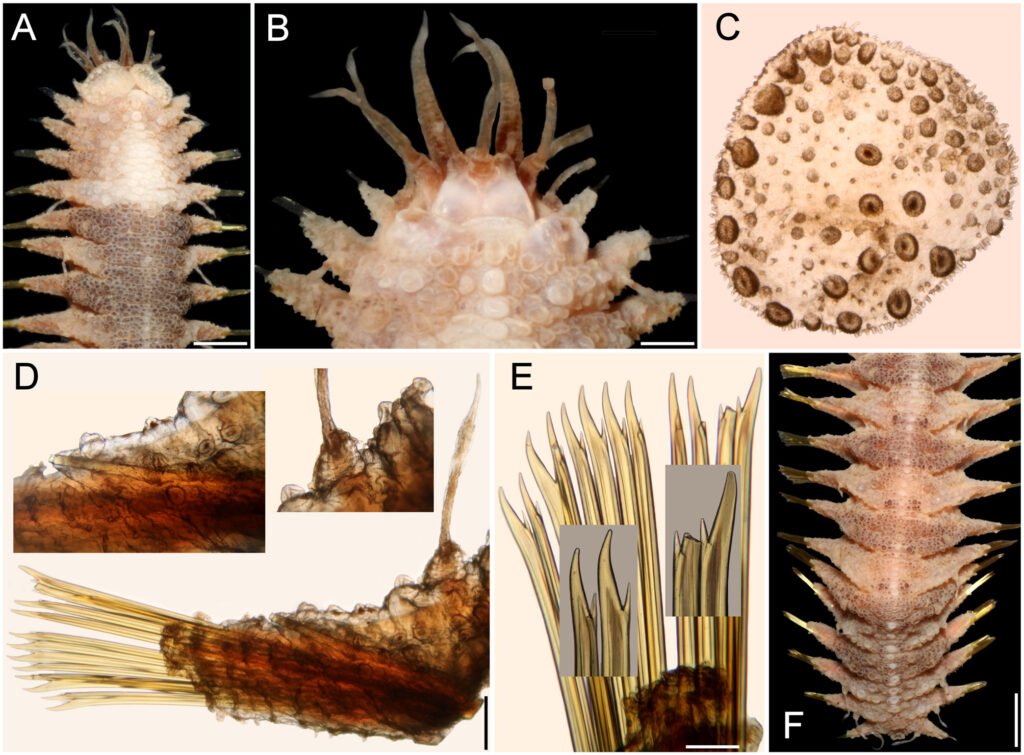
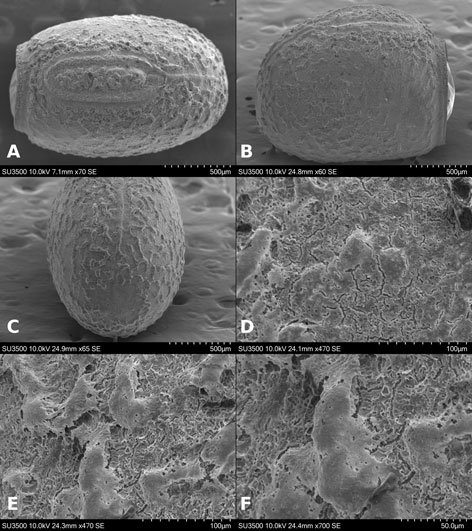
Microestructura: (n = 1) (figs. 8, 9) cápsula de superficie granulosa (fig. 8A, B), con granos formados por basamentos piramidales de 6-8 niveles (fig. 8E, F); la longitud varía entre 37.18-59.04 μm. En toda la superficie se observa un patrón de terrazas (polígonos irregulares y escalonados, en su mayoría rectangulares), que pueden o no formar los gránulos (fig. 8E). El huevo suele estar cubierto (cuando es ovipuesto) por una sustancia adherente o pegajosa que presenta rugosidades irregulares y separadas, suele cubrir la mitad ventral (fig. 8C, D); las arrugas son lisas (fig. 8D). Lámina micropilar con ornamentación y textura similar a la cápsula (fig. 9A). Borde a manera de una carina con 66 μm de amplitud (fig. 9D), tiende a ensancharse hacia la copa micropilar (fig. 9C). Tubérculo micropilar como un triángulo invertido, con 286 μm de longitud y 198 μm de amplitud (fig. 9C). Copa micropilar con forma de ‘y’, fusionada al borde, con 362 μm de amplitud y 39 μm de grosor (fig. 9C). Línea media como una carina de 40 μm de amplitud (figs. 8C, 9B). Las estructuras antes mencionadas, salvo la superficie de la lámina micropilar (fig. 9E), son de textura rugosa. Opérculo de superficie rugosa, con arrugas que forman una elevación a manera de semicírculo en la región anterior; la textura de las arrugas es verrugosa (fig. 9F).
Pseudosermyle sp. 2 (figs. 1, 6B, 7B, 10, 11)
Material examinado:19 huevos. México, Ciudad de México, Coyoacán, REPSA, Espacio Escultórico-Caseta de vigilancia, 19°19’3.4824” N, 99°11’5.4744” O, 2,311 m snm [voucher: PHMX 304-322 depositados en CNIN y MZFC].
Medidas en μm: (n = 19)L = 3246.57 ± 87.28 (3102.5-3467.5), W = 1544.52 ± 51.69 (1460-1606), H = 1646.34 ± 64.25 (1533-1752), mpl = 1254.44 ± 94.4 (1095-1460), mpw = 714.63 ± 82.8 (620.5-876), oph = 929.78 ± 49.22 (803-985.5), opw = 718.47 ± 63.28 (620.5-839.5), %h/l (elongación) = 50.73 ± 2.18 (48.31-56.47), %w/h (compresión) = 93.86 ± 2.59 (89.36-100).
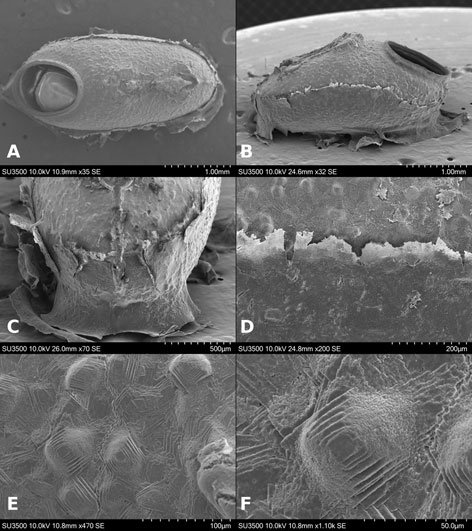
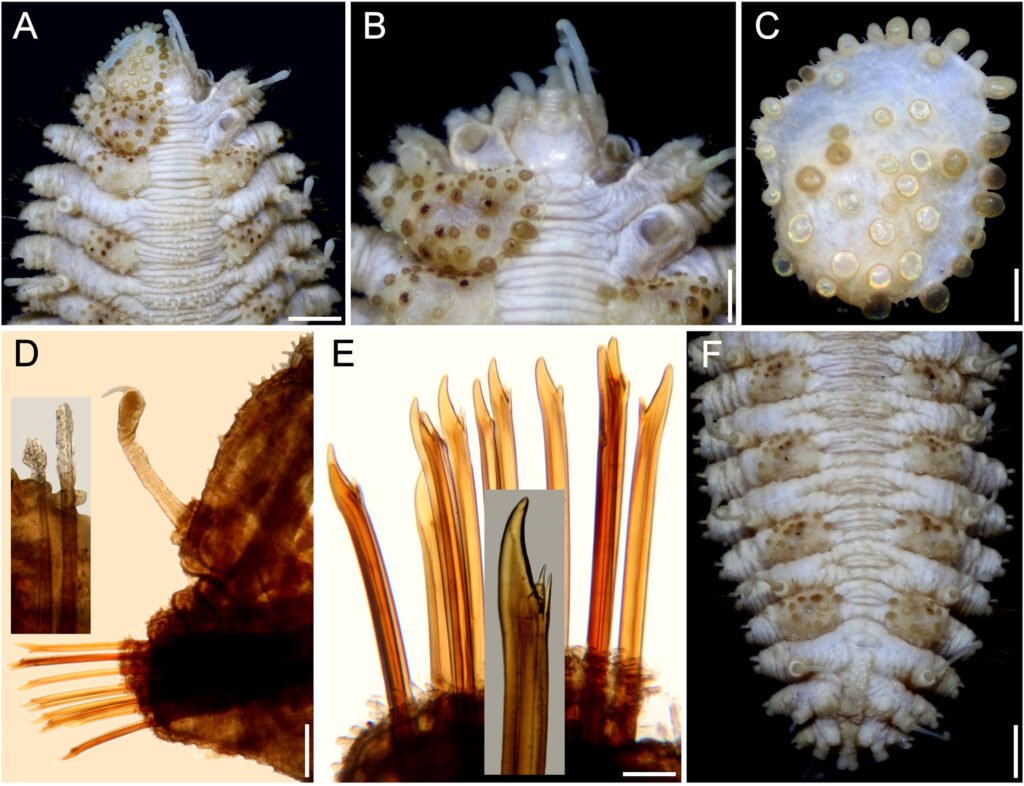
Microestructura: (n = 1) (figs. 10, 11) cápsula de superficie coliculado-granulosa (fig. 10A, B), con granos formados por basamentos piramidales de 4-6 niveles; la longitud varía entre 24.66-34.39 μm (fig. 10E, F). En toda la superficie se presenta un patrón de polígonos irregulares y escalonados —en su mayoría rectangulares, que pueden o no formar los gránulos (fig. 10E); en ciertas regiones hay máculas irregulares de textura escabriculosa. El huevo suele estar cubierto (cuando es ovipuesto) por una sustancia pegajosa que muestra rugosidades irregulares y muy cercanas entre sí, suele cubrir la mitad ventral (fig. 10B, C); las arrugas son lisas (fig. 10D). Lámina micropilar con ornamentación similar al patrón presente en la superficie de la cápsula (fig. 11A), con secciones irregulares de textura escabriculosa (fig. 11E). Borde como una carina de 73 μm de amplitudl (fig. 11D) y tiende a ensancharse hacia la copa micropilar (fig. 11C), con textura papilada (fig. 11D). Tubérculo micropilar como un triángulo invertido, con 282 μm de longitud y 136 μm de amplitud (fig. 11C); textura similar a la presente en la superficie de la cápsula (fig. 11C). Copa micropilar con forma de ‘v’, fusionada al borde, con 321 μm de amplitud y 45 μm de grosor, de superficie rugosa (fig. 11A, C). Línea media con 533 μm de longitud y 61 μm de amplitud (figs. 10C, 11B); de textura tuberculosa al centro y escabriculosa en la unión con la cápsula (fig. 11B) – esta línea media exhibe un cambio de texturas en la cápsula. Opérculo de textura rugulosa que forma secciones poligonales de grupos de protuberancias (fig. 11F).
Pseudosermyle sp. 3 (figs. 1, 6C, 7C, 12, 13)
Material examinado: 6 huevos. México, Jalisco, La Huerta, alrededores EB Chamela, 19°29’57.516” N, 105°2’41.424” O, 87 m snm [voucher: PHMX 323-328 depositados en CNIN y MZFC].
Medidas en μm: (n = 6) L = 3809.7 ± 169.27 (3626.1-3993.3), W = 1384.65 ±127.91 (1147.5-1514.7), H = 1591.2 ± 94.81 (1422.9-1689.3), mpl = 1384.65 ± 79.05 (1239.3-1468.8), mpw = 749.7 ± 55.58 (688.5-826.2), oph = 956.25 ± 98.08 (872.1-1101.6), opw = 772.65 ± 73.53 (688.5-872.1), %h/l (elongación) = 41.76 ± 1.65 (39.24-,43.75) y %w/h (compresión) = 86.95 ± 5.21 (80.64-94.28).
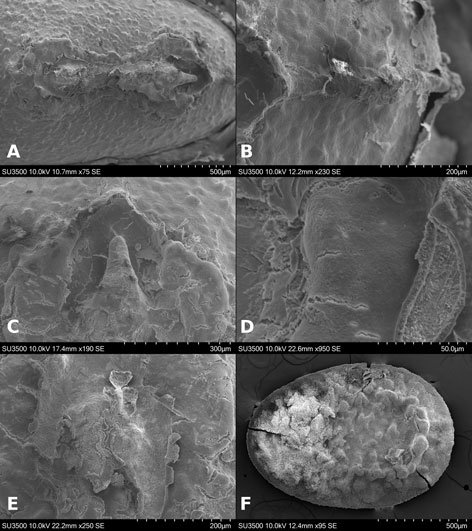
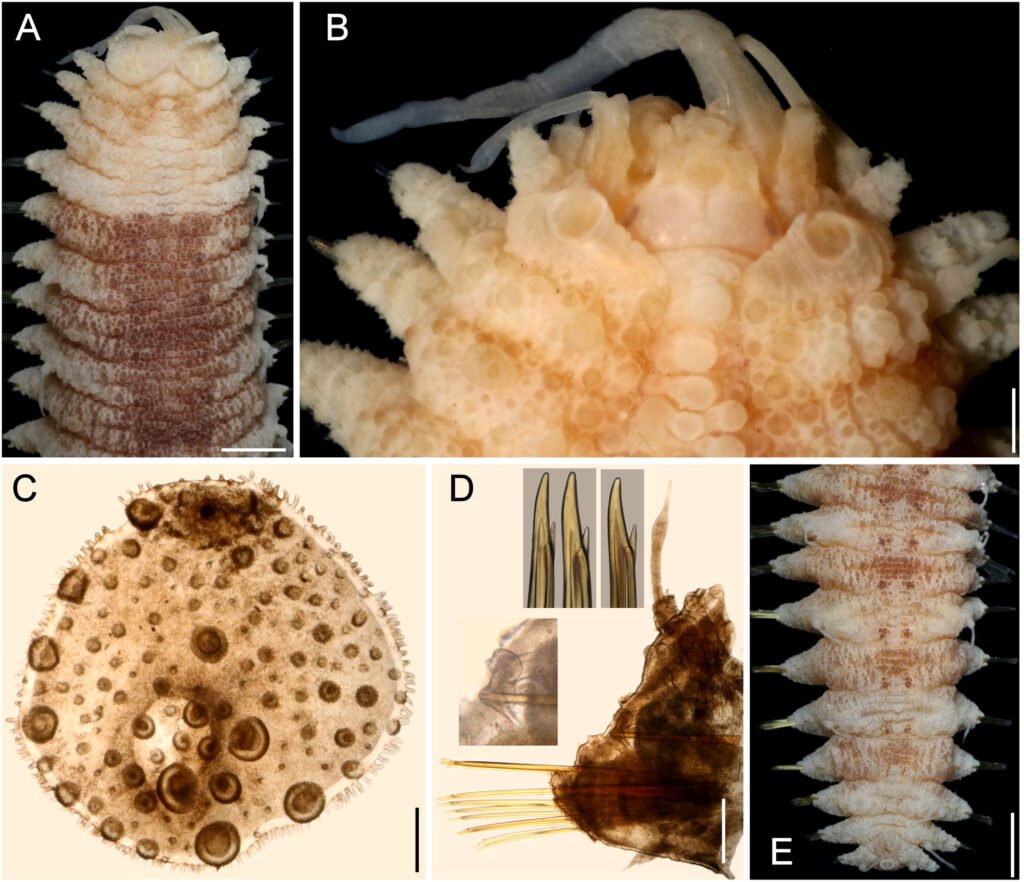
Microestructura: (n = 1) (figs. 12, 13) cápsula de superficie rugosa, con arrugas irregulares de longitud 54.04-148.04 μm y amplitud de 28.19-53.26 μm (fig. 12A, B); unidas por una especie de membrana (fig. 12D). Los espacios entre las arrugas están saturados de gránulos con diámetro 28.19-42.29 μm (fig. 12D, F), éstos suelen estar muy juntos hacia el dorso y más separados hacia los lados; en las superficies laterales se ven algunos niveles, como si fuesen basamentos piramidales (fig. 12E). El huevo suele estar cubierto (cuando ovipuesto) por una sustancia adherente que exhibe rugosidades irregulares y muy cercanas, suele cubrir la mitad ventral (fig. 12B, C); las arrugas son lisas (fig. 12D). Lámina micropilar con ornamentación y textura similar a la cápsula, salvo que las arrugas están hacia el centro (fig. 13E) y los gránulos hacia la periferia (fig. 13A).
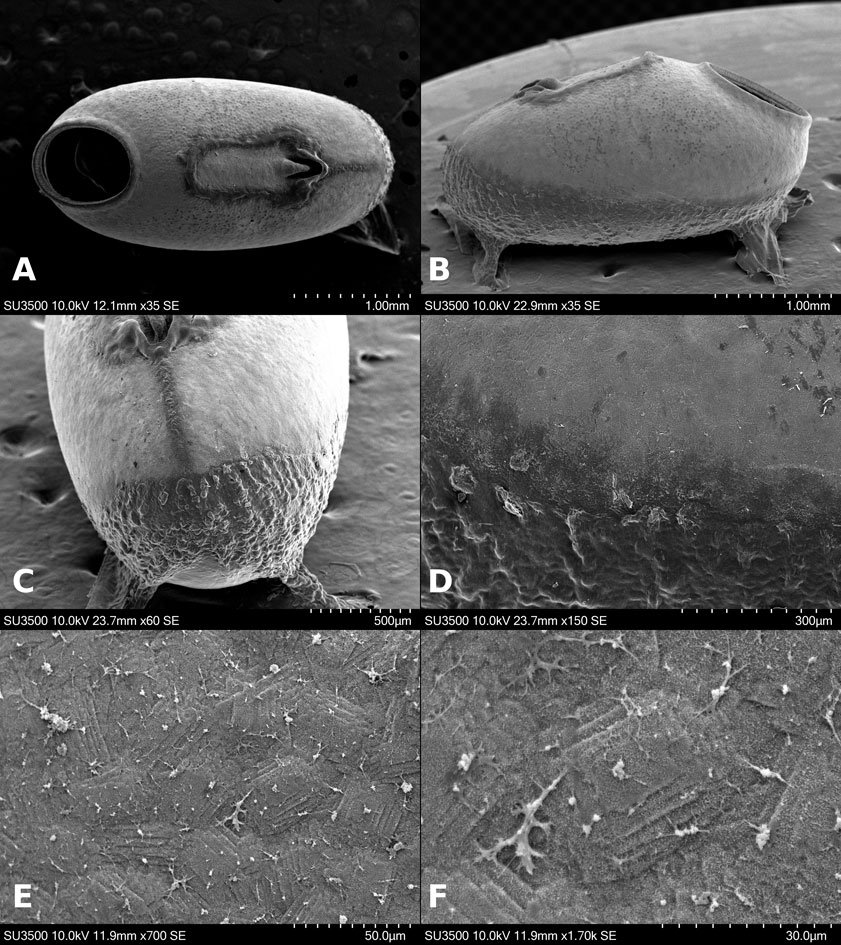
Borde de textura escabriculosa elevada a manera de carina, con 77 μm de amplitud (fig. 13D). Tubérculo micropilar en forma de matraz invertido con 381 μm de longitud y 237 μm de amplitud, de textura rugosa (fig. 13C). Copa micropilar con forma de ‘v’, fusionada al borde, con 437 μm de amplitud y 97 μm de grosor, de textura rugosa (fig. 13C). Línea media con 351 μm de longitud y 98 de amplitud; como una serie de arrugas elevadas con una textura escabriculosa en el centro (figs. 12C, 13B). Opérculo con espacio entre las arrugas radiales; hacia la periferia es granuloso como la cápsula y hacia el centro de las arrugas la textura es rugosa, pero sin formar arrugas del tamaño y forma a las que rodean esta zona (fig. 13F).
Pseudosermyle grupo 2
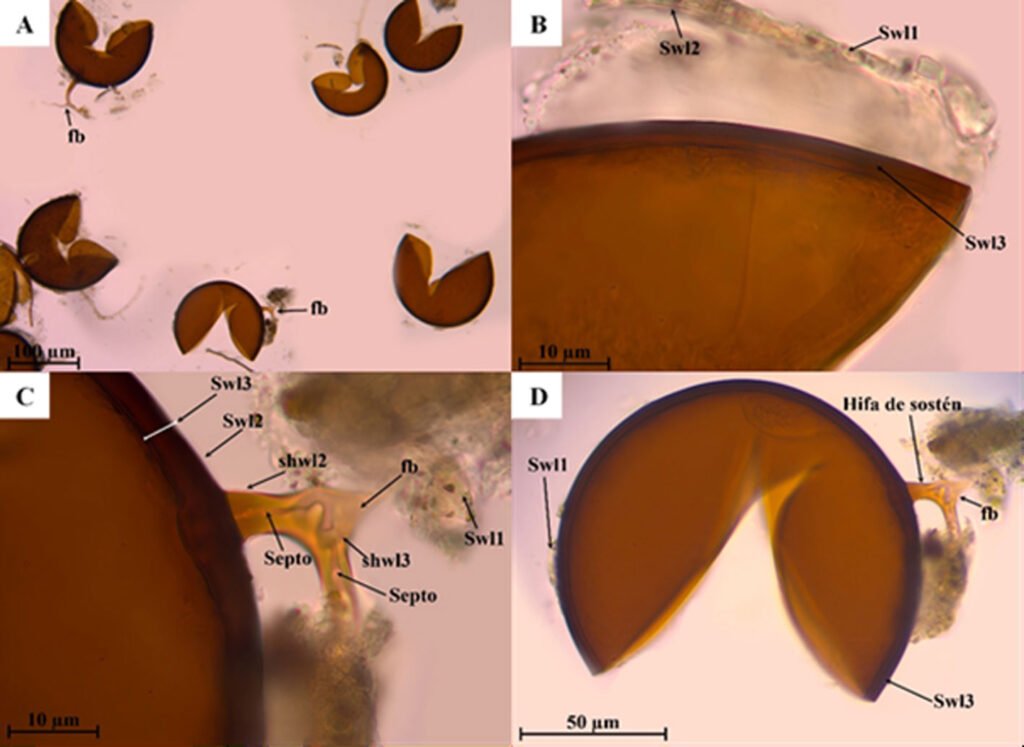
Huevo: adhesivo con oviposición en ooteca (fig. 5C). Medidas en mm (n = 35): L = 3.6 ± 0.08 (3.44-3.71), W = 1.3 ± 0.06 (1.14-1.37), H = 1.46 ± 0.06 (1.33-1.6), mpl = 0.61 ± 0.09 (0.32-0.73), mpw = 0.53 ± 0.07 (0.22-0.59), oph = 0.79 ± 0.06 (0.64-0.87) y opw = 0.74 ± 0.05 (0.64-0.82). Opérculo orientado hacia la superficie dorsal en + 40° aproximadamente. Lámina micropilar reducida, con una longitud cercana a un sexto de la longitud de la cápsula. Lámina micropilar interna paralela sin línea media (fig. 6D, E).
Especies incluidas: Pseudosermyle tridens (Burmeister, 1838) y Pseudosermyle sp. 4.
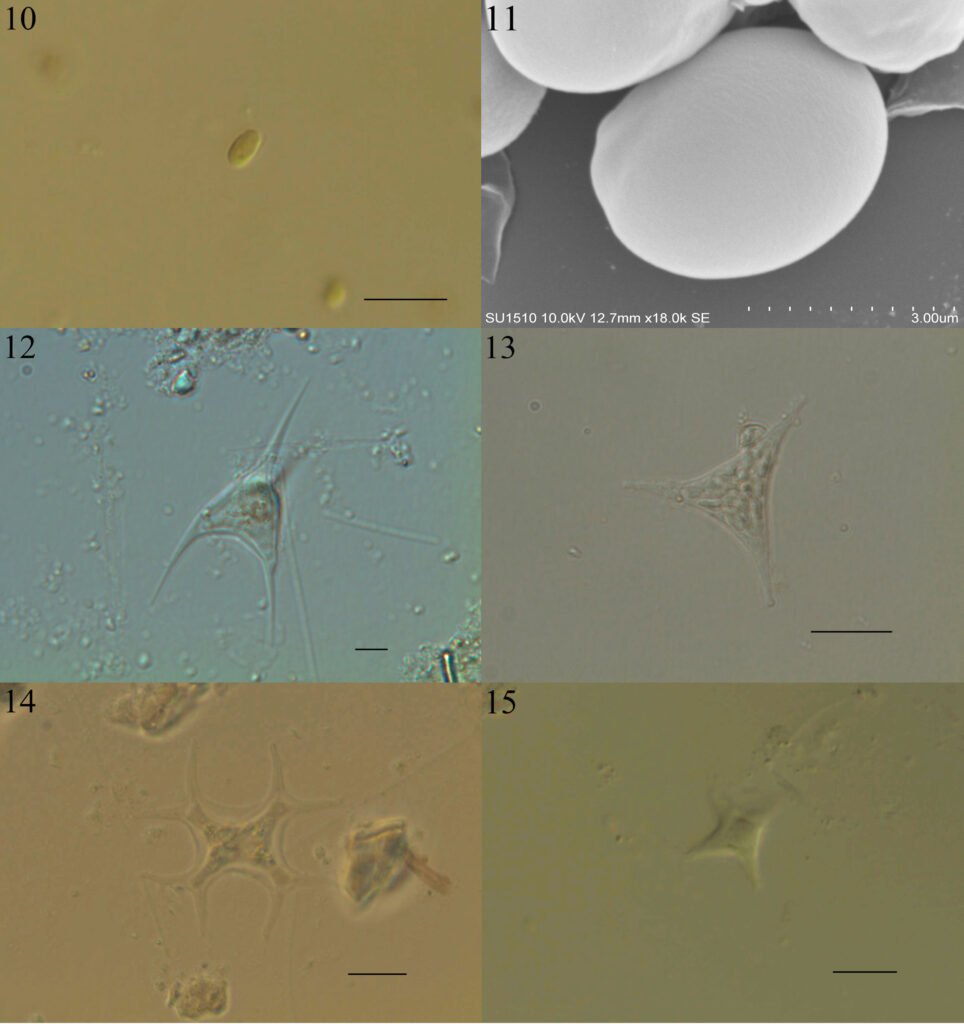
Pseudosermyle tridens (Burmeister, 1838)(figs. 1, 6D, 7D, 14, 15)
Material examinado: 20 huevos disecados y 3 ootecas. México, Morelos, Ayala, Venustiano Carranza esquina Iturbide, Cruz Verde, 18°45’36.6264” N, 98°58’33.9528” O, 1,295 m snm [voucher: PHMX 329-348, 616-618 depositados en CNIN y MZFC].
Medidas en μm: (n = 20) L = 3597 ± 99.7 (3442.5-3717.9), W = 1282.6 ± 70.4 (1147.5-1377), H = 1444 ± 52.4 (1331.1-1514.7), mpl = 600.7 ± 74.7 (459-688.5), mpw = 528.3 ± 50.3 (367.2-596.7), oph = 741.7 ± 37.2 (642.6-826.2), opw = 778.2 ± 27.8 (734.4-826.2), %h/l (elongación) = 40.14 ± 1.09 (38.27-41.77), %w/h (compresión) = 88.89 ± 5.28 (78.12-100).
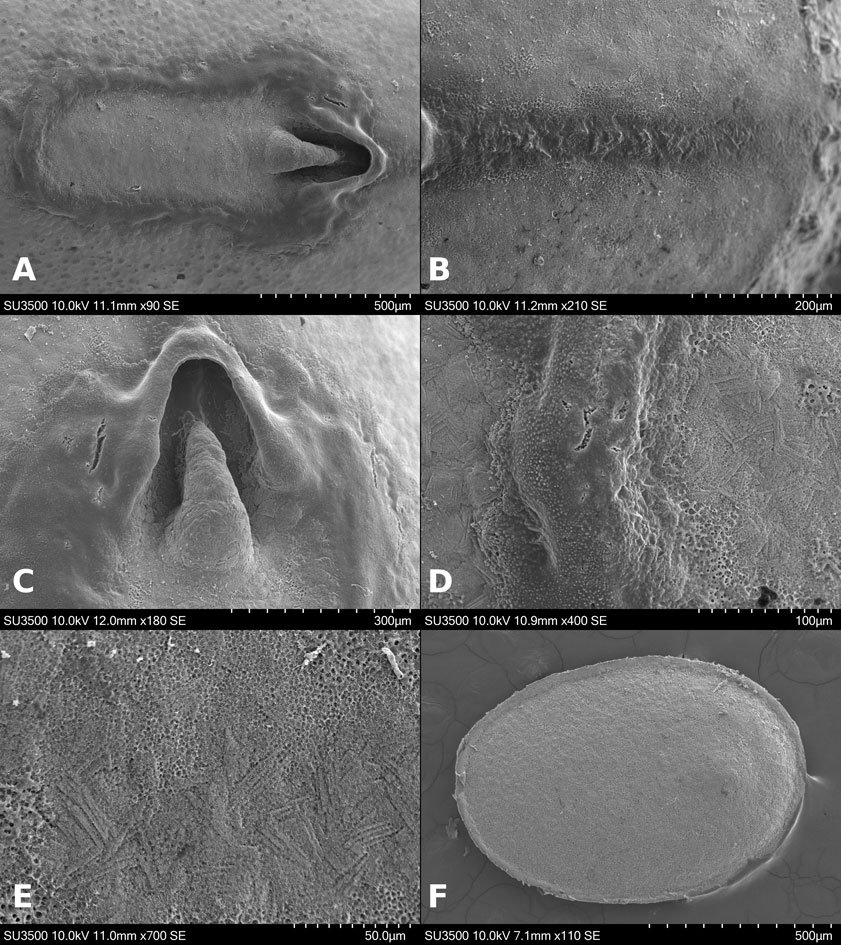
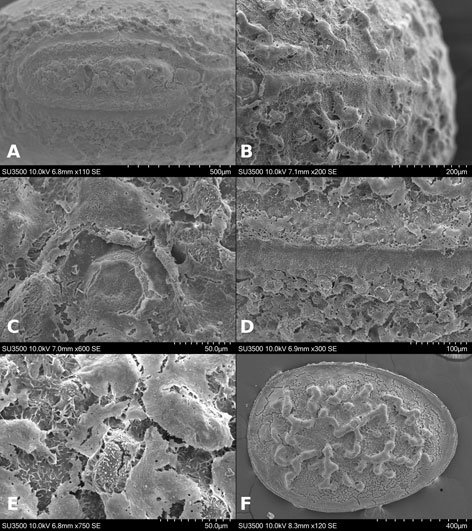
Microestructura: (n = 1) (figs. 14, 15) cápsula con superficie dorsal cubierta por paralelepípedos (fig. 14A, B) con longitudes de arista entre 6-9.5 μm (fig. 14E, F). En las superficies laterales y ventrales es lisa (fig. 14C, D). Lámina micropilar en general con textura lisa hacia el centro (fig. 15A); con tendencia a formar fibras que se vuelven una retícula hacia la periferia (fig. 15B). Tubérculo micropilar lineal, liso, con 273 μm de longitud y 108 μm de amplitud aproximadamente (fig. 15C). El borde es el límite entra las texturas de la lámina micropilar y la cápsula. Sin copa micropilar, ni línea media. Opérculo de textura como en la cápsula (fig. 15D).
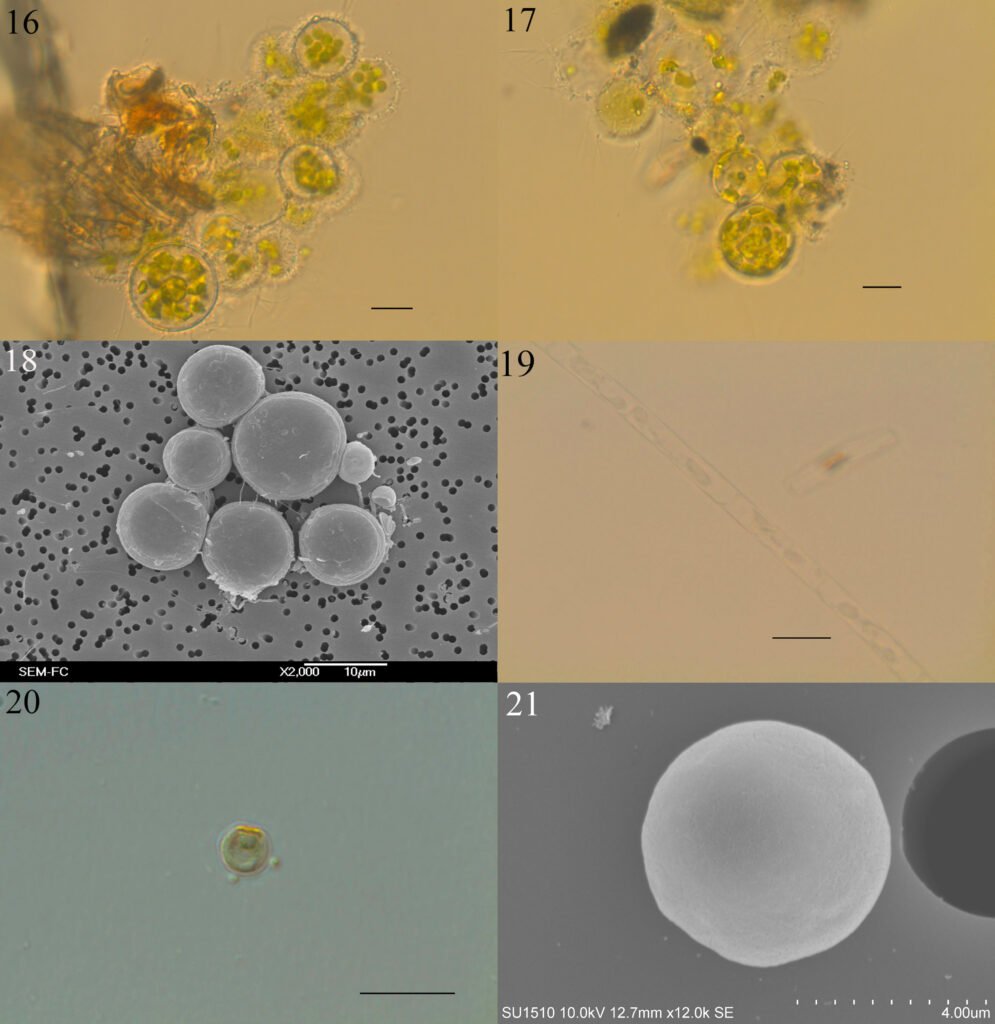
Pseudosermyle sp. 4 (figs. 1, 6E, 7E, 16, 17)
Material examinado: 15 huevos disecados y 3 ootecas. México, Guanajuato, Silao de la Victoria, Villa Esmeralda, 20°57’13.212” N, 101°26’0.996” O, 1,782 m snm [voucher: PHMX 359-373, 423-425 depositados en CNIN y MZFC].
Medidas en μm: (n = 15) L= 3604.68 ± 54.49 (3488.4-3672), W= 1324.98 ± 48.65 (1239.3-1377), H = 1499.4 ± 72.91 (1377-1606.5), mpl = 633.42 ± 107.22 (321.3-734.4), mpw = 535.5 ± 96.07 (229.5-596.7), oph = 859.86 ± 21.01 (826.2-872.1), opw = 694.62 ± 29.37 (642.6-734.4), %h/l (elongación) = 41.61 ± 2.29 (38.46-46.05), %w/h (compresión) = 88.57 ± 5.66 (79.41-100).
Microestructura: (n = 1) (figs. 16, 17) cápsula de superficie dorsal cubierta por paralelepípedos (fig. 16A, B), con longitudes de arista entre 1-3 μm (fig. 16E, F). En las superficies laterales y ventral con una reducción gradual de los paralelepípedos (fig. 16C, D). Lámina micropilar en general de textura lisa hacia el tubérculo micropilar; hacia el borde es rugosa (fig. 17A). Tubérculo micropilar liso, con 321 μm de longitud y 136 μm de amplitud aproximadamente (fig. 17C).
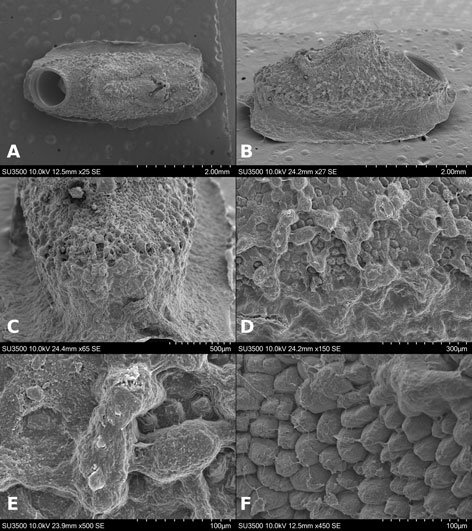
El borde es una ligera elevación que rodea la lámina micropilar y se encuentra abierto en el área polar (figs. 16C, 17A); su textura es rugosa (fig.17B), de aproximadamente 64 μm de amplitud. Sin copa micropilar, ni línea media (figs. 16C, 17A). Opérculo de textura como en la cápsula (fig. 17D).
Pseudosermyle grupo 3
Huevo: alveolar, de oviposición por caída (fig. 5A), doliforme. Medidas en mm (n = 79): L = 2.14 ± 0.14 (1.82-2.41), W = 1.44 ± 0.11 (1.14-1.64), H = 1.61 ± 0.1 (1.38-1.79), mpl = 1.03 ± 0.09 (0.85-1.26), mpw = 0.5 ± 0.07 (0.38-0.64), oph = 1.05 ± 0.09 (0.82-1.29) y opw = 0.89 ± 0.09 (0.67-1.05). Lámina micropilar en general oblonga y con una longitud cercana a la mitad de la longitud de la cápsula. Lámina micropilar interna abierta con línea media (fig. 6F-I).
Especies incluidas: Pseudosermyle carinulata (Brunner von Wattenwyl, 1907), P. striata (Burmeister, 1838), Pseudosermyle sp. 5 y se incluye a Nooxapty isabelae López-Mora et Llorente-Bousquets, 2023 como parte de este grupo debido a su similitud coriónica, aunque la microestructura es más especializada.
Pseudosermyle carinulata (Brunner von Wattenwyl, 1907) (figs. 1, 6F, 7F, 18, 19)
Material examinado: 7 huevos. México, Edo. de México, Valle de Bravo, bajo mesa, 19°5’9.96” N, 100°4’35.94” O, 2, 201 m snm [voucher: PHMX 416-422 depositados en CNIN y MZFC].
Medidas en μm: (n = 7) L = 1961.4 ± 89.35 (1822.8-2058), W = 1327.2 ± 82.15 (1176-1411.2), H = 1528.8 ± 83.15 (1381.8-1587.6), mpl = 970.2 ± 48 (911.4-1029), mpw = 399 ± 23.13 (382.2-441), oph = 919.8 ± 50.1 (823.2-970.2), opw = 806.4 ± 41.07 (735-852.6), %h/l (elongación) = 77.93 ± 1.96 (74.6-79.41), %w/h (compresión) = 86.78 ± 1.4 (84.9-88.88).
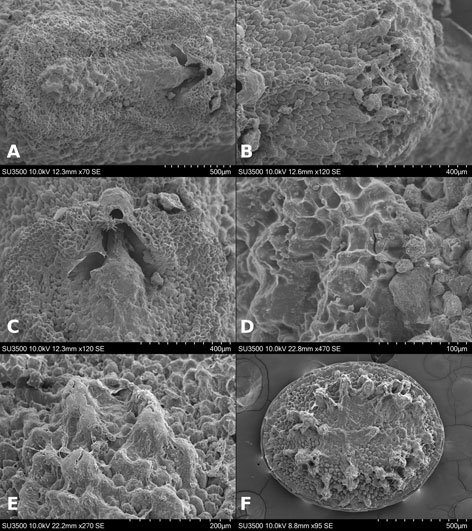
Microestructura: (n = 1) (figs. 18, 19) cápsula de superficie granulosa (fig. 18A, B), con gránulos de diámetro entre 25.7-50.3 μm (fig. 18D), toda la superficie está cubierta por proyecciones digitiformes de altura entre 1.2-2.1 μm y una separación entre ellos de 0.7-3 μm (fig. 18E, F). Lámina micropilar de superficie como en la cápsula (fig. 19A), aunque los gránulos son de textura verrugosa (fig. 19E), el espacio entre los gránulos muestra la misma textura que aquellos de la cápsula (fig. 19E). Borde de una superficie con gránulos menos marcados y con un surco circumperiférico que lo separa del centro de la lámina micropilar (fig. 19A, D), con proyecciones digitiformes muy separadas, mide 76 μm de amplitud. Tubérculo micropilar como una giba más o menos rectangular de 97 μm de longitud y 69 μm de amplitud, su textura es verrugosa (figs. 18A, 19A). Copa micropilar separada del borde, con forma de ‘u’ abierta de 145 μm de amplitud y 22 μm de grosor (fig. 19C). Línea media como una carina de 31 μm de amplitud (figs. 18C, 19B). Las últimas 2 estructuras son de textura verrugosa. Opérculo de superficie granulosa (fig. 19F); la textura de los gránulos es similar a los que tiene la cápsula.
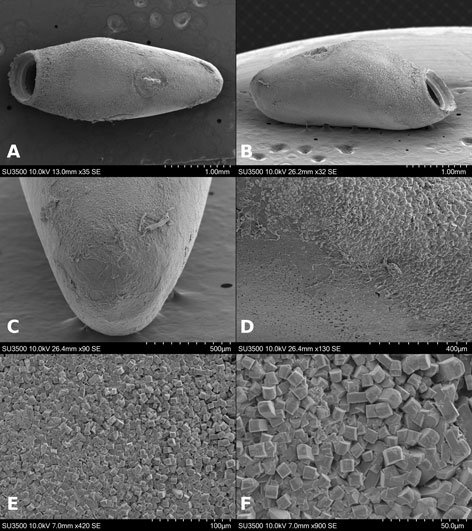
Pseudosermyle striata (Burmeister, 1838) (figs. 1, 6G, 7G, 20, 21)
Material examinado: 45 huevos. México, Puebla, Cuetzalan del Progreso, camino a Tzinacapan, 20°0’59.6088” N, 97°32’23.388” O, 657 m snm [voucher: PHMX 259-303 depositados en CNIN y MZFC]
Medidas en μm: (n = 45) L = 2212.18 ± 91.94 (2028.6-2410.8), W = 1486.98 ± 60.92 (1323-1587.6), H = 1641.82 ± 73.35 (1470-1764), mpl = 1051.21 ± 101.48 (852.6-1264.2), mpw = 529.2 ± 36.54 (441-588), oph = 1069.5 ± 56.16 (940.8-1176), opw = 939.49 ± 51.28 (793.8-1058.4), %h/l (elongación) = 74.21 ± 3.24 (67.53-81.69), %w/h (compresión) = 90.56 ± 3.1 (81.35-98.03).
Microestructura: (n = 1) (figs. 20, 21) cápsula de superficie rugosa en general (fig. 20A, B), con arrugas que varían en tamaño entre 70-170 μm de longitud y 10-45 μm de amplitud (fig. 20D); estas estructuras están cubiertas por una retícula (fig. 20E) donde en cada intersección se produce una proyección cilíndrica o cónica de 1-3 μm de alto y una separación entre ellas de 1-3 μm (fig. 20F); con gránulos alrededor de la lámina micropilar cuyo diámetro mide entre 20-28 μm (figs. 20A, 21A), con textura similar a las arrugas. Lámina micropilar de textura rugosa (fig. 21E), con las arrugas hacia el centro y coliculada hacia el borde (fig. 21A). Borde a modo de carina periférica (fig. 21A); mide 13 μm de amplitud (fig. 21D).
Tubérculo micropilar en forma de triángulo invertido, mide 191 μm de longitud y 128 μm de amplitud (fig. 21A). Copa micropilar separada del borde, con forma de ‘u’ abierta; comienza donde termina el borde, mide 171 μm de amplitud y 24 μm de grosor (fig. 21C). Línea media es una carina con un surco en medio a lo largo, mide 56 μm de amplitud (figs. 20C, 21B). La textura de todas las estructuras anteriores es similar a la que exhiben las arrugas de la cápsula. Opérculo de composición similar a la cápsula, las arrugas suelen ser menos prominentes hacia el centro, el borde del opérculo es una carina periférica (fig. 21F). La textura es similar a la que poseen las arrugas de la cápsula.
Pseudosermyle sp. 5 (figs. 1, 6H, 7H, 22, 23)
Material examinado: 15 huevos. México, Puebla, Cuetzalan del Progreso, camino a Tzinacapan, 20°0’59.6088” N, 97°32’23.388” O, 657 m snm [voucher: PHMX 374-388 depositados en CNIN y MZFC].
Medidas en μm: (n = 15) L = 1969.8 ±89.58 (1822.8-2087.4), W= 1277.92 ± 59.7 (1146.6-1352.4), H = 1495.48 ± 39.85 (1440.6-1587.6), mpl = 1048.6 ± 99.8 (911.4-1234.8), mpw = 392 ± 14.34 (382.2-411.6), oph = 966.28 ± 39.85 (911.4-1029), opw = 746.76 ± 45.54 (676.2-823.2), %h/l (elongación) = 76 ± 2.32 (71.83-79.36), %w/h (compresión) = 85.44 ± 3.02 (79.59-90).
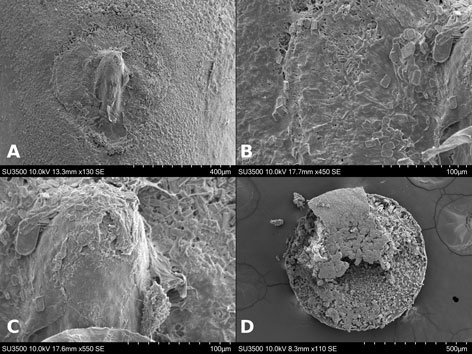
Microestructura: (n = 1) (figs. 22, 23) cápsula de superficie rugosa en general (fig. 22A, B), con arrugas que varían en tamaño, mide entre 67-185 μm de longitud y 9-35 μm de amplitud (fig. 22D, E); estas estructuras están cubiertas por una textura rugulosa con orificios irregulares que varían en diámetro de 0.5-3.2 μm (fig. 22F). Lámina micropilar de superficie como en la cápsula (fig. 23A, E). Borde como un surco de 4.8 μm de amplitud (fig. 23D). Tubérculo micropilar como una giba más o menos rectangular, con 123 μm de longitud y 69 μm de amplitud (fig. 23A). Copa micropilar separada del borde, en forma de ‘u’ abierta, mide 187 μm de amplitud y 54 μm de grosor (fig. 23C). Línea media a modo de carina, mide 35 μm de amplitud (figs. 22C, 23B). La textura es similar a la que muestran las arrugas de la cápsula. Opérculo rugoso (fig. 23F), con arrugas similares a las que exhibe la cápsula y con la misma textura.
Nooxapty isabelae López-Mora et Llorente-Bousquets, 2023 (figs. 1, 6I, 7I, 24, 25)

Material examinado:12 huevos. México, Oaxaca, Totontepec Villa de Morelos, curva 1 Amatepec-Chinantequilla, 17°17’5.46” N, 95°59’18.1032” O, 1,562 m snm [voucher: PHMX 389-400 depositados en CNIN y MZFC].
Medidas en μm (n = 12): L = 2234.4 ± 77.27 (2116.8-2352), W = 1538.6 ± 66.72 (1440.6-1646.4), H = 1724.8 ± 84.4 (1558.2-1793.4), mpl = 1021.65 ± 39.88 (970.2-1087.8), mpw = 590.45 ± 29.28 (558.6-646.8), oph = 1200.5 ± 66.13 (1087.8-1293.6), opw = 980 ± 60.55 (882-1058.4), %h/l (elongación) = 77.2 ± 3.18 (72.6-84.72), %w/h (compresión) = 89.28 ± 3.41 (72.6-84.72).
Microestructura: (n = 1) (figs. 24, 25) cápsula de superficie espinosa (fig. 24A, B); espinas de diámetro entre 21-38 μm y altitud entre 81-211.5 μm (fig. 24A-D). Toda la superficie está cubierta por proyecciones digitiformes de altura entre 1.5-4.5 μm y una separación entre ellos de 1.7-4.4 μm (fig. 24D-F).
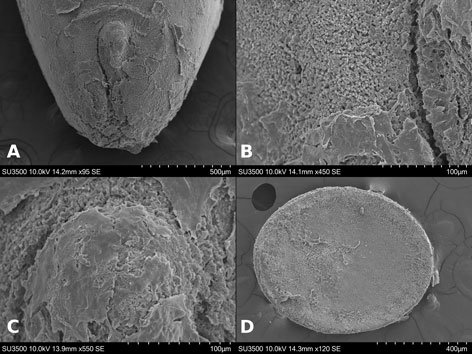
Lámina micropilar cuya ornamentación y textura es similar a la cápsula (fig. 25A). Borde a modo de carina, con una sucesión de espinas unidas (similares a las de la cápsula) (fig. 25A, D). Tubérculo micropilar en forma de ‘y’, a manera de sucesión de espinas; mide 351 μm de longitud total, 199 μm de longitud hasta la bifurcación y 145 μm de longitud en cada brazo de la ‘y’, mide 27 μm de grosor (fig. 25A). Copa micropilar separada del borde, como una ‘u’ abierta, las espinas del borde acaban en los límites de la copa micropilar; mide 153 μm de amplitud y 24 μm de grosor (fig. 25C). Línea media a modo de sucesión de espinas solitarias (figs. 24C, 25B), de amplitud igual al diámetro de las mismas (21-38 μm). La textura en todas las estructuras anteriores es similar a la que posee la cápsula (fig. 25E). Opérculo espinoso con la misma composición, textura y medidas que las espinas de la cápsula; el borde carece de espinas y exhibe un surco que encierra a todas las espinas (fig. 25F).
Pseudosermyle grupo 4
Huevo: alveolar, de oviposición por caída (fig. 5A), doliforme.
Medidas en mm: (n = 105) L = 2.68 ± 0.09 (2.37-2.92), W = 1.69 ± 0.08 (1.38-1.89), H = 1.87 ± 0.08 (1.38-1.89), mpl = 0.74 ± 0.08 (0.58-0.94), mpw = 0.4 ± 0.08 (0.25-0.54), oph = 1.43 ± 0.11 (1.16-1.75) y opw = 1.16 ± 0.09 (0.94-1.42). Lámina micropilar en general oblonga y de longitud cercana a un tercio de la longitud de la cápsula, lámina micropilar interna abierta con línea media (fig. 6J-L).
Especies incluidas: Pseudosermyle phalangiphora (Rehn, 1907), P. procera Conle, Hennemann et Fontana, 2007 y Pseudosermyle sp. 6.
Pseudosermyle phalangiphora (Rehn, 1907) (fig. 1, 6J, 7J, 26, 27)
Material examinado: 45 huevos. México, Veracruz, San Andrés Tuxtla, camino viejo EBTLT, 18°35’9.89988” N, 95°4’31.8” O, 143 m snm [voucher: PHMX 169-213 depositados en CNIN y MZFC].
Medidas en μm: (n = 45) L = 2686.4 ± 101.28 (2372.5-2920), W = 1657.1 ± 82.86 (1387-1898), H = 1826.62 ± 85.58 (1496.5-2007.5), mpl = 829.76 ± 59.46 (693.5-949), mpw = 478.55 ± 42.06 (401.5-547.5), oph = 1460.81 ± 122.66 (1168-1752), opw = 1176.11 ± 113.27 (1022-1423.5), %h/l (elongación) = 68.01 ± 2.52 (63.07-75.34), %w/h (compresión) = 90.76 ± 3.23 (84.61-101.96).
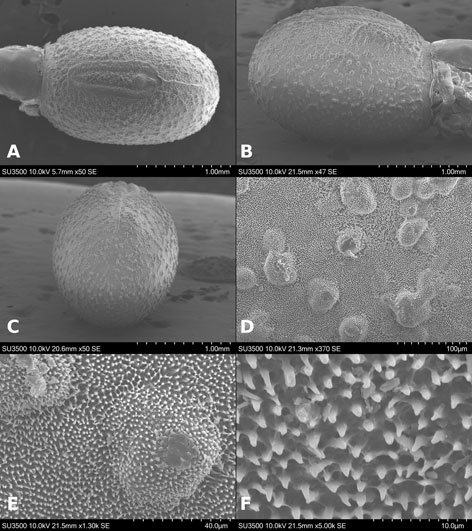
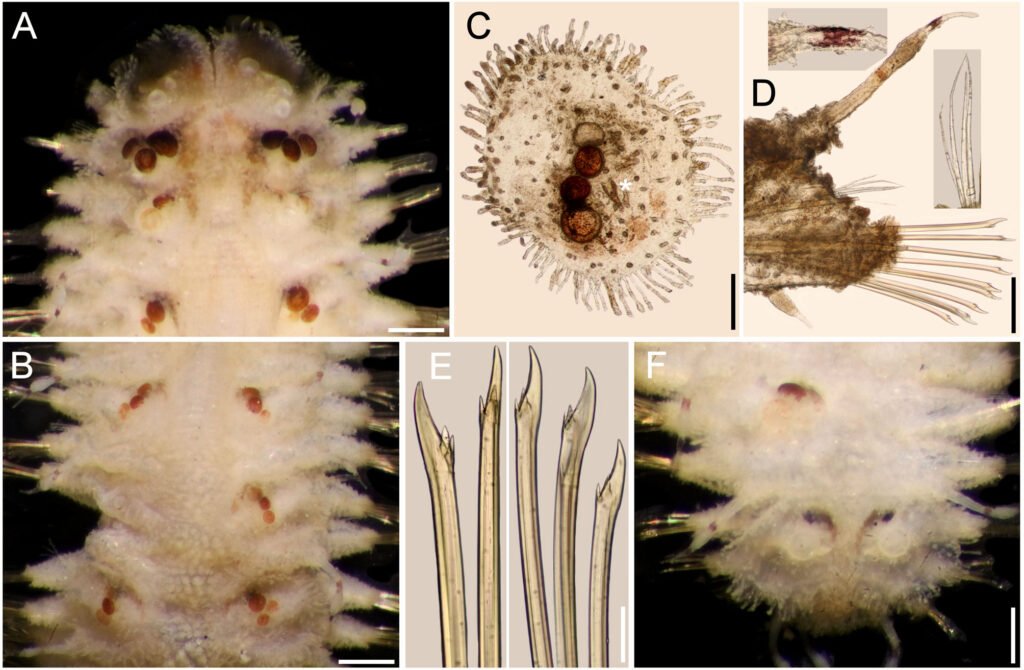
Microestructura: (n = 1) (figs. 26, 27) cápsula de superficie gibosa (fig. 26A, B), con gibas irregulares de diámetro entre 197.05-352.94 μm; suelen exhibir entre 1 y 4 poros de diámetro aproximado de 24 μm (fig. 26D), en el centro de este poro se produce una espina sombrilla (fig. 26D, E) de altura aproximada entre 44-48 μm, cuya amplitud es de 5 μm; la sombrilla de la espina formada por varios lóbulos es de diámetro aproximado de 18 μm (fig. 26E). La textura de la superficie dorsal es foveada (fig. 26D), con fóveas de 20 μm aproximadamente; éstas a su vez están punteadas con orificios de 0.5-1.8 μm de diámetro (fig. 26F); en el área polar en lugar de fóveas se forman gránulos (fig. 26C) de diámetro entre 12.5-17.18 μm.
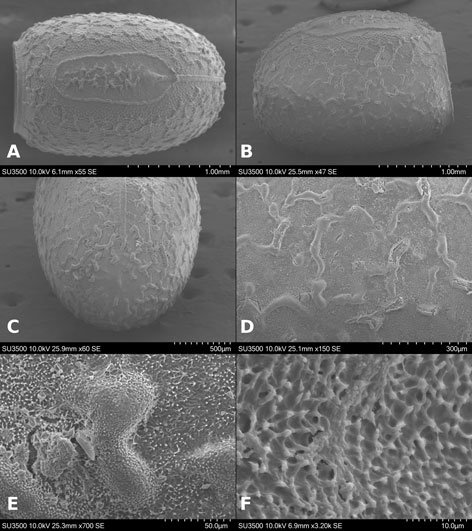
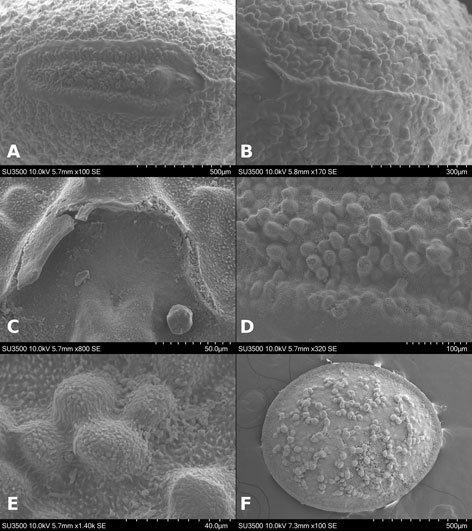
Lámina micropilar con superficie coliculada (fig. 27A) y textura rugulosa (fig. 27E). Borde como una carina de 207 μm de amplitud (fig. 27D); textura similar a la cápsula. Tubérculo micropilar similar a una media esfera de 114 μm de longitud y 153 μm de amplitud (fig. 27A); ornamentación similar a la lámina micropilar. Copa micropilar fusionada al borde con forma de ‘u’, mide 230 μm de amplitud y 129 μm de grosor (fig. 27C). Línea media a modo de carina de 179 μm de amplitud (figs. 26C, 27B). La textura de estas últimas 2 estructuras es similar a la cápsula. Opérculo muestra una giba al centro, mide 73-182 μm de longitud y entre 365-547 μm de amplitud, cuya altura es de 474-839 μm; está giba puede exhibir una muesca al centro, con esto adquiere una apariencia de pequeño cráter; en la cúspide presenta poros con espinas sombrilla del mismo tamaño y forma que los de la cápsula (fig. 27F). La textura es similar a la cápsula; en el borde se forma una carina circumperiférica (fig. 27F).
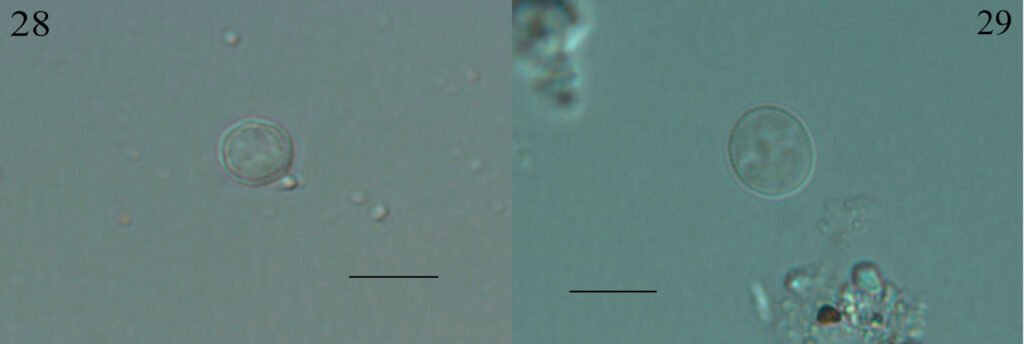
Pseudosermyle procera Conle, Hennemann et Fontana, 2007 (figs. 1, 6K, 7K, 28, 29)
Material examinado: 45 huevos. México, Veracruz, San Andrés Tuxtla, camino viejo EBTLT, 18°35’9.89988” N, 95°4’31.8” O, 143 m snm [voucher: PHMX 214-258 depositados en CNIN y MZFC].
Medidas en μm: (n = 45) L = 2715.6 ± 61.47 (2555-2810.5), W = 1747.13 ± 54.80 (1606-1825), H= 1933.68 ± 54.18 (1788.5-2044), mpl = 682.14 ± 41.77 (584-766.5), mpw = 346.34 ± 55.36 (255.5-438), oph = 1464.05 ± 83.16 (1314-1642.5), opw = 1180.16 ± 57.18 (1095-1277.5), %h/l (elongación) = 71.24 ± 2.06 (67.1-76.71), %w/h (compresión) = 90.36 ± 2.06 (83.92-94.33).
Microestructura: (n = 1) (figs. 28, 29) cápsula con superficie verrugosa (fig. 28A, B), cuyas verrugas miden de diámetro entre 40.8-289.32 μm, de textura rugulosa (fig. 28D, E), compuesta por protuberancias de diámetro de 2.42-8.53 μm (fig. 28E); entre las verrugas la superficie es foveada (fig. 28D), con fóveas de 17.68-28.06 μm de diámetro, e igual que las verrugas son de textura rugulosa (fig. 28F). Lámina micropilar de superficie escasamente coliculada (fig. 29A); textura rugulosa como la cápsula (fig. 29D). Borde a modo de carina (fig. 29A), mide 42 μm de amplitud, textura como en la cápsula (fig. 29C). Tubérculo micropilar como una media esfera de 61 μm de longitud y 80 μm de amplitud (fig. 29A); textura similar a la lámina micropilar. Copa micropilar fusionada al borde (fig. 29B), con forma de ‘u’, de 230 μm de amplitud y 159 μm de grosor, cuya textura es rugulosa. Sin línea media evidente. Opérculo con ornamentación similar a la cápsula, las verrugas forman un anillo periférico (fig. 29E); al centro la superficie es coliculada, pero mantiene la textura rugulosa (fig. 29F).
Pseudosermyle sp. 6 (figs. 1, 6L, 7L, 30, 31)
Material examinado: 15 huevos. México, Oaxaca, Santiago Choápam, curva Choápam-Latani, 17°22’39.9144” N, 95°54’58.5144” O, 701 m snm [voucher: PHMX 401-415 depositados en CNIN y MZFC].
Medidas en μm:(n = 15) L = 2584.2 ± 77.05 (2482-2701), W = 1625.46 ± 43.33 (1569.5-16.79), H = 1834.73 ± 44.63 (1752-1898), mpl = 686.2 ± 31.45 (657-766.5), mpw = 347.96 ± 23.35 (292-365), oph = 1270.2 ± 41.84 (1168-1350.5), opw = 1085.26 ± 54.25 (949-1131.5), %h/l (elongación)= 71.01 ± 1.27 (68.49-72.85), %w/h (compresión) = 88.63 ± 2.81 (84.31-93.87).
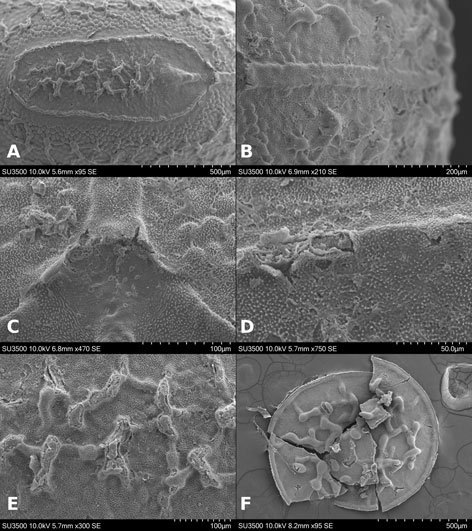
Microestructura: (n = 1) (figs. 30, 31) cápsula coliculada (fig. 30A, B) con gránulos de 31.30-51.20 μm de diámetro, superficie rugulosa con verrugas de 1.76-4.12 de diámetro (fig. 30D, F). Las espinas sombrilla por lo general en grupos de al menos 3 (fig. 30E), aunque en ocasiones se encuentran solitarias; su altura es de 47-51 μm, su amplitud entre 5.9-10 μm; la sombrilla de la espina está formada por un círculo con diámetro entre 47.64-59.24 μm (fig. 30E). Lámina micropilar con ornamentación similar a la cápsula, pero carece de espinas sombrilla (fig. 31A). Borde a modo de carina de 49 μm de amplitud (fig. 31A, D), su textura rugulosa (fig. 31D). Tubérculo micropilar como un triángulo invertido de 252 μm de longitud y 155 μm de amplitud (fig. 31A); textura similar a la lámina micropilar (fig. 31E). Copa micropilar fusionada al borde, en forma de ‘u’, mide 139 μm de longitud y 48 μm de grosor (fig. 31C), de textura rugulosa como la cápsula. Línea media como una sucesión de gránulos (fig. 31B), puede exhibir espinas sombrilla; de 322 μm de longitud y 89 μm de amplitud, de textura rugulosa. Opérculo con espinas sombrilla que forman un anillo concéntrico rodeado de textura coliculada; al centro presenta la misma textura y algunas espinas sombrilla (fig. 31F).
Comportamiento de oviposición. Los grupos encontrados presentan 3 comportamientos distintos de oviposición: 1) por caída, para las especies: P. striata, P. carinulata, Pseudosermyle sp. 5 y Nooxapty isabelae del grupo 3 y P. phalangiphora, P. procera y Pseudosermyle sp. 6 del grupo 4 (fig. 5A); 2) pegados en sustrato, para las especies: Pseudosermyle sp. 1, Pseudosermyle sp. 2 y Pseudosermyle sp. 3 del grupo 1 (fig. 5B); y 3) agrupados en ooteca, para las especies: P. tridens y Pseudosermyle sp. 4 del grupo 2 (fig. 5C).
Variabilidad morfológica del huevo. Los caracteres constantes entre los grupos son: tipo de oviposición, tipo de huevo, forma de la cápsula, ángulo opercular, número de capas presentes en el opérculo, porcentaje de cobertura de la longitud de la lámina micropilar (mpl) con respecto a la longitud de la cápsula (L), forma de la lámina micropilar interna y posiciones del tubérculo y copa micropilar. Por lo tanto, suponemos que son caracteres relevantes para identificar los grupos obtenidos por PCA y nos permiten definirlos. En contraste, los caracteres como ornamentación y textura de la cápsula, opérculo, lámina micropilar y línea media son caracteres variables entre especies, pero constantes entre los huevos de distintas hembras de la misma especie. Podemos suponer que estos caracteres son específicos (tablas 10-12). A continuación, se discuten a nivel de grupo los caracteres mencionados como específicos y algunas de sus posibles tendencias.
Discusión
Las especies dePseudosermyle presentan distintos tipos de morfología del huevo, lo que nos permite reconocer 4 grupos, con Nooxapty isabelae próximo al grupo 3. Se reconocen 2 tipos de huevo, alveolar (grupos 3 y 4) y adhesivos (grupos 1 y 2); con 3 comportamientos de oviposición: por caída (grupos 3 y 4), adheridos al sustrato (grupo 1) e incluidos en 1 ooteca (grupo 2); se admiten 4 grupos acorde a las medidas obtenidas por PCA, que coinciden con aquellos reconocidos cualitativamente con otras estructuras (morfología del macho y la hembra). Esta diferenciación permite proponer el reconocimiento de 4 unidades ovocíticas distintas dentro de Pseudosermyle. Se observó que dentro de cada grupo existen ciertas características comunes en la morfología del huevo (tablas 10-12); pero a su vez existen diferencias suficientes entre las especies que los conforman (tablas 10-12). Por lo tanto, se puede reconocer y diferenciar de manera inequívoca a cada especie y el grupo al que pertenece. Las ilustraciones de P. truncata y Bacteria cacica Kaup, 1871 (sinónimo deP. tridens [Hebard, 1932]) corresponden conel patrón del huevo que encontramos en el grupo 1.
En cambio, la ilustración provista por Zompro (2001) de P. tridens sigue el patrón del grupo 2, lo que sugiere queB. cacica fue sinonimizada equivocadamente conP. tridens por Hebard (1932). Consideramos que es indispensable revisar más organismos de estas 2 especies con la finalidad de examinar esta sinonimia posiblemente errónea y reconocer a B. cacica como especie válida. Por último, P. phalangiphora corresponde con el grupo 4; no obstante, la morfología coriónica ilustrada por Conle et al. (2007) no corresponde con la encontrada en el presente trabajo. Conle et al.(2007) mencionan que esta especie es muy variable en sus genitales, por ende, una revisión detallada es necesaria para clarificar si se trata de variación intraespecífica o bien de 2 especies distintas con algunos caracteres homoplásticos.
Cabe destacar que en nuestro estudio se encontró un tipo de oviposición que previamente solo había sido registrado para la subfamilia Korinninae (hoy Necrosciinae) por Goldberg et al. (2015). Éste representa el segundo caso de formación de ooteca en Phasmatodea y a su vez una convergencia para ambos casos. Nuestros resultados representan el primer registro para América y el primero en la familia Diapheromeridae. Hay diferencia entre las ootecas de ambos taxones referente a la forma en la que los huevos están acomodados; mientras en Korinninae los huevos están acomodados de forma radial y se generan 4 cámaras, en nuestro caso, en el grupo 2de Pseudosermyle están acomodados en líneas sin formación de cámaras.
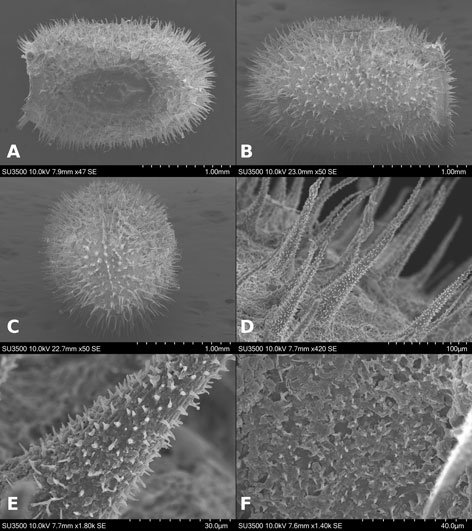
Debido a que las especies con ootecas, en este estudio, provienen de ambientes con temporada seca muy marcada como el matorral xerófilo y la selva baja subcaducifolia, deducimos que la formación de una ooteca con cápsula muy dura y ancha posiblemente evita que los huevos se desequen; tal como Salas-Araiza et al. (2013) reportan para algunos Acrididae hallados en matorral xerófilo, pues se trata de una adaptación a medios xéricos. Otro aspecto importante del fenómeno es que una condición previa a la formación de una ooteca es la presencia de huevos pegados a un sustrato, tal y como lo mencionan Robertson et al. (2018); en nuestro caso, también encontramos ese comportamiento de oviposición (grupo 1) en el mismo género donde se presentan ootecas. Para poner a prueba esta aseveración, es necesario realizar un análisis filogenético donde se incluyan más especies de Pseudosermyle y así examinar el proceso en términos de posibles tendencias evolutivas, de acuerdo con las secuencias reconocidas.
El huevo en Pseudosermyle es diferente en todas las especies respecto a su forma, texturas y la disposición de sus ornamentaciones, que son exclusivas de cada especie; además, estas características se agrupan en patrones más generales, que reconocemos como grupos. Asimismo, estos caracteres son constantes entre los huevos de distintas hembras de la misma especie. Dentro de Phasmatodea, las hembras de muchas especies son muy similares y el huevo ha sido un primer paso para reconocer si pertenecen a la misma o a distintas especies. A continuación, se listan los casos donde este carácter fue útil como primer paso en el reconocimiento de especies muy similares.
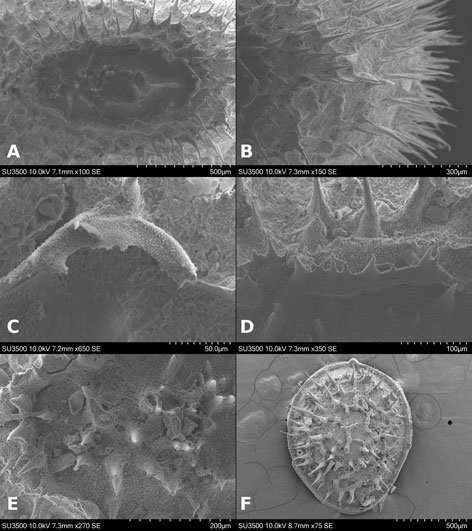
El primer caso corresponde con P. striata y Pseudosermyle sp. 5, donde son simpátridas e incluso los machos se parecen mucho. Al inicio, se pensó que pertenecían a la misma especie, hasta que se analizaron los huevos bajo el estereoscopio y el MEB. Se registró que los huevos eran diferentes en varios aspectos, como la ornamentación y la textura de la cápsula, la forma de la lámina micropilar y el opérculo. Entonces, para corroborar que se trataba de 2 especies distintas, se realizó la técnica descrita en materiales y método, con lo cual se confirmó nuestra hipótesis.
El segundo caso se dio entre P. phalangiphora y P. procera, que también son simpátridas. Se realizó el mismo procedimiento descrito en materiales y método. Las diferencias entre los huevos fueron la ornamentación de la cápsula, el opérculo y la presencia del relieve micropilar. En este caso, las diferencias entre machos eran conspicuas, así que la pregunta fue ¿cuál hembra y qué huevo correspondía a qué macho? Al igual que en el caso anterior, la respuesta se obtuvo al criar separadamente las ninfas eclosionadas de las 2 morfologías tal y como se describe en materiales y método. Después de obtener los adultos se pudo asignar a las hembras con sus respectivos machos y confirmar la continuidad morfológica con la reproducción.
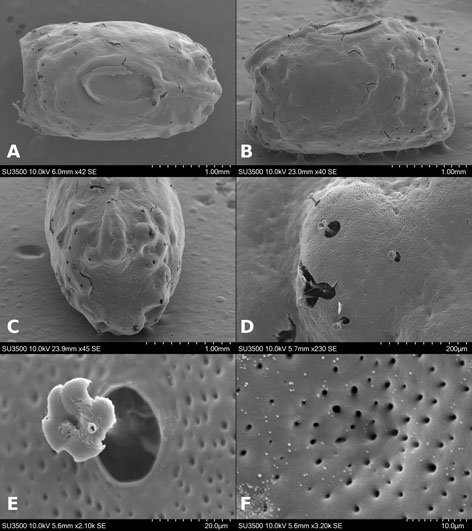
El tercer caso es entre P. tridens y Pseudosermyle sp. 4, las diferencias entre machos suelen ser igual de sutiles que las mostradas entre hembras. En ese caso, las especies no son simpátridas y se pensaba que ambas eran una única especie, pues presentaban oviposición en ooteca y morfología genital similar. Por esta causa se recurrió a la disección de hembras para obtener los huevos y realizar la comparación; entonces se encontraron las primeras diferencias, pues la lámina micropilar de P. tridens es circular y está cerca del centro de la cápsula; la lámina de Pseudosermyle sp. 4 es un triángulo invertido desplazado al área polar. Para corroborarlo se obtuvo la primera generación de Pseudosermyle sp. 4, donde las hembras y los machos presentaban la misma morfología que los parentales; también se observó que los huevos tenían la misma morfología. El cultivo de P. tridens no se logró; cabe mencionar que fue hasta la observación de los huevos que se pudo determinar a P. tridens, pues el huevo es similar a la ilustración de Zompro (2001).
Con estos casos verificamos que la afirmación de Robertson et al.(2018) sobre la especificidad del huevo a nivel de especie es cierta para este clado de Phasmatodea. Al seguir esta aseveración pudimos notar que la imagen presentada porConle et al.(2007) del huevo de P. phalangiphora de un cultivo de Belice, puede ser una especie distinta a la que reconocemos aquí como P. phalangiphora.
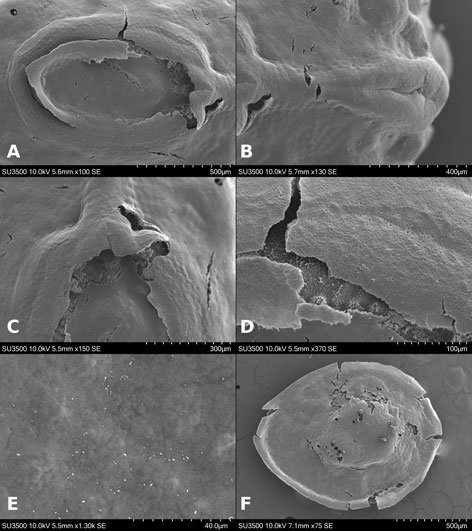
Sin embargo, es complicado conocer la identidad con certeza, pues los autores anteriores mencionan que esta especie presenta gran variabilidad en los caracteres masculinos y femeninos; en consecuencia, aquí reconocimos a los ejemplares que entraban dentro del rango de variabilidad de P. phalangiphora como esta especie, aunque una revisión más exhaustiva de los caracteres de ésta y otras poblaciones es indispensable.
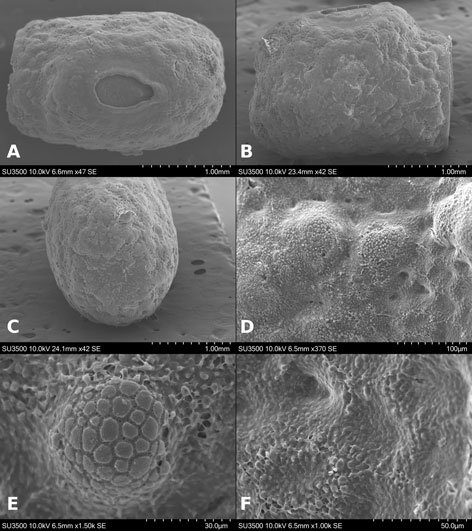
Los grupos 1 y 3 exhiben gránulos, pero la diferencia entre sus texturas es lo que los diferencia, pues el grupo 1 presenta gránulos como basamentos piramidales y el grupo 3 como semicírculos. También se observa una tendencia a aumentar o disminuir el número de niveles en el basamento piramidal y por lo tanto el tamaño del gránulo en el grupo 1; por el momento, hacen falta estudios comparativos que incluyan más especies, para después postular una posible tendencia (aumentar o disminuir el número de niveles en los basamentos piramidales) a este carácter, después de un ulterior análisis filogenético. El grupo 2 presenta especies que carecen de copa micropilar y línea media.
El grupo 3 se aproxima al género Nooxapty, por lo que se podría sugerir que al menos a nivel de medidas coriónicas son similares en forma. Este grupo exhibe gran variación en la microestructura coriónica de sus estructuras (tablas 10-12). La diferencia mayor entre Nooxapty y el grupo 3 es la presencia de espinas en el primero y de gránulos en el segundo. Se reconoce una tendencia de los gránulos a formar arrugas, pero se carece de hipótesis filogenética del género, que nos permita realizar una comparación precisa sobre tal tendencia. Además, el hecho que Nooxapty esté agrupado dentro de este grupo sugiere la necesidad de revisar estos caracteres bajo un enfoque filogenético, para aclarar si la similitud morfológica se debe a simplesiomorfías o a convergencia. Consideramos que un análisis filogenético nos permitiría contrastar y conocer los alcances de las medidas coriónicas, la ornamentación y la microestructura al momento de definir los géneros en Phasmatodea.
El grupo 4, al igual que el 3, exhibe gran variación en su microestructura coriónica (tablas 10-12). Bradler (2009) agrupa las 2 especies (P. phalangiphora y P. incongruens [Brunner von Wattenwyl, 1907]) dentro del género Pseudosermyle por presentar cercos asimétricos y con 2 ápices.Las demás, P. neptuna (Brunner von Wattenwyl, 1907), P. tridens (cercos con 3 ápices)y P. striata (con cercos simples), junto con este clado, forman un grupo monofilético a manera de peine, cuya sinapomorfía es la reducción del segundo esclerito del “poculum”. En particular, consideramos que tal variación en los cercos es muy grande y podría estar agrupando entidades distintas, por ejemplo, géneros distintos. En el presente trabajo mostramos evidencia que sustenta la formación de 4 grupos al usar la morfología coriónica y que cualitativamente observamos una correspondencia entre estos grupos y la morfología de los adultos. Sin embargo, se debe poner a prueba esta hipótesis bajo un enfoque filogenético que incluya más grupos de caracteres (v. gr. genitales internos) y especies.
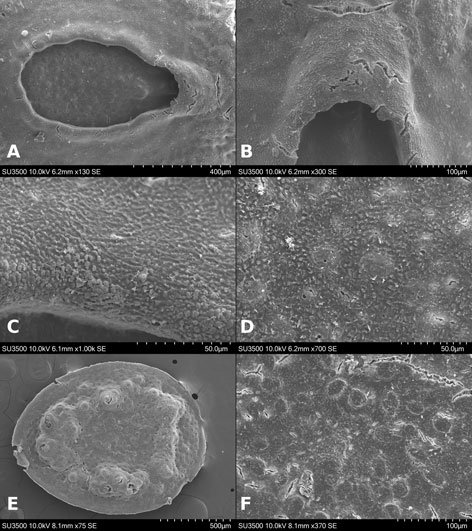
A grandes rasgos, los caracteres como textura, forma de tubérculo micropilar, borde de la lámina micropilar, línea media externa y ornamentación (tablas 10-12) son de utilidad específica entre las especies. Para hacer más robusta esta hipótesis es necesario poner a prueba estos caracteres bajo un análisis filogenético, en el cual se deben considerar más especies de cada grupo. En los análisis previos, los grupos 1, 2 y 3 solo están representados por una especie y el grupo 4 por 2 especies (Bradler, 2009); mientras que el grupo 4 se ha incluido en análisis que consideran a todo Phasmatodea (Goldberg et al. 2015; Robertson et al. 2018) y Pseudosermyle no se incluyó en los análisis de Whiting et al. (2003) y Bradler et al. (2014), pese a ser el género con mayor diversidad en América del Norte (de Luna, 2022); esto evidencia la falta de información en un género tan ampliamente distribuido.

Medidas coriónicas. Cuando aplicamos PCA a las medidas de huevo (L, W, H, mpl, mpw, oph y opw) obtuvimos 4 agrupaciones, que corresponden con los patrones generales del huevo explicados anteriormente. Al revisar la contribución de las variables a cada componente (fig. 4), nos percatamos de que la longitud de la cápsula (L), la altitud (oph) y amplitud (opw) del opérculo, así como la longitud micropilar (mpl) son las medidas coriónicas que mejor explican la variación de la forma del huevo. Podemos observar que L es una variable independiente de las restantes y la que más contribuye al componente 1 (fig. 4); mientras que oph y opw están más correlacionadas positivamente con la amplitud (W) y altitud (H) de la cápsula, las variables que más contribuyen al componente 2 (fig. 4). En cambio, mpl es la variable que más contribuye al componente 3 (fig. 4) y su correlación es inversamente proporcional a oph y opw; podemos destacar que cada estructura del huevo (cápsula, lámina micropilar y opérculo) está aportando una de las medidas que lo caracterizan. En consecuencia, recomendamos que al momento de realizar descripciones del huevo se incluyan todas las medidas mencionadas.
Las medidas del huevo nos permiten distinguir 4 grupos, que además son congruentes con otros caracteres. Esto podría indicar que el género Pseudosermyle pueda estar conformado por géneros distintos, como lo sugiere Conle et al. (2007), quienes llegan a esta conclusión debido a la variabilidad de formas en los genitales de los machos. Ellos admiten que el conocimiento del género es fragmentado, en consecuencia, no realizan una redescripción del mismo. Así también, ninguna de las especies que ellos describen sigue la descripción original de Pseudosermyle pues no cumplen con las características que menciona Caudell (1903); sin embargo, coinciden con la redescripción que realizó Zompro (2001). En contraste, resaltamos que las medidas por sí solas no son suficientes en la caracterización del huevo pues N. isabelae, por sus medidas, se aproxima al grupo 3, pero al revisar la microestructura notamos que la ornamentación es distinta entre esta especie y las restantes dentro del grupo, pues exhibe espinas, mientras que las demás presentan arrugas y gránulos. En conclusión, notamos que la microestructura, como sugieren Mazzini y Scali (1983), es bastante útil al reconocer especies cercanas dentro del mismo género.
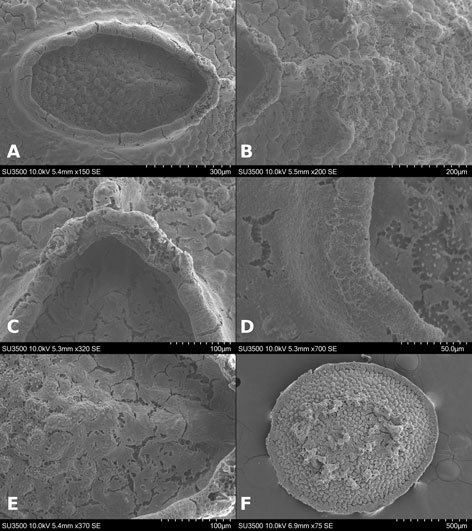
Por último, es importante destacar que Pseudosermyle exhibe gran variabilidad en los caracteres morfológicos del huevo, por lo cual consideramos que para aclarar si estos caracteres nos permiten inferir distintos géneros o representan variabilidad dentro del mismo, es indispensable revisar más caracteres, v. gr., genitales externos e internos para ambos sexos y observar una correspondencia entre los mismos. Así mismo, es necesario efectuar un análisis filogenético que nos permita postular hipótesis evolutivas sobre el género y sus caracteres o rasgos. Las especies restantes de Pseudosermyle no fueron incluidas en este trabajo debido a la carencia de tiempo y recursos para recolectar un área tan vasta como México, América Central y el sur de Estados Unidos. Por lo tanto, en el futuro será oportuno un trabajo más exhaustivo que incluya lo antes mencionado y amplíe el número de especies analizadas. Aún queda mucho trabajo por realizar con Pseudosermyle, pues al igual que muchos géneros de Phasmatodea americanos, se desconoce su bionomía.
Agradecimientos
Al posgrado en Ciencias Biológicas, UNAM, por el financiamiento a la beca de Secihti (cvu: 599426 y cvu: 1039296). A Susana Guzmán Gómez por la asistencia técnica en las micrografías en el Laboratorio de Microscopia y Fotografía de la Biodiversidad II, IB UNAM. A Arturo Arellano Covarrubias por la asesoría en la realización del mapa. A Isabel Vargas Fernández y María Berenit Mendoza Garfias por su asistencia técnica al montar las muestras y tomar las fotomicrografías con microscopio electrónico de barrido. Isabel Vargas ayudó críticamente en la elaboración de las figuras. JLB agradece al proyecto PAPIIT-UNAM IN 202415. ULM agradece a la Orthopterists Society por el Theodore J. Cohn Research Fund. Por último, agradecemos a 2 revisores anónimos en la revisión previa del presente manuscrito.
Referencias
Adler, D., Murdoch, D. Nenadic, O., Urbanek, S., Chen, M., Gebhardt, A. et al. (2018). rgl: 3D Visualization Using OpenGL. R package version 0.99.16. Recuperado el 10 junio 2019 de: https://cran.r-project.org/web/packages/shinyRGL/index.html
Allred, M. L., Stark, B. P. y Lentz; D, L. (1986). Egg capsule morphology of Anisomorpha buprestoides (Phasmatodea: Pseudophasmatidae). Entomological News, 97, 169–174.
Bradler, S. (2009). Die Phylogenie der Stab- und Gesepnstruchrecken (Insecta: Phasmatodea). Species, Phylogeny and Evolution, 2, 3–139. https://doi.org/10.17875/gup2009-710
Bradler, S. y Buckley, T. R. (2018). Biodiversity of Phasmatodea. En R. G. Foottit y P. H. Adler (Eds.), Insect biodiversity: science and society, Volumen II (pp. 281–313). Ottawa: Jonh Wiley & Sons Ltd. https://doi.org/10.1002/9781118945582.ch11
Bradler, S., Robertson, J. A. y Whiting, M. F. (2014). A molecular phylogeny of Phasmatodea with emphasis on Necrosciinae, the most species-rich subfamily of stick insects. Systematic Entomology, 39, 205–222. https://doi.org/10.1111/syen.12055
Brock, P. D., Büscher, T. y Baker; E, (2023). Phasmida Species File Online. Versión 5.0/5.0 Recuperado el 20 abril 2019 de: https://phasmida.speciesfile.org/
Camousseigth, A. y Bustamante, I. (1991). Descripción de los huevos de los fásmidos (Phasmatodea: Pseudophasma-
tidae) de Chile. Revista Chilena de Entomología, 19, 39–43.
Caudell, A. N. (1903). The Phasmidae or walkingsticks, of the United States. Proceedings of the United States National Museum, 26, 863–885. https://doi.org/10.5479/si.00963801.26-1335.863
Caudell, A. N. (1914). The egg of Pseudosermyle truncata Caudell. Proceedings of the Entomological Society of Washington, 16, 96.
Clark, J. T. (1976a). The capitulum of phasmid eggs (Insecta: Phasmida). Zoological Journal of the Linnean Society, 59, 365–614. https://doi.org/10.1111/j.1096-3642.1976.tb01019.x
Clark, J. T. (1976b). The eggs of stick insects (Phasmida): a review with descriptions of the eggs of eleven species. Systematic Entomology, 1, 95–105. https://doi.org/10.1111/j.1365-3113.1976.tb00342.x
Clark, J. T. (1979). A key to the eggs of stick and leaf insects (Phasmida). Systematic Entomology, 4, 325–331. https://doi.org/10.1111/j.1365-3113.1979.tb00617.x
Conle, O. V., Hennemann, F, H. y Fontana, P. (2007). Studies on Neotropical Phasmatodea V: notes on certain species of Pseudosermyle Caudell, 1903, with the descriptions of three new species from Mexico (Phasmatodea: Diapheromeridae: Diapheromerinae: Diapheromerini). Zootaxa, 1496,31–51. https://doi.org/10.11646/zootaxa.1496.1.2
de Luna, M. (2022). Checklist of stick insects (Insecta: Phasmatodea) of North America, with three new records for Nuevo León, México. Phasmid Studies, 21, 90–105.
GNU Image Manipulation Program (GIMP 2.8.22). Recuperado el 10 junio 2019 de: https://www.gimp.org/
Goldberg, J., Bresseel, J., Constant, J., Kneubühler, B., Leubner, F., Michalik, P. et al. (2015) Extreme convergence in egg-laying strategy across insect orders. Scientific Reports, 5, 7825. https://doi.org/10.1038/srep07825
Harris, R. A. (1979). A glossary of surface sculpturing. Occasional Papers in Entomology, 28,1–31.
Hebard, M. (1932). New species and records of Mexican Orthoptera. Transactions of the American Entomological Society, 58,201–219.
Horikoshi, M. y Tang, Y. (2016). ggfortify: data visualization tools for statistical analysis results. Recuperado el 10 de junio de 2019 de: https://doi.org/10.32614/cran.package.ggfortify
Jintsu, Y., Uchifune, T. y Machida, R. (2010). Structural features of egg of the basal Phasmatodean Timema monikensis Vickery et Sandoval, 1988 (Insecta: Phasmatodea: Timematidae). Arthropod Systematics & Phylogeny, 68, 71–78. https://doi.org/10.3897/asp.68.e31716
Kaup, J. (1871). Ueber die Eier der Phasmiden. Berliner Entomologische Zeitschrift, 15, 17–24. https://doi.org/10.
1002/mmnd.18710150106
López-Mora, U. y Llorente-Bousquets, J. (2018). Lista de especies y clave ilustrada de los géneros de Phasmato-
dea (Insecta) de México. Revista Mexicana de biodiversidad, 89, 46–78. https://doi.org/10.22201/ib.2007
8706e.2018.1.2175
López-Mora, U. y Llorente-Bousquets, J. (2023). Nooxapty gen. nov. con dos especies nuevas (Phasmatodea: Diapheromeridae) de Oaxaca, México. Dugesiana, 30, 11–33. https://doi.org/10.32870/dugesiana.v30i1.7272
Mazzinni, M., Carcupino, M. y Fausto, A. M. (1993). Egg chorion architecture in stick insects (Phasmatodea). International Journal of Insect Morphology and Embriology,22, 391–415. https://doi.org/10.1016/0020-7322(93)90021-r
Mazzini, M., Nascetti, G. y Bullini, L. (1982). The egg of the stick-insect Bacillus atticus caprai Nascetti et Bullini: a scanning electron microscope study (Cheleutoptera Bacillidae). Italian Journal of Zoology, 16, 93–103. https://doi.org/10.1080/01688170.1984.10510070
Mazzini, M., Nascetti, G. y Bullini, L. (1984). A scanning electron microscope study on the egg of a hybrid stick-insect (Cheleutoptera, Bacillidae). International Journal of Invertebrate Reproduction and Development, 7, 43–49. https://doi.org/10.1080/01688170.1984.10510070
Mazzini, M. y Scali, V. (1977). Fine structure of the insect micropyle. Scannin electron microscope investigations of the egg of the stick insect Bacillus rossius (Rossi) (Insecta Cheleutoptera). Monitore Zoologico Italiano-Italian Journal of Zoology, 11, 71–82. https://doi.org/10.1016/0020-7322(77)90020-4
Mazzini, M. y Scali, V. (1980). Eggs of the stick insects, Lonchodes pterodactylus Gray and Carausius morosus Br. (Phasmatodea: Heteronemiidae). International Journal of Insect Morphology & Embriology,9, 369–382. https://doi.org/10.1016/00207322(80)90010-0
Mazzini, M. y Scali, V. (1983). A scanning electron microscope study of the eggs of three stick insect species of Ramulus (Phasmatodea Heteronemiidae) from Somalia. Italian Journal of Zoology, 17, 89–103.
Nieves-Uribe. S., Llorente-Bousquets, J. y Flores-Gallardo, A. (2021). Toward standards in practices and techniques on ootaxonomy in the Pieridae (Lepidoptera: Papilionoidea). Zootaxa,4985, 301–344. https://doi.org/10.11646/zootaxa.4985.3.1
Ooms, J. (2018). magick: advanced graphics and image-processing in R. R package version 2.0. Recuperado el 10 junio 2019 de: https://CRAN.R-project.org/package=magick https://doi.org/10.32614/cran.package.magickgui
QGIS Dveelopment Team, (2019). QGIS Geographic Information System. Open Source Geospatial Foundation Project. Recuperado el 10 junio 2019 de: https://qgis.org.
R Core Team. (2013). R: a language and environment for statistical computing. R foundation for Statistical Computing, Vienna, Austria. Recuperado el 10 junio 2019 de: http://www.R- project.org/
Robertson, J. A., Bradler, S. y Whiting, M. F. (2018). Evolution of oviposition techniqus in stick and leaf insects (Phasmatodea). Frontiers in Ecology and Evolution, 6, 2016. https://doi.org/10.3389/fevo.2018.00216
RStudio Team (2015). RStudio: Integrated Development for R. RStudio, Inc., Boston, MA. Recuperado el 10 de junio de 2019 de: http://www.rstudio.com/. https://doi.org/10.4135/9781526472557
Salas-Araiza, M. D., Mackay, W. P., Valdez-Carrasco, J., Salazar-Solís; E, y Martínez-Jaime, O. A. (2013). Characterization and comparison of the eggs of seven species of Mexican grasshoppers. Southwestern Entomologist, 38,267–274. https://doi.org/10.3958/059.038.0210
Scali, V. y Mazzini, M. (1977). Fine morphology and amino acid analysis of the egg capsule of the stick insect, Clonopsis gallica (Charp.) (Cheleutoptera: Bacillinae). International Journal of Insect Morphology and Embryology, 6,
255–264. https://doi.org/10.1016/0020-7322(77)90020-4
Scali, V. y Mazzini, M. (1981). The eggs of stick insects, Sipyloidea sipylus (Westwood) and Orxines macklotti De Haan (Phasmatodea, Heteronemiidae). International Journal of Invertebrate Reproduction, 4, 25–38. https://doi.org/10.1080/01651269.1981.10553416
Scali, V. y Mazzini, M. (1982). Interpopulation differences in egg sculpturing of the stick insect, Clonopsis gallica (Charp.) (Phasmatodea: Bacillidae). International Journal of Insect Morphology and Embriology, 11, 189–195.
https://doi.org/10.1016/s0020-7322(82)80004-4
Scali, V. y Mazzini, M. (1983). Egg capsule morphology of the stick insect Burria longixipha Brunner (Phasmatodea Heteronemiidae) from Somaliland. Italian Journal of Zoology, 17, 303–312.
Seiler, C., Bradler, S. y Koch, R. (2006). Fásmidos: insectos palo e insectos hoja. España: Hispano Europea.
Sellick, J. T. C. (1994). A redefinition of the orientation terminology of phasmid eggs. Phasmid Studies, 3, 1–2.
Sellick, J. T. C. (1997a). The range of egg capsule morphology within the Phasmatodea and its relevance to the taxonomy of the order. Italian Journal of Zoology,64, 97–104. https://doi.org/10.1080/11250009709356178
Sellick, J. T. C. (1997b). Descriptive terminology of the phasmid egg capsule, with an extended key to the phasmid genera based on egg structure. Systematic Entomology,22, 97–122. https://doi.org/10.1046/j.1365-3113.1997.d01-30.x
Sellick, J. T. C. (1997c). The “umbrella spines” and other surface projections of some phasmid eggs and some comments on phasmid taxonomy. Phasmid Studies, 6, 15–20. https://doi.org/10.1111/j.1096-3642.1988.tb01364.x
Sellick, J. T. C. (1998). The micropylar plate of the eggs of Phasmida, with a survey of the range of plate form within the order. Systematic Entomology, 23, 203–228. https://doi.org/10.1046/j.1365-3113.1998.00056.x
Severin, H. P. (1910). A study on the structure of the egg of the walking-stick Diapheromera femorata Say. Annals of The Entomological Society of America, 3, 83–92. https://doi.org/10.1093/aesa/3.2.83
Stark, B. P. y Lentz; D, L. (1986). Morphology of the egg capsule in Megaphasma dentricus (Phasmatodea: Heteronemiidae). Journal of the Kansas Entomological Society, 52, 398–401.
Whiting, M. F., Bradler, S. y Maxwell, T. (2003). Loss and recovery of wings in stick insects. Letter to Nature, 421, 264–267. https://doi.org/10.1038/nature01313
Wickham, H. (2016). ggplot2: elegant graphics for data analysis. Nueva York: Springer-Verlag.
Weiner, J. (2017). pca3d: Three dimensional PCA plots. R package version 0.10. Recuperado el 10 junio 2019 de: https://CRAN.R-project.org/package=pca3d
Zompro, O. (2001). A generic revision of the insect order Phasmatodea: the new world genera of the stick insect subfamily Diapheromeridae: Diapheromerinae = Heteronemiidae: Heteronemiinae sensu Gradley et Galil, 1977. Revue Suisse de Zoologie, 108, 189–255. https://doi.org/10.5962/bhl.part.79626