Illustrated keys for the identification of species and tribes of Scolytinae (Coleoptera: Curculionidae) from Tucumán Province, Argentina
Silvia Patricia Córdoba a, * y Thomas H. Atkinson b
a Fundación Miguel Lillo, Instituto de Entomología, Área de Zoología, Miguel Lillo 251, 4000 San Miguel de Tucumán, Argentina
b University of Texas at Austin, University Texas Insect Collection, Lake Austin Center 3001 Lake Austin Boulevard, Suite 1.314, Austin, 78703 Texas, EUA
*Autor para correspondencia: spcordoba@lillo.org.ar (S.P. Córdoba)
Recibido: 08 abril 2025; aceptado: 25 septiembre 2025
Resumen
La subfamilia Scolytinae es reconocida por comprender especies de importancia forestal, frutícola y ornamental debido a su impacto económico y por poseer la función, desde el punto de vista ecológico, de regular las poblaciones vegetales con las que se asocian. Para la Argentina, no existen claves para la determinación de las tribus y especies, por lo que en el presente trabajo se incluye una para la identificación de las tribus y 12 claves para la identificación de 56 especies, como así también su distribución en América del Sur y Argentina. También se añaden fotografías del aspecto general y caracteres más importantes de cada especie.
Palabras clave: Escarabajos descortezadores; Escarabajos de ambrosía; América del Sur; Tucumán; Distribución; Forestal
Abstract
The subfamily Scolytinae is recognized for comprising species of forestal, fruit, and ornamental importance due to their economic impact and their ecological role in regulating the plant populations with which they are associated. For Argentina, there are no keys for identifying the tribes and species; therefore, this work includes a key for identifying the tribes and 12 keys for identifying 56 species, as well as their distribution in South America and Argentina. Photographs of the general appearance and most important characteristics of each species are also included.
Keywords: Bark beetles; Ambrosia beetles; South America; Tucumán; Distribution; Forestry
Introducción
La subfamilia Scolytinae constituye un grupo grande y diverso de escarabajos barrenadores (Atkinson, 2017). Presentan una amplia gama de modos de alimentación, pero se dividen principalmente en 2 grupos: los escarabajos descortezadores y los de ambrosía. Los primeros se alimentan del floema de árboles enfermos o moribundos y por su actividad, la corteza termina por desprenderse. Los escarabajos de ambrosía perforan el xilema de árboles debilitados, moribundos o enfermos y cultivan hongos simbiontes, los cuales constituyen su alimento (Kirkendall et al., 2015). La subfamilia es reconocida por comprender especies de importancia económica y por poseer la función, desde el punto de vista ecológico, de regular las poblaciones vegetales con las que se asocian (Pérez-De La Cruz et al., 2016). Además, los escarabajos descortezadores son importantes, ya que fomentan la sucesión, lo que conlleva a mantener la salud forestal en muchos ecosistemas del mundo (Morris et al., 2018). Aunque la mayoría se encuentra en árboles moribundos, debilitados, enfermos o trocería recién cortada, algunas especies pueden constituir verdaderas plagas al invadir árboles sanos o sin evidencia de debilitamiento (Lombardero, 1995; Pérez-Silva et al., 2021). Su peligrosidad radica, además, en que algunas especies son vectores de hongos fitopatógenos, los cuales pueden ocasionar la muerte de la planta o producir daños que alteren la calidad de la madera provocando pérdidas económicas importantes (Lombardero, 1995). Además, por la naturaleza críptica de las galerías, son difíciles de detectar y esto conlleva a que muchas especies se hayan establecido en otras áreas fuera de su rango de distribución, estableciéndose como especies invasoras, planteando graves amenazas a los bosques, productos forestales y cultivos (Kirkendall, 2018).
Hasta el año 2018 en Argentina y, particularmente en la provincia de Tucumán, gran parte de los estudios sobre Scolytinae corresponden a trabajos dispersos en la literatura (Bruch, 1914; Bosq, 1943; Hayward, 1960; Santoro, 1966; Viana, 1964; Wood, 2007). Hasta la fecha se han descrito unas 6,400 especies en todo el mundo (Hulcr et al., 2015; Wood y Bright, 1992). Para Argentina, Atkinson (2025) lista 17 tribus, 52 géneros y 199 especies, de las cuales 18 son introducidas en el país desde otros continentes. Para la provincia de Tucumán, se han reportado 56 especies distribuidas en 12 tribus y 26 géneros (Córdoba et al., 2025).
Hasta el momento, no se han desarrollado claves para la identificación de tribus y especies en Argentina, lo cual limita la capacidad de diagnóstico y manejo de estos insectos. El presente trabajo constituye la primera iniciativa dirigida a la elaboración de claves ilustradas con figuras, que permitan la determinación precisa de las tribus y especies presentes en el país. Estas herramientas son esenciales, ya que algunas especies tienen un impacto significativo en cultivos forestales, ornamentales y frutales, que afectan tanto la economía nacional como la biodiversidad regional. En un contexto de cambio climático y globalización, la identificación temprana y precisa de estas especies resulta esencial para prevenir posibles brotes. La ausencia de herramientas específicas adaptadas a las condiciones locales hace que este trabajo sea aún más relevante al proporcionar un recurso indispensable para investigadores, técnicos y productores.
Materiales y métodos
Gran parte del material estudiado fue obtenido de recolectas directas e indirectas, realizadas desde el 2016 al 2024, en la provincia de Tucumán, noroeste de Argentina. Las recolectas indirectas se realizaron utilizando trampas elaboradas con botellas plásticas y con etanol 96% como atrayente. Los ejemplares fueron separados y determinados siguiendo las claves de Wood (2007), así como por comparación con los ejemplares de distintas colecciones y la revisión por parte del segundo autor de los especímenes del Smithsonian National Museum of Natural History (USNM), Washington, DC (EE.UU.) y el Naturhistorisches Museum Wien (NHMW), Viena, Austria.
La elaboración de las claves se realizó con base en las descripciones de Wood (2007) y en la revisión de los ejemplares de las colecciones de la Fundación Miguel Lillo (I-FML), Museo de La Plata (MLP) y Museo Argentino de Ciencias Naturales Bernardino Rivadavia (MACN). En las claves fueron incluidos mayormente caracteres de las hembras, sin embargo, en algunos casos se analizaron los caracteres del macho, por lo que se aclara con (Macho), al inicio de cada llave. Las especies marcadas con un asterisco (*) son especies exóticas. La distribución de las especies en el país se realizó con base en la información obtenida de las colecciones revisadas, la literatura existente, datos de las recolectas y en la información presente en el sitio web Bark and Ambrosia Beetles of the Americas (Atkinson, 2025). Las claves incluyen especies que se distribuyen en otras provincias de Argentina, por lo que pueden ser utilizadas en otras regiones del país.
Las fotografías fueron tomadas con una cámara Leica DMC 2900 incorporada a un microscopio estereoscópico Leica M205 C, para cada foto se tomó una serie de capas a través del Software Leica Application Suite Core versión 4.7.1.
Resultados
Se identificaron 56 especies pertenecientes a 25 géneros y 12 tribus: Bothrosternini, Corthylini, Dryocoetini, Hexacolini, Hylurgini, Ipini, Micracidini, Phloeosinini, Phloeotribini, Scolytini, Trypophloeini y Xyleborini. La tribu más diversa fue Xileborini, con 14 especies, seguida de Bothrosternini, con 12 especies.
Los géneros históricamente incluidos dentro de Cryphalini fueron agrupados de acuerdo con la propuesta de Johnson et al. (2020), Hypothenemus Westwood, 1836 se incluye dentro de la tribu Trypophloeini, y Acorthylus y Cryptocarenus se incluyen dentro de la tribu Corthylini (subtribu Pityophthorina). Además, se incluyen tanto a Xyleborus bispinatus Eichhoff, 1868 como a X. ferrugineus (Fabricius, 1801) como 2 especies distintas de acuerdo con Kirkendall y Jordal (2006). Theoborus theobromae (Hopkins,1915) se trata como Coptoborus villosulus (Blandford, 1898), de acuerdo con Smith y Cognato (2021).
La clave para tribus es una clave simplificada que no se puede utilizar fuera del área de estudio, en gran parte porque omite grupos no presentes en el noroeste de Argentina. Las claves para tribus y géneros de Wood (1982, 2007) no permiten ubicar todos los géneros en tribus con certeza. En particular, los géneros Acorthylus y Cryptocarenus fueron tratados por Wood (1982, 2007) en su tribu Cryphalini, pero autores más recientes como Johnson et al. (2020) los han incluido en la tribu Corthylini (subtribu Pityophthorina). En esta clave se identifican por separado.
Clave de las tribus de Scolytinae presentes en Tucumán
1. Cabeza parcialmente cubierta por el pronoto; pronoto en vista lateral con curvatura gradual desde la base hasta el ápice (fig. 1a-d) 2
1’. Cabeza completamente cubierta por el borde anterior del pronoto (mejor visto en aspecto lateral); pronoto en vista lateral generalmente con un cambio abrupto en armadura o contextura (fig. 1e- h) 7
2. Protibia sin dentículos laterales, con gancho apical en borde exterior (fig. 2a) Scolytini
2’. Protibia con dentículos laterales, proyecciones apicales pueden estar presentes en borde interior (fig. 2b-d) 3
3. Protibia con 1 proyección subapical en borde exterior, consistiendo en 2 dentículos prominentes (fig. 2b) Bothrosternini
3’. Protibia sin proyección subapical en borde exterior (fig. 2c, d) 4
4. Maza antenal con segmentos, independientemente móviles (fig. 1c, d) Phloeotribini
4’. Maza antenal con segmentos fusionados o sin segmentación (fig. 2f-n) 5
5. Funículo se une a la maza antenal en el centro de la base del mismo (fig. 2f) Hylurgini
5’. Funículo se une a la maza antenal lateralmente (fig. 2g, h) Phloeosinini
6. Perfil lateral del pronoto curvado, cima poco desarrollada (fig. 1e, f) 7
6’. Perfil lateral del pronoto con cima pronunciada y abrupta (fig. 1g, h) 8
7. Protibia con 2 dentículos prominentes ubicados en el ápice (fig. 2e); funículo antenal con 7 segmentos Hexacolini
7’. Protibia con dentículos abundantes, similares en tamaño (fig. 2a, b), funículo antenal con 5 segmentos Dryocoetini
8. Parte terminal del dorso del último segmento abdominal parcialmente visible en vista ventral (abdomen parece tener 6 segmentos en vista ventral) (fig. 1j) Corthylini (Corthylini, Pityophthorini en parte)
8’. Parte terminal del dorso del último segmento abdominal parcialmente no visible en vista ventral (abdomen parece tener 5 segmentos en vista ventral) (fig. 1i) 9
9. Zona posterior de la cavidad oral deprimida debajo del nivel de la cabeza en vista ventral (fig. 1k) Xyleborini
9’. Zona posterior de la cavidad oral no deprimidas (fig. 1l) 10
10. Suturas de maza antenal similares en caras anterior y posterior (fig. 2k, l) 11
10’. Suturas de maza antenal conspicuamente desplazadas en cara posterior (oblicuamente truncada) (fig. 2m, n) 13
11. Segundo segmento del flagelo antenal tan largo como segmentos 3 y 5 juntos (fig. 2i) Acorthylus (Corthylini: Pityopthorina
11’. Segundo segmento del flagelo antenal igual de largo como segmentos 3 y 5 12
12’. Vestidura de las interestrías del disco elitral escasa o ausente, setas en forma de cuchara (fig. 2o) Cryptocarenus (Corthylini: Pityopthorina)
12’. Vestidura de las interestrías abundante desde la base del disco hasta el ápice del declive; setas en forma de cinta, truncadas en su ápice (fig. 2p) Trypophloeini
13. Funículo antenal con 6 segmentos (fig. 2j) Micracidini
13’. Funículo antenal con 5 segmentos Ipini
Tribu Bothrosternini Blandford, 1896
Presentan dimorfismo sexual en la frente, los ojos son enteros, el funículo antenal lleva 6 segmentos, la maza antenal es moderadamente aplanada y con suturas bien marcadas, las procoxas están moderadamente o ampliamente separadas, el pronoto carece de armaduras o lleva pocas ornamentaciones, las protibias presentan un proceso bífido en el ángulo apical externo que excede el ángulo apical interno, la base de los márgenes de los élitros generalmente llevan una fila de crenulaciones poco desarrolladas, representada en algunas especies, por una costa continua. Son monógamos, con excepción del género Bothrosternus, donde ocurre algún tipo de partenogénesis. La mayoría de las especies son barrenadoras de la médula de ramas pequeñas, con excepción de Pagiocerus que barrena semillas y Bothrosternus que también barrena ramitas, pero aparentemente es xylomicetófago. Esta tribu se restringe a zonas tropicales de América, solo una especie se extiende hasta el sureste de EUA (Wood, 2007).
Clave de las especies de la tribu Bothrosternini
1. Cuerpo alargado y delgado (fig. 3a, c); vestidura que incluye setas o escamas; suturas de la maza antenal rectas y transversales (fig. 3e); ancho del rostro mayor que distancia entre los ojos; pronoto longitudinalmente estriado y con puntos; principalmente barrenadores de ramas y tallos delgados 2
1’. Cuerpo ovalado y robusto (fig. 3b, d); vestidura compuesta de setas; suturas de maza antenal fuertemente procurvadas (fig. 3f); ancho del ápice del rostro igual a distancia entre los ojos; pronoto con puntuación bien marcada; barrenadores de semillas Pagiocerus frontalis (Fabricius)
2. Presencia de crenulaciones en las zonas anterolaterales del pronoto; pronoto casi tan ancho como largo; ancho del ápice del epistoma mayor que distancia entre los ojos 3
2’. Superficie de pronoto lisa; pronoto más largo que ancho (fig. 4b); ancho del ápice del epistoma igual a distancia entre ojos Cnesinus dividuus Schedl
3. Vestidura compuesta por escamas y setas grisáceas (fig. 4a, c); lados del pronoto paralelos (fig. 5a); frente con abundante pubescencia, compuesta de setas blanquecinas, apretadas contra el fondo y dirigidas hacia el centro (fig. 4e) Cnesinus squamifer Wood
3’. Vestidura compuesta de setas amarillentas (fig. 4b, d); lados del pronoto convexos (fig. 4b); frente con escasa pubescencia, setas amarillentas, semierectas y dirigidas hacia el centro (fig. 4f) Cnesinus hispidus Eggers
Pagiocerus frontalis (Fabricius, 1801) (fig. 3b, d, f)
Distribución. Argentina: S/D, Tucumán; América del Sur: Bolivia, Brasil, Chile, Colombia, Ecuador, Guyana Francesa, Paraguay, Perú, Trinidad y Tobago y Venezuela (Atkinson, 2025; Córdoba y Atkinson, 2018; Córdoba et al., 2021, 2023, 2025; Smith et al., 2017; Wood, 2007).
Comentarios. Costilla y Coronel (1994) citan a esta especie como Pagiocerus fiorii Eggers sin especificar ninguna ubicación. Está extensamente distribuida en regiones tropicales de América.
Cnesinus dividuus Schedl, 1938 (fig. 3a, c, e)
Distribución. Argentina: Buenos Aires, Tucumán; América del Sur: Brasil (Atkinson, 2025; Córdoba et al., 2025; Wood, 2007).
Cnesinus squamifer Wood, 2007 (fig. 4a, c, e)
Distribución. Argentina: Tucumán (Atkinson, 2025; Córdoba et al., 2023; Wood, 2007).
Cnesinus hispidus Eggers, 1943 (fig. 4b, d, f)
Distribución. Argentina: Tucumán; América del Sur: Bolivia y Brasil (Atkinson, 2025; Córdoba et al., 2021, 2023, 2025; Wood, 2007).
Tribu Corthylini LeConte, 1876
Por lo general machos y hembras similares en tamaño. Presentan un surco en el extremo anterior del metapisternon que conforma un mecanismo de bloqueo que mantiene los élitros en su lugar cuando están en reposo. La maza antenal es aplanada, con las suturas similares en ambos lados de la misma y los de la cara posterior no están fuertemente desplazados hacia el ápice. Las tibias son delgadas y llevan pocos dentículos en el margen lateral. Esta tribu se divide en 2 subtribus: Corthylina y Pityophthorina (Wood, 2007).

Figura 1. a, Vista lateral de cabeza y pronoto de Scolytopsis toba;b, vista dorsal de cabeza y pronoto de S. toba; c, vista lateral de cabeza y pronoto de Phloeotribus harringtoni; d, vista dorsal de cabeza y pronoto de P. harringtoni; e, vista lateral de cabeza y pronoto de Scolytodes tucumani; f, vista dorsal de cabeza y pronoto de S. tucumani; g, vista lateral de cabeza y pronoto de Orthotomicus laricis; h, vista dorsal de cabeza y pronoto de O. laricis; i, vista ventral del abdomen de Xyleborus volvulus; j, vista ventral del abdomen de Araptus sp.; k, vista ventral de partes bucales de Xylosandrus crassiusculus; l, vista ventral de partes bucales de Araptus pubescens.

Figura 2. a, Protibia de Scolytopsis puncticollis; b, protibia de Pagiocerus frontalis; c, protibia de Coccotrypes carpophagus; d, protibia de Orthotomicus laricis; e, protibia de Scolytodes tucumani; f, antena de Xylechinus imperialis; g, antena de Chramesus argentiniae; h, antena de Pseudochramesus acuteclavatus; i, antena de Acorthylus bosqui; j, antena de Hylocurus giganteus; k, vista de cara anterior de la antena de Gnathotrichus sulcatus; l, vista de cara posterior de la antena de G. sulcatus; m, vista de cara anterior de la antena de Xyleborus volvulus; n, vista de cara posterior de la antena de X. volvulus; o, disco y declive elitral de Cryptocarenus seriatus; p: disco y declive elitral de Hypothenemus crudiae.

Figura 3. a: Vista dorsal de Cnesinus dividuus (tomada de Atkinson, 2025); b, vista dorsal de Pagiocerus frontalis (tomada de Atkinson, 2025); c, vista lateral de C. dividuus (tomada de Atkinson, 2025); d, vista lateral de P. frontalis (tomada de Atkinson, 2025); e, antena de C. dividuus;f, antena de P. frontalis.
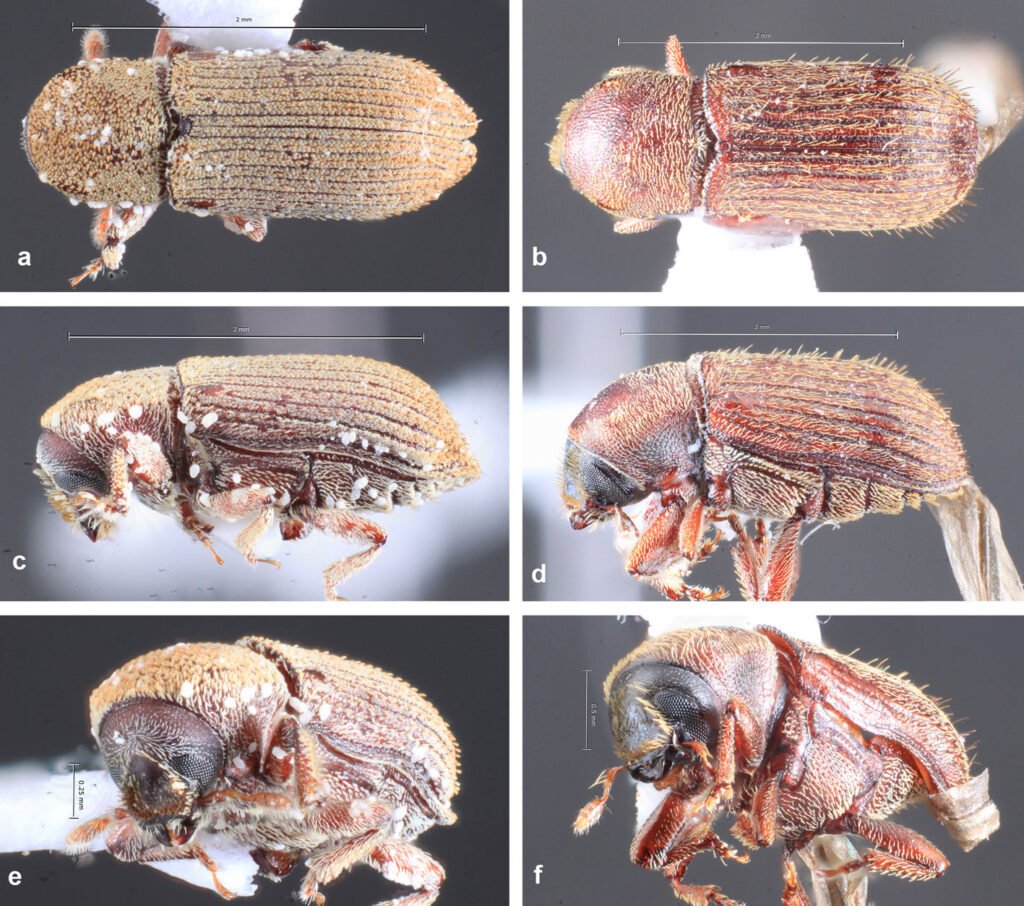
Figura 4. a, Vista dorsal de Cnesinus squamifer (tomada de Atkinson, 2025); b, vista dorsal de C. hispidus (tomada de Atkinson, 2025); c, vista lateral de C. squamifer (tomada de Atkinson, 2025); d, vista lateral de C. hispidus (tomada de Atkinson, 2025); e, vista frontal de C. squamifer (tomada de Atkinson, 2025); f, vista frontal de C. hispidus (tomada de Atkinson, 2025).
Subtribu Corthylina LeConte, 1876
Funículo antenal con 1-5 segmentos, maza grande y generalmente asimétrica; pieza intercoxal prosternal ausente, pubescencia comúnmente muy reducida, es insignificante muy confusa (no ordenada en filas); el declive elitral es convexo o truncado a profundamente excavado, generalmente con procesos similares a espinas. La mayoría de las especies perforan los tejidos del xilema del huésped e inoculan esporas de sus hongos simbióticos en las paredes del túnel, luego se alimentan principalmente de las esporas del hongo y el micelio (Wood, 2007).
Clave de las especies de la subtribu Corthylina
1. Funículo antenal de 2 segmentos; masa antenal truncada apicalmente, ovalada o redonda 2
1’. Funículo antenal de 1 segmento; masa antenal ovalada o redonda 3
2. Cuerpo castaño con 3 manchas más claras y rojizas en base del pronoto y 2 manchas alargadas longitudinales amarillentas en élitros, van desde la base hasta antes del declive elitral (fig. 5a, c); pronoto 1.5 veces más largo que ancho, borde anterior del pronoto armado con dientes; declive elitral amplio, moderadamente cóncavo, espina 1 en interestría 1 diminuta y puntiaguda, 2 en interestría 2, ligeramente más grandes que 1, espina 3 diminuta, espina 4 ligeramente más grandes que 2, puntiagudas (fig. 5e Monarthrum chapuisi Kirsch
2’. Cuerpo castaño rojizo muy oscuro y homogéneo (fig. 5b, d); pronoto 1.3 veces más largo que ancho, borde anterior del pronoto liso (sin dientes); declive elitral empinado, reticulado, estrecho y suavemente impreso, con espinas 2 y 3 diminutas (fig. 5f Monarthrum subimpressum Wood
3. Maza antenal 1.5 veces más larga que ancha, con sutura visible y cirro delgado (fig. 6e); frente fuertemente cóncava, mitad inferior amarillenta y esponjosa, sin setas (fig. 6g); margen anterior del pronoto débilmente aserrado; declive elitral muy empinado, redondeado y convexo, con setas erectas largas difusas (fig. 6c) Corthylus alineus Schedl
3’. Maza antenal 1.3 veces más larga que ancha, con 3 suturas visibles y cirro muy largo (fig. 6f); frente moderadamente cóncava, con áreas laterales a ambos lados de la frente, amarillas y esponjosas, con setas largas y erectas a ambos lados del área esponjosa (fig. 6h); borde apical de la frente con fila de setas plumosas orientadas hacia el centro de la frente; margen anterior del pronoto con espinas; declive elitral muy empinado (casi truncado) débilmente convexo, con cresta costal elevada no cerrada, con escasas setas largas y erectas (fig. 6d) Corthylus serrulatus Eggers
Monarthrum chapuisi Kirsch, 1866 (fig. 3a, c, e)
Distribución. Argentina: Tucumán; América del Sur: Bolivia, Colombia, Perú y Venezuela (Atkinson, 2025; Córdoba et al., 2023, 2025; Smith et al., 2017; Wood, 2007).
Monarthrum subimpressum Wood, 2007 (fig. 5b, d, f)
Distribución. Argentina: Salta, Tucumán (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Corthylus alineus Schedl, 1966 (fig. 6a, c, e, g)
Distribución. Argentina: Salta y Tucumán; América del Sur: Colombia, Ecuador y Perú (Atkinson, 2025; Córdoba y Atkinson, 2018; Córdoba et al., 2023, 2025; Smith et al., 2017; Wood, 2007).
Corthylus serrulatus Eggers, 1934 (fig. 6b, d, f, h)
Distribución. Argentina: Jujuy, Salta y Tucumán; América del Sur: Bolivia, Brasil y Perú (Atkinson, 2025; Córdoba et al., 2018, 2021, 2023, 2025; Smith et al., 2017; Wood, 2007).
Subtribu Pityophthorina Eichhoff, 1878
Se caracteriza por presentar el funículo antenal mayormente de 5 segmentos, maza antenal más pequeña y simétrica; pieza intercoxal prosternal agudamente puntiaguda; pubescencia abundante, generalmente en filas en los élitros; declive elitral comúnmente convexo a bisulcado, armadura ausente. Se alimentan directamente del tejido de la planta huésped y son floeófagas, mielófagas o espermófagas. No hay especies verdaderamente xilófagas (Wood, 2007).
Clave de las especies de la subtribu Pityophthorina
1. Revestimiento del cuerpo formado por escamas (fig. 7a, b); flagelo antenal con 2 segmentos; maza antenal alargada y subrectangular (fig. 7c); pronoto con 8 filas transversales de espinas romas; ramillete de setas largas en cara interna de protibias, que van desde la base hasta el ápice de las mismas (fig. 7e); menos de 2 mm de longitud del cuerpo Acorthylus bosqui (Schedl)
1’. Revestimiento del cuerpo formado por setas; flagelo antenal con 4 segmentos; maza antenal redondeada y aplanada (fig. 7d); pronoto con espinas romas o sin espinas; tibias anteriores con pubescencia abundante (fig. 7f); más de 2 mm de longitud del cuerpo 2
2. Pronoto con rugosidades pronunciadas en la parte anterior; pronoto en vista lateral, convexo hasta el disco, luego con una elevación pronunciada en medio, más bajo y recto hasta la base; maza antenal con 2 suturas parcial o totalmente septadas 3
2’. Pronoto sin rugosidades pronunciadas en la parte anterior; pronoto en vista lateral con curvatura uniforme desde el ápice hasta la base, sin elevación pronunciada; maza antenal con 1 sutura total o parcialmente septada 5
3. Declive elitral con sulcos, interestría 1 moderadamente elevada, armada por 10 o más tubérculos; pubescencia de los élitros confinada al declive (fig. 9e) Pityophthorus tucumanensis Wood
3’. Declive elitral completamente convexo, sin sulcos, interestría 1 sin tubérculos 4
4. Longitud del cuerpo 1.4 a 1.8 mm; frente con fuerte impresión transversal y con pequeño tubérculo medio a nivel de los ojos (fig. 8e); color del cuerpo castaño oscuro (fig. 8a, c) Cryptocarenus heveae (Hagedorn)
4’. Longitud del cuerpo 1.4 a 1.5 mm; frente cóncava (fig. 8f); coloración del cuerpo castaño rojizo o claro (fig. 8b, d) Cryptocarenus seriatus Eggers
5. Pronoto de lados paralelos; élitros 2 veces más largos que el pronoto (fig. 9b, d) Araptus araujiae (Brèthes)
5’. Pronoto de lados convexos; élitros entre 1.6 y 1.7 más largos que el pronoto 6
6. Frente con quilla media aguda, más fuertemente elevada en mitad media superior (fig. 10g); maza antenal redondeada; pubescencia del cuerpo abundante (fig. 10a,d) Araptus pubescens (Schedl)
6’. Frente sin quilla; maza antenal ovalada; pubescencia no muy abundante 7
7. Frente muy débilmente convexa, con pubescencia corta y escasa (fig. 10h); declive elitral convexo y bisulcado (fig. 10j) Araptus frenatus (Schedl)
7’. Frente claramente convexa, con pubescencia larga abundante y erecta; con tubérculo en el ápice de la frente, poco marcado que se afina hasta la base (fig. 10i); declive elitral convexo con surco poco profundo en las interestrías 1 y 2 (fig. 10k) Araptus volastos (Schedl)

Figura 5. a, Vista dorsal de Monarthrum chapuisi (tomada de Atkinson, 2025); b, vista dorsal de M. subimpresum (tomada de Atkinson, 2025); c, vista lateral de M. chapuisi (tomada de Atkinson, 2025); d, vista lateral de M. subimpresum (tomada de Atkinson, 2025); e, vista posterior de M. chapuisi; f, vista posterior de M. subimpresum (tomada de Atkinson, 2025).

Figura 6. a, Vista dorsal de Corthylus alineus;b, vista dorsal de C. serrulatus (tomada de Atkinson, 2025); c, vista lateral de C. alineus; d, vista lateral de C. serrulatus (tomada de Atkinson, 2025); e, antena de C. alineus; f, antena de C. serrulatus; g, vista frontal de C. alineus; h, vista frontal de C. serrulatus.
Acorthylus bosqui (Schedl, 1938) (fig. 7a, b, c, e)
Distribución. Argentina: Jujuy y Tucumán; América del Sur: Bolivia (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Cryptocarenus heveae (Hagedorn, 1912) (fig. 7d, f, 8a, c, e)
Distribución. Argentina: Buenos Aires, Misiones, Santiago del Estero y Tucumán; América del Sur: Brasil, Colombia Perú, Trinidad y Tobago y Venezuela (Atkinson, 2025; Córdoba et al., 2021, 2023, 2025; Iturre y Darchuck, 1996; Smith et al., 2017; Wood, 2007).
Cryptocarenus seriatus Eggers, 1933 (fig. 8b, d, f)
Distribución. Argentina: Tucumán; América del Sur: Bolivia, Brasil, Colombia, Guyana Francesa, Paraguay, Perú y Venezuela (Atkinson 2025; Córdoba et al., 2023, 2025; Smith et al., 2017; Wood, 2007).
Pityophthorus tucumanensis Wood, 2007 (fig. 9a, c, e)
Distribución. Argentina: Tucumán (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Araptus araujiae (Brèthes, 1921) (fig. 9b, d)
Distribución. Argentina: Buenos Aires y Tucumán (Atkinson, 2025; Bachmann y Lanteri, 2013; Córdoba et al., 2023, 2025; Wood y Bright, 1992).
Araptus pubescens (Schedl, 1950) (fig. 10a, d, g)
Distribución. Argentina: Córdoba y Tucumán (Atkinson, 2025; Córdoba et al., 2025; Wood, 2007).
Araptus frenatus (Schedl, 1939) (fig. 10b, e, h, j)
Distribución. Argentina: Córdoba y Tucumán (Atkinson, 2025; Córdoba et al., 2025; Wood, 2007).
Araptus volastos (Schedl, 1938) (fig. 10c, f, i, k)
Distribución. Argentina: Jujuy, Salta y Tucumán; América del Sur: Bolivia (Atkinson, 2025; Córdoba et al., 2025; Wood, 2007).
Tribu Dryocoetini Lindemann, 1877

Figura 7. a, Vista dorsal de Acorthylus bosqui (tomada de Atkinson, 2025); b, vista lateral de A. bosqui (tomada de Atkinson, 2025); c, antena de A. bosqui; d, antena de Cryptocarenus heveae; e, tibia de A. bosqui; f, tibia de C. heveae (tomada de Atkinson, 2025).

Figura 8. a, Vista dorsal de Cryptocarenus heveae (tomada de Atkinson, 2025); b, vista dorsal de C. seriatus (tomada de Atkinson, 2025); c, vista lateral de C. heveae (tomada de Atkinson, 2025); d, vista lateral de C. seriatus (tomada de Atkinson, 2025); e, vista frontal de C. heveae (tomada de Atkinson, 2025); f, vista frontal de C. seriatus
Presentan dimorfismo sexual en la frente. En los machos es convexa a variadamente impresa y en las hembras es convexa a aplanada o con elevaciones; el ojo está emarginado o dividido; el escapo antenal es alargado, el funículo está compuesto de 4 a 6 segmentos, la maza antenal puede estar oblicuamente truncada o conspicuamente aplanada, en este último caso las suturas son procurvadas u obsoletas; el pronoto puede estar o no armado con asperezas; las procoxas pueden ser contiguas o estar muy poco separadas; margen lateral de las protibias con 3 o más dentículos alveolares; el declive elitral puede ser convexo, sulcado, aplanado y, a veces, con pequeños gránulos; la pubescencia está compuesta por setas; la mayoría de las especies son polígamas y algunas son haploides; hay especies espermatófagas, mielófagas y floeófagas. De los 17 géneros que se conocen en el mundo, solo 4 se encuentran en América del Sur, pero 2 de ellos son introducidos (Wood, 2007). Las especies del género Coccotrypes presentes en la región son barrenadores de semillas de palmeras.
Clave de las especies de la tribu Dryocoetini
1. Tamaño del cuerpo entre 1.8 a 2.3 mm; pubescencia moderadamente abundante (fig. 11a, c); pronoto de lados marcadamente convexos que se angosta de manera abrupta hacia el ápice, con asperezas pequeñas y abundantes (fig. 11a) Coccotrypes dactyliperda (Fabricius)
1’. Tamaño del cuerpo entre 1.5 y 1.9 mm; pubescencia muy abundante (fig. 11b, d); pronoto redondeado, angostado en el ápice, con asperezas gruesas y marcadas (fig. 11b) Coccotrypes carpophagus (Hornung)
Coccotrypes dactyliperda (Fabricius, 1801)* (fig. 11a, c)
Distribución. S/D, Tucumán (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood y Bright, 1992).
Coccotrypes carpophagus (Hornung, 1842)* (fig. 11b, d)
Distribución. Tucumán (Atkinson, 2025; Córdoba et al., 2023, 2025).
Tribu Hexacolini Eichhoff, 1878
Sus miembros presentan dimorfismo sexual: los machos pueden presentar una impresión en la frente, a veces oscura; los machos son convexos y las hembras son esculpidas y ornamentadas de forma variada; los ojos son en general alargados, con su margen anterior entero o sinuoso; el escapo antenal es alargado; el funículo lleva 5 o 6 segmentos (con 7 segmentos en Gymnochilus); la maza antenal puede o no llevar suturas; la zona apical del pronoto puede estar ornamentada o no; las procoxas están ampliamente separadas; las protibias llevan, en el margen lateral, 1 o más dentículos alveolares generalmente incrustados en la cutícula (Wood, 2007).
Clave de las especies de la tribu Hexacolini
1. Color castaño amarillento, con franja más oscura en mitad apical del pronoto (fig. 12a, c); frente con callo transversal por debajo del nivel superior de ojos (fig. 12e); pronoto con superficie reticulada; élitros de lados convexos (fig. 12a); declive elitral ampliamente convexo (fig.12c) Scolytodes sparsepilosus Wood
1’. Color castaño amarillento, con mitad apical más oscura (fig. 12b, d); frente con callo medio estrecho que se extiende dorsalmente desde elevación epistomal hasta ligeramente por encima del nivel de inserción de antena (fig. 12f); pronoto liso y brillante; élitros de lados paralelos (fig. 12b); declive estrechamente convexo (fig. 12d) Scolytodes tucumani Wood
Scolytodes sparsepilosus Wood, 2007 (fig. 12a, c, e)
Distribución. Argentina: Tucumán (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Scolytodes tucumani Wood, 2007 (fig. 12b, d, f)
Distribución. Argentina: Tucumán; América del Sur: Ecuador (Atkinson, 2025; Córdoba et al., 2023, 2025; Jordal y Smith, 2020; Wood, 2007).
Tribu Hylurgini Gistel, 1848
Presentan dimorfismo sexual en la frente, siendo convexa en las hembras e impresa en los machos; los ojos son enteros y ovalados; las antenas presentan un escapo alargado, el funículo con 5 a 7 segmentos y la maza antenal es simétrica, aplanada y generalmente con 3 o 4 suturas; el pronoto es generalmente liso; las procoxas son contiguas o están muy poco separadas; las tibias están armadas por dientes en los márgenes laterales y apicales; todas las especies de esta tribu son monógamas y fleófagas (Wood, 2007).

Figura 9. a, Vista dorsal de Pityophthorus tucumanensis (tomada de Atkinson, 2025); b, vista dorsal de Araptus araujiae; c, vista lateral de P. tucumanensis (tomada de Atkinson, 2025); d, vista lateral de A. araujiae; e, vista posterior de P. tucumanensis (tomada de Atkinson, 2025).
Clave de las especies de la tribu Hylurgini
Longitud 2.1-2.6 mm; color castaño oscuro, con pubescencia formada por setas y escamas con patrón de coloración mezclada (fig. 13a, b); frente convexa, reticulada y rugosa por encima de los ojos y lisa y brillante por debajo de ellos (fig. 13c); pronoto 0.85 veces más largo que ancho, base más ancha que el ápice, lados convexos, con superficie reticulada (fig. 13a); interestrías de élitros armadas por tubérculos; en macho las interestrías 3 y base de la 1 elevadas y armadas por dentículos en declive elitral Xylechinus imperialis (Schedl)
Xylechinus imperialis (Schedl, 1958) (fig. 13a-c)
Distribución. Argentina: Buenos Aires, Jujuy, Salta, Santa Fe y Tucumán (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Tribu Ipini Bedel, 1888
Se distinguen por presentar dimorfismo sexual en la frente, siendo convexa en los machos y de forma variada en las hembras; la antena presenta un escapo afinado y alargado, el funículo antenal está formado por 5 segmentos y la maza puede ser oblicuamente truncada o aplanada, con suturas desplazadas hacia el ápice de la cara posterior; mitad anterior del ápice del pronoto es declivado y áspero; las procoxas son contiguas; protibias presentan 3 o 4 dientes; el declive elitral es sulcado o profundamente excavado, puede estar armado con espinas o tubérculos; el cuerpo presenta una pubescencia similar a setas. Todas las especies de esta tribu son floeófagas y monógamas o polígamas (Wood, 2007).

Figura 10. a, Vista dorsal de Araptus pubescens (tomada de Atkinson, 2025); b, vista dorsal de A. frenatus (tomada de Atkinson, 2025); c, vista dorsal de A. volastos (tomada de Atkinson, 2025); d, vista lateral de A. pubescens (tomada de Atkinson, 2025); e, vista lateral de A. frenatus (tomada de Atkinson, 2025); f: vista lateral de A. volastos (tomada de Atkinson, 2025); g: vista frontal de A.pubescens; h, vista frontal de A. frenatus (tomada de Atkinson, 2025); i, vista frontal de A. volastos; j, vista posterior de A. frenatus (tomada de Atkinson, 2025); k, vista posterior de A. volastos (tomada de Atkinson, 2025).

Figura 11. a, Vista dorsal de Coccotrypes dactyliperda (tomada de Atkinson, 2025); b, vista dorsal de C. carpophagus (tomada de Atkinson, 2025); c, vista lateral de C. dactyliperda (tomada de Atkinson, 2025); d, vista lateral de C. carpophagus (tomada de Atkinson, 2025).

Figura 12. a, Vista dorsal de Scolytodes sparsepilosus (tomada de Atkinson, 2025); b, vista dorsal de S. tucumani (tomada de Atkinson, 2025); c, vista lateral de S. sparsepilosus (tomada de Atkinson, 2025); d, vista lateral de S. tucumani (tomada de Atkinson, 2025); e, vista frontal de S. sparsepilosus (tomada de Atkinson, 2025); f, vista frontal de S. tucumani (tomada de Atkinson, 2025).
Clave de las especies de la tribu Ipini
(Macho) Longitud: 3.0-3.7 mm; 2.7 veces más largo que ancho (fig. 14a, b); frente levemente convexa con abundante pubescencia larga, fina y erecta; pronoto 1,07 veces más largo que ancho, mitad anterior moderadamente declinada y mitad basal levemente cóncava, con pubescencia escasa en el centro y con setas largas y erectas en los bordes y ápice (fig. 14b); declive elitral cóncavo, con 3 espinas en bordes externos, 1 espina en interestría 1 y otra en la interestría 2 (fig. 14c) Orthotomicus laricis (Fabricius)
Orthotomicus laricis (Fabricius, 1792)* (fig. 14a, b, c)
Distribución. Argentina: Neuquén y Tucumán; América del Sur: Chile (Atkinson, 2025; Córdoba et al., 2021, 2023, 2025; Kirkendall, 2018; Wood, 2007).
Tribu Micracidini LeConte, 1876
Se distinguen por presentar dimorfismo sexual en la frente, siendo en la hembra generalmente cóncava y en el macho, raramente cóncava; los ojos pueden ser ovalados, alargados, enteros o sinuados; antenas con el escapo corto o alargado, aplanado o expandido, con setas, el funículo presenta 6 segmentos, la maza antenal puede o no tener suturas; el pronoto presenta asperezas en la zona anterior, los lados son redondeados; las procoxas están ligeramente separadas; generalmente presentan setas subplumosas en alguna parte del cuerpo; pueden tener hábitos xilófagos, floeófagos o mielófagos; todos son bígamos excepto el género Micraciella que es monógamo (Wood, 2007).
Clave de las especies de la tribu Micracidini
(Macho) Longitud 3.2 a 3.5 mm; 2.8 veces más largo que ancho; frente convexa con carena transversal (fig. 15c); antena con escapo ligeramente aplanado con mechón de pelos (fig. 15c), sutura procurvada; mitad apical del pronoto con tubérculos que van disminuyendo hacia la mitad, margen apical con 6 dientes; declive elitral convexo con nódulos en las interestrías de la base, interestría 9 con quilla, pubescencia escasa, aumenta en el declive elitral, élitros terminados en punta aguda (fig. 15d) Hylocurus giganteus (Schedl)
Hylocurus giganteus (Schedl, 1950) (fig. 15a-d)
Distribución. Argentina: Salta y Tucumán; América del Sur: Brasil (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Tribu Phloeosinini Nüsslin, 1912
Presentan dimorfismo sexual en la frente, machos con diferentes impresiones y hembras con frente aplanada o convexa; ojos pueden estar emarginados; antenas llevan un funículo con 5-7 segmentos, maza antenal aplanada, pueden ser asimétricas en diferentes medidas, pueden llevar suturas o no; pronoto no tiene asperezas, excepto en Dendrosinus, que presenta asperezas débiles; tercer segmento tarsal comprimido o bilobulado; escutelo puede o no ser visible; pueden ser polígamos o bígamos; pueden ser floeófagos o xilófagos (Wood, 2007).
Clave para las especies de la tribu Phloeosinini
1. Maza antenal fuertememente aplanada, en forma de riñón, la unión con el funículo es en su parte lateral, sin suturas ni fila de setas; escutelo presente pero diminuto; pronoto liso o reticulado 2
1’. Maza antenal con suturas fuertemente procurvadas y claramente marcadas por fila de setas, unión con el funículo excéntrica; escutelo visible; pronoto liso o armado con pequeños gránulos 4
2. Frente del macho con márgenes laterales fuertemente elevados y con cuentas 3
2’. Frente del macho con márgenes laterales agudamente elevados con cresta irregular pero sin cuentas (fig. 16g) Chramesus phloeotriboides Schedl
3. Margen lateral de la frente del macho fuertemente elevado y con cuentas solo en el tercio inferior (fig. 16h); maza antenal 2.6 veces más larga que ancha; pronoto con superficie lisa y brillante, zona basal con algunos tubérculos pequeños y aislados Chramesus argentinae Wood
3’. Margen lateral de la frente del macho agudamente elevado y marcado con 9 cuentas (fig. 16i); maza antenal 2.3 veces más larga que ancha; pronoto con zona basal profundamente punteada Chramesus globosus Hagedorn
4. Frente ampliamente convexa; estrías de los élitros claramente impresas o no impresas con punciones regulares 5
4’. Frente ancha y ligeramente cóncava (fig. 17g); estrías de los élitros impresas con punciones bastantes grandes; interestría 7 elevada en los machos Pseudochramesus costulatus Blackman
5. Interestrías con escamas de fondo castañas oscuras y pálidas, formando un patrón, setas pálidas uniseriadas en interestrías (fig. 17b, e); frente con elevación a nivel de inserción de antenas (fig. 17h) Pseudochramesus acuteclavatus (Hagedorn)
5’. Interestrías con escamas de fondo castañas, a lo largo de la sutura, pálidas (fig. 17c, f); frente sin elevación a nivel de la inserción de las antenas (fig. 17i) Pseudochramesus harringtoni Blackmann
Chramesus phloeotriboides Schedl, 1958 (fig. 16a, d, g)
Distribución. Argentina: Córdoba y Tucumán (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Chramesus argentinae Wood, 2007 (fig. 16b, e, h)
Distribución. Argentina: Tucumán (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Chramesus globosus Hagedorn, 1909 (fig. 16c, f, i)
Distribución. Argentina: Buenos Aires, La Rioja, Misiones, Santa Fe y Tucumán; América del Sur: Brasil y Uruguay (Atkinson, 2025; Bachmann y Lanteri, 2013; Córdoba et al., 2023, 2025; Wood, 2007).
Pseudochramesus costulatus Blackman, 1939 (fig. 17a, d, g)
Distribución. Argentina: Jujuy y Tucumán; América del Sur: Bolivia (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Pseudochramesus acuteclavatus (Hagedorn, 1909) (fig. 17b, e, h)
Distribución. Argentina: Buenos Aires, Salta y Tucumán; América del Sur: Bolivia, Brasil y Paraguay (Atkinson, 2025; Bachmann y Lanteri, 2013; Córdoba et al., 2023, 2025; Wood, 2007).
Pseudochramesus harringtoni Blackmann, 1939 (fig. 17c, f, i)
Distribución. Argentina: Salta y Tucumán; América del Sur: Bolivia y Brasil (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Tribu Phloeotribini Chapuis, 1869
Presentan dimorfismo sexual en la frente, siendo con impresiones variadas en los machos y planas o convexas en las hembras; los ojos son enteros; antenas con funículo de 5 segmentos, la maza antenal puede ser muy delgada o fuertemente asimétrica, está dividida en 3 segmentos móviles, usualmente sublamelados; las procoxas son contiguas; el pronoto puede llevar o no asperezas, los márgenes laterales son redondeados; son especies monógamas y floeófagas (Wood, 2007).

Figura 13. a, Vista dorsal de Xylechinus imperialis (tomada de Atkinson, 2025); b, vista lateral de X. imperialis (tomada de Atkinson, 2025); c, vista frontal de X. imperialis (tomada de Atkinson, 2025).

Figura 14. a, Vista dorsal de Orthotomicus laricis (tomada de Atkinson, 2025); b, vista lateral de O. laricis (tomada de Atkinson, 2025); c, vista frontal de O. laricis (tomada de Atkinson, 2025).

Figura 15. a, Vista dorsal de Hylocurus giganteus (tomada de Atkinson, 2025); b, vista lateral de H. giganteus (tomada de Atkinson, 2025); c, vista frontal de H. giganteus; d, vista posterior de H. giganteus (tomada de Atkinson, 2025).

Figura 16. a, Vista dorsal de Chramesus phloeotriboides (tomada de Atkinson, 2025); b, vista dorsal de C. argentinae (tomada de Atkinson, 2025); c, vista dorsal de C. globosus (tomada de Atkinson, 2025); d, vista lateral de C. phloeotriboides (tomada de Atkinson, 2025); e, vista lateral de C. argentinae (tomada de Atkinson, 2025); f, vista lateral de C. globosus (tomada de Atkinson, 2025); g, vista frontal de C. phloeotriboides (tomada de Atkinson, 2025); h, vista frontal de C. argentinae (tomada de Atkinson, 2025); i, vista frontal de C. globosus (tomada de Atkinson, 2025).

Figura 17. a, Vista dorsal de Pseudochramesus costulatus (tomada de Atkinson, 2025); b, vista dorsal de P. acuteclavatus (tomada de Atkinson, 2025); c, vista dorsal de P. harringtoni (tomada de Atkinson, 2025); d, vista lateral de P. costulatus (tomada de Atkinson, 2025); e, vista lateral de P. acuteclavatus (tomada de Atkinson, 2025); f, vista lateral de P. harringtoni (tomada de Atkinson, 2025); g, vista frontal de P. costulatus (tomada de Atkinson, 2025); h, vista frontal de P. acuteclavatus (tomada de Atkinson, 2025); i, vista frontal de P. harringtoni (tomada de Atkinson, 2025).
Clave para las especies de la tribu Phloeotribini
1. Frente con área cóncava; pronoto con crenulaciones en mitad apical y puntos grandes; élitros con interestrías iguales o más angostas que estrías; declive elitral con espinas 2
1’. Frente con área cóncava y carena epitosmal muy elevada en macho (fig. 18g); pronoto con asperezas en mitad apical y puntos medianos; élitros con interestrías 3 veces más anchas que estrías; declive elitral con tubérculos pequeños (fig. 18j) Phloeotribus subovatus Blandford
2. Escapo antenal con mechón grande de setas largas (fig. 18h); interestrías de igual ancho que estrías; declive elitral con tubérculos espiniformes en interestrías 2-9 (fig. 18k) Phloeotribus asperulus Eggers
2’. Escapo antenal con escasas setas (fig. 18i); interestrías más angostas que las estrías; declive elitral con espinas en las interestrías 1 a la 9 (fig. 18l) Phloeotribus harringtoni Blackman
Phloeotribus subovatus Blandford, 1897 (fig. 18a, d, g, j)
Distribución. Argentina: Jujuy, Salta y Tucumán; América del Sur: Perú y Venezuela (Atkinson, 2025; Córdoba et al., 2025; Wood, 2007).
Phloeotribus asperulus Eggers, 1943 (fig. 18b, e, h, k)
Distribución. Argentina: Tucumán; América del Sur:
Bolivia y Brasil (Atkinson, 2025; Córdoba et al., 2025; Wood y Bright, 1992).
Phloeotribus harringtoni Blackman, 1943 (fig. 18c, f, i, l)
Distribución. Argentina: Salta y Tucumán (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Tribu Scolytini Latreille, 1804

Figura 18. a, Vista dorsal de Phloeotribus subovatus (tomada de Atkinson, 2025); b, vista dorsal de P. asperulus (tomada de Atkinson, 2025); c, vista dorsal de P. harringtoni (tomada de Atkinson, 2025); d, vista lateral de P. subovatus (tomada de Atkinson, 2025); e, vista lateral de P. asperulus (tomada de Atkinson, 2025); f, vista lateral de P. harringtoni (tomada de Atkinson, 2025); g, vista frontal de P. subovatus; h, vista frontal de P. asperulus (tomada de Atkinson, 2025); i, vista frontal de P. harringtoni (tomada de Atkinson, 2025); j, vista posterior de P. subovatus (tomada de Atkinson, 2025); k, vista posterior de P. asperulus (tomada de Atkinson, 2025); l, vista posterior de P. harringtoni (tomada de Atkinson, 2025).
Protibias y, usualmente, metatibias desarmadas de espinas, solo llevan un único proceso similar a una espina curvado en el ángulo apical lateral; los márgenes laterales del pronoto son subagudos y elevados; antena con funículo de 7 segmentos, maza antenal puede presentar suturas fuertemente procurvadas, parciales u obsoletas; frente en los machos puede llevar impresiones y la de las hembras es convexa; los ojos son ovalados y enteros (Wood, 2007).
Clave para las especies de la tribu Scolytini
1. Macho. Frente ampliamente convexa, con setas finas moderadamente abundantes (fig. 19g); pronoto 1 vez más largo que ancho; estrías e interestrías confusas; abdomen gradualmente ascendente hasta los élitros (fig. 19d) Scolytus rugulosus (Müller)
1’. Macho. Frente oculta por cepillo de setas largas (fig. 19h, i); pronoto tan largo como ancho; abdomen abruptamente flexionado hacia arriba desde el margen posterior del esternito visible 2 (fig. 19e, f) 2
2. Pronoto con puntos pequeños en el disco que aumentan de tamaño hacia las zonas laterales; setas interestriales robustas y 10 veces más largas que anchas Scolytopsis toba Wichmann
2’. Pronoto con puntos medianos en el disco y con zona anterior y laterales reticulada; setas interestriales 4 veces más largas que anchas Scolytopsis punticollis Blandford
Scolytus rugulosus (Müller, 1818)* (fig. 19a, d, g)
Distribución. Buenos Aires, Catamarca, La Rioja, Mendoza y Misiones; América del Sur: Brasil, Chile, Perú y Uruguay (Atkinson, 2025; Smith et al., 2017; Córdoba y Atkinson, 2018; Córdoba et al., 2023, 2025; Wood, 2007).
Comentario. Esta especie es de origen euroasiático, pero se distribuye actualmente en todas las regiones templadas del mundo.
Scolytopsis toba Wichmann, 1914 (fig. 19b, e, h)
Distribución. Argentina: Misiones y Tucumán; América del Sur: Brasil y Paraguay (Atkinson, 2025; Córdoba et al., 2025; Petrov, 2017; Wood, 2007).
Scolytopsis punticollis Blandford, 1896 (fig. 19c, f, i)
Distribución. Argentina: Misiones y Tucumán; América del Sur: Brasil (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Tribu Trypophloeini Nüsslin, 1911
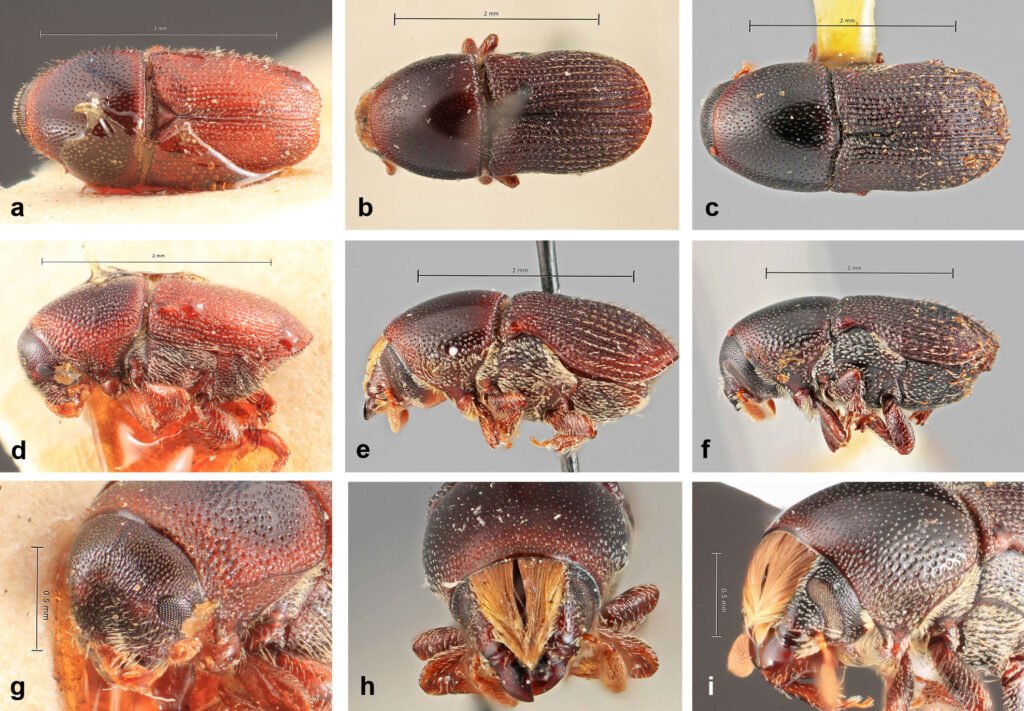
Figura 19. a, Vista dorsal de Scolytus rugulosus (tomada de Atkinson, 2025); b, vista dorsal de Scolytopsis toba (tomada de Atkinson, 2025); c, vista dorsal de S. punticollis (tomada de Atkinson, 2025); d, vista lateral de S. rugulosus (tomada de Atkinson, 2025); e, vista lateral de S. toba (tomada de Atkinson, 2025); f, vista lateral de S. punticollis (tomada de Atkinson, 2025); g, vista frontal de S. rugulosus (tomada de Atkinson, 2025); h, vista frontal de S. toba (tomada de Atkinson, 2025); i, vista frontal de S. punticollis (tomada de Atkinson, 2025).
Se diferencian por la presencia del tercer tarso de forma cilíndrica; ojos son emarginados; funículo antenal con 3-5 segmentos y maza puede presentar suturas y un único septo parcial; pubescencia del hipomeron está compuesta de setas simples raramente mezclado con setas bifurcadas; setas de interestrías similares a escamas; macho similar a la hembra, de tamaño más pequeño y no volador en Hypothenemus, generalmente hay dimorfismo sexual en la frente (Johnson et al., 2020).

Figura 20. a, Vista dorsal de Hypothenemus meridensis (tomada de Atkinson, 2025); b, vista dorsal de H. eruditus (tomada de Atkinson, 2025); c, vista lateral de H. meridensis (tomada de Atkinson, 2025); d, vista lateral de H. eruditus (tomada de Atkinson, 2025); e, vista dorsal del pronoto de H. meridensis; f, vista dorsal del pronoto de H. eruditus.
Clave para las especies de la tribu Trypophloeini
1. Margen anterior del pronoto con 2 dientes (fig. 20e); pendiente anterior del pronoto con dientes gruesos elevados Hypothenemus meridensis,Wood
1’. Margen anterior del pronoto con 6 dientes (fig. 20f); pendiente anterior del pronoto con dientes medianos 2
2. Tamaño pequeño, 1.0- 1.3 mm; frente con superficie rugosa y reticulada; élitros con interestrías 2 veces más anchas que estrías Hypothenemus eruditus Westwood
2’. Tamaño del cuerpo de 1.4- 1.6 mm; frente rugosa y reticulada, con surco o tubérculo; élitros con estrías tan anchas como interestrías 3
3. Frente con tubérculo pequeño ubicado encima del nivel superior de ojos y surco poco profundo que se extiende desde el tubérculo hasta el epistoma (fig. 21e); declive elitral fuertemente convexo (fig. 21c) Hypothenemus crudiae (Panzer)
3’. Frente con surco poco profundo que llega hasta la tercera parte de distancia del margen del epistoma (fig. 21f); declive elitral convexo (fig. 21d) Hypothenemus seriatus (Eichhoff)
Hypothenemus meridensis Wood, 2007 (fig. 20a, c, e)
Distribución. Argentina: Tucumán; América del Sur: Brasil y Venezuela (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Hypothenemus eruditus Westwood, 1836 (fig. 20b, d, f)
Distribución. Argentina: Buenos Aires, Corrientes, Misiones, Santiago del Estero y Tucumán; América del Sur: Brasil, Colombia, Ecuador, Guyana, Trinidad y Tobago y Venezuela (Atkinson, 2025; Córdoba y Atkinson, 2018; Córdoba et al., 2021, 2023, 2025; Smith et al., 2017; Wood, 2007).
Hypothenemus crudiae (Panzer, 1791)* (fig. 21a, c, e)
Distribución. Argentina: Buenos Aires y Tucumán; América del Sur: Bolivia, Brasil, Colombia, Ecuador, Guyana, Paraguay, Surinam, Trinidad y Tobago y Venezuela (Atkinson, 2025; Atkinson y Flechtmann, 2021; Córdoba et al., 2023, 2025; Wood, 2007).
Comentarios. Esta especie se distribuye desde Estados Unidos hasta Argentina, también posiblemente introducida en Asia y África.
Hypothenemus seriatus (Eichhoff, 1872) (fig. 21b, d, f)
Distribución. Argentina: Tucumán; América del Sur: Bolivia, Brasil, Colombia, Ecuador, Paraguay, Perú y Venezuela (Atkinson, 2025; Córdoba et al., 2021, 2023, 2025; Smith et al., 2017; Wood, 2007).
Tribu Xyleborini LeConte, 1876

Figura 21. a, Vista dorsal de Hypothenemus crudiae (tomada de Atkinson, 2025); b, vista dorsal de H. seriatus (tomada de Atkinson, 2025); c, vista lateral de H. crudiae (tomada de Atkinson, 2025); d, vista lateral de H. seriatus (tomada de Atkinson, 2025); e, vista frontal de H. crudiae (tomada de Atkinson, 2025); f, vista frontal de H. seriatus.
Se caracterizan por presentar dimorfismo sexual marcado, macho generalmente más pequeño que hembra y no volador, ojo reducido en tamaño y haploide, la hembra normal y diploide; frente convexa, sin ornamentaciones; ojos son emarginados o divididos; frecuentemente escapo antenal alargado, funículo lleva 5 segmentos y maza antenal truncada de manera oblicua; parte anterior del pronoto empinada y armada con asperezas; procoxas varían de contiguas a ampliamente separadas; protibias expandidas, arqueadas y armadas con dentículos; escutelo puede ser grande y plano o modificado o ausente; en cuanto a su biología, la xilomicetofagia y la poligamia endogámica son universales en esta tribu (Wood, 2007).
Clave para las especies de la tribu Xyleborini
1. Declive de élitros abruptamente truncados con quilla circundeclivital, cara del declive ligeramente convexa con 3 estrías marcadas (fig. 22a, c, e); élitros tan largos como pronoto; procoxas contiguas (fig. 22g) Amasa parviseta Knížek et Smith
1’. Declive elitral aplanado o convexo, nunca truncado; élitros más largos que pronoto; procoxas contiguas o separadas 2
2. Escutelo en forma de espina y poco visible, dejando base de élitros con sutura hueca y cubierta de setas 3
2’. Escutelo en forma triangular y visible, concavidad sutural completamente llena hasta uperficie anterior de élitros, emarginación sin setas 5
3. Declive elitral convexo, empinado y débilmente impreso (fig. 22d, f); margen anterior del pronoto armado por dientes pequeños; longitud del cuerpo 1.9 a 2.4 mm Xyleborinus saxesenii (Ratzeburg)
3’. Declive elitral empinado e impreso; margen anterior del pronoto débilmente aserrado; longitud del cuerpo 2.0 a 2.6 mm 4
4. Frente reticulada, toscamente punteada (fig. 23e); longitud del cuerpo 2.0 a 2.2 mm y 2.9 más largo que ancho; declive elitral empinado e impreso hasta la sutura 3, con interestrías 1 y 2 impresas sin tubérculos, 3 débilmente elevada con 4 espinas (3 de mayor tamaño), intercaladas con otras más pequeñas, interestría 4 con tubérculos puntiagudos pequeños (fig. 23g) Xyleborinus linearicollis (Schedl)
4’. Frente reticulada con punciones gruesas y profundas (fig. 23f); longitud del cuerpo 2.3 a 2.6 mm y 3.2 veces más largo que ancho; declive elitral corto, muy empinado, fuertemente impreso desde la sutura hasta la interestría 3, interestría 1 con un tubérculo en la base, interestría 3 moderadamente elevada con 3 espinas grandes igualmente espaciadas (fig. 23h) Xyleborinus sentosus (Eichhoff)
5. Procoxas moderada o ampliamente separadas; pieza intercoxal continua, longitudinalmente sin emarginación 6
5’. Procoxas contiguas; pieza intercoxal longitudinalmente emarginada 7
6. Longitud del cuerpo 1.3 a 1.5 mm; coloración castaño oscura; pronoto más ancho en base, lados bastante convexos que convergen al ápice estrechamente redondeado, con mechón de setas ubicado longitudinalmente en la base del pronoto (fig. 24a, e); declive elitral brillante abruptamente redondeado en la base, con carena subserrada en el margen posterolateral, interestrías 2 y 3 con fila de pequeños tubérculos (fig. 24g) Xylosandrus curtulus (Eichhoff)
6’. Longitud del cuerpo 2.1 a 2.9 mm; coloración castaño rojiza; pronoto más ancho en base, lados poco convexos, con setas largas en los bordes y medianas en toda la superficie (fig. 24b, f); declive elitral opaco, muy convexo, densamente cubierto por pequeños gránulos uniforme e irregularmente distribuidos, con carena irregularmente dentada (fig. 24h) Xylosandrus crassiusculus Motschulsky
7. Tercio apical de cara posterior del maza antenal con 2 suturas, cara anterior con segundo segmento más grande, esclerotizado y levemente curvado (fig. 25e, g); cuerpo pequeño, robusto, convexo; longitud del cuerpo 1.8 a 2.1 mm; margen anterior del pronoto armado con 5 dientes medianos Coptoborus villosulus (Blandford)
7’. Tercio apical de cara posterior de maza antenal con 1 o sin suturas marcadas, cara anterior con segundo segmento, si es visible, no esclerotizado y fuertemente curvado (fig. 25f, h); cuerpo alargado, perfil muy levemente convexo a aplanado; longitud del cuerpo 2.0 a 3.2 mm; margen anterior de pronoto sin dientes 8
8. Pronoto subcuadrado (fig. 25b), margen anterior recto, superficie finamente estriada; longitud 2.2 a 2.5 mm; interestrías del declive elitral con filas de tubérculos de diferente tamaño Euwallacea posticus (Eichhoff)
8’. Pronoto más largo que ancho, margen anterior procurvado, superficie lisa; longitud 2.0 3.2 mm; interestrías del declive elitral con tubérculos o espinas 9
9. Declive elitral aplanado y brilloso 10
9’. Declive elitral convexo y opaco o brilloso 11
10. Especie pequeña, cuerpo delgado, longitud del cuerpo 2.0 a 2.9 (fig. 26a); frente con quilla débil ancha que se extiende en zona media, desde epistoma hasta ojos (fig. 26e); declive elitral suavemente empinado, interestría 3 con tubérculo mediano más cerca del ápice que de base del declive (fig. 24g) Xyleborus ferrugineus (Fabricius)
10’. Especie grande, cuerpo robusto, longitud del cuerpo 2.8 a 3.2 (fig. 24b); frente con quilla confinada a zona superior del epistoma (fig. 26f); declive elitral abrupto y empinado, interestría 3 con tubérculo mediano más cerca de base que del ápice del declive (fig. 26h) Xyleborus bispinatus Eichhoff
11. Frente con gránulos pequeños y dispersos (fig. 27e); declive elitral muy empinado y base abrupta (fig. 27c), interestría 1 con tubérculo grande ubicado sobre base protuberante en el tercio basal (fig. 27a, c, g) Xyleborus biconicus Eggers
11’. Frente reticulada sin gránulos; declive eitral con tubérculos pequeños o medianos en las interestrías (fig. 27h) 12
12. Frente fuertemente reticulada y de superficie opaca (fig. 27f); superficie del declive elitral opaca (fig. 27h) Xyleborus affinis Eichhoff
12’. Frente reticulada y de superficie brillante; superficie del declive elitral brillante (fig. 28g, h) 13
13. Frente toscamente reticulada, con línea media elevada y lisa desde el epistoma hasta el nivel superior de los ojos (fig. 28e); declive elitral con interestría 1 con 3 a 5 tubérculos puntiagudos y de tamaño mediano, interestría 2 con 2 o 3 tubérculos puntiagudos y medianos en el cuarto basal y 1 o 2 medianos cerca del ápice, interestría 3 con 3 tubérculos puntiagudos medianos muy espaciados entre sí en el 3 cuarto basal y 3 o más tubérculos pequeños en el cuarto basal (fig. 28g); margen ventrolateral del declive moderadamente elevado y con crenulaciones; coloración del cuerpo castaño rojizo Xyleborus volvulus (Fabricius)
13’. Frente fuertemente reticulada y sin elevaciones (fig. 28f); declive elitral con interestría 1 débilmente elevada, 2 y 3 con fila de tubérculos pequeños y de igual tamaño; coloración del cuerpo castaño rojizo muy oscuro Xyleborus scaber Schedl
Amasa parviseta Knížek et Smith, 2024* (fig. 22a, c, e, g)
Distribución. Argentina: Tucumán; América del Sur: Brasil y Uruguay (Atkinson, 2025; Córdoba et al., 2023, 2025; Flechtmann y Cognato, 2011; Gómez et al., 2017a; Knížek y Smith, 2024; Rainho et al., 2018)

Figura 22. a, Vista dorsal de Amasa parviseta (tomada de Atkinson, 2025); b, vista dorsal de Xyleborinus saxesenii (tomada de Atkinson, 2025); c, vista lateral de A. parviseta (tomada de Atkinson, 2025); d, vista lateral de X. saxesenii (tomada de Atkinson, 2025); e, vista posterior de A. parviseta (tomada de Atkinson, 2025); f, vista posterior de X. saxesenii (tomada de Atkinson, 2025); g, vista ventral de A. parviseta (tomada de Atkinson, 2025).
Comentarios. Es originaria de Australia y se extendió en asociación con especies introducidas de eucalipto. Se informó en Brasil (2015) (Rainho et al., 2018), Uruguay en 2015 (Gómez et al., 2017a), Chile en 2016 (Kirkendall, 2018) y Argentina en 2018 (Córdoba et al., 2023) como A. truncata y A. nr. truncata.
Xyleborinus saxesenii (Ratzeburg, 1837)* (fig. 22b, d, f)
Distribución. Argentina: Buenos Aires, Salta, Santiago del Estero y Tucumán; América del Sur: Brasil, Chile, Ecuador, Paraguay y Uruguay (Atkinson, 2025; Córdoba y Atkinson, 2018; Córdoba et al., 2021, 2023, 2025; Gómez et al., 2017a; Iturre y Darchuck, 1996; Wood, 2007).
Comentarios. Esta es una especie euroasiática y ha sido introducida en todas las regiones templadas y subtropicales del mundo.
Xyleborinus linearicollis (Schedl, 1937) (fig. 23a, c, e, g)
Distribución. Buenos Aires y Tucumán; América del Sur: Brasil (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Xyleborinus sentosus (Eichhoff, 1868) (fig. 23b, d, f, h)
Distribución. Argentina: Tucumán; América del Sur: Brasil, Paraguay y Perú (Atkinson, 2025; Córdoba et al., 2021, 2023, 2025; Smith et al., 2017; Wood, 2007).

Figura 23. a, Vista dorsal de Xyleborinus linearicollis (tomada de Atkinson, 2025); b, vista dorsal de X. sentosus (tomada de Atkinson, 2025); c, vista lateral de X. linearicollis (tomada de Atkinson, 2025); d, vista lateral de X. sentosus (tomada de Atkinson, 2025); e, vista frontal de X. linearicollis (tomada de Atkinson, 2025); f, vista frontal de X. sentosus (tomada de Atkinson, 2025); g, vista posterior de X. linearicollis (tomada de Atkinson, 2025); h, vista posterior de X. sentosus (tomada de Atkinson, 2025).
Xylosandrus curtulus (Eichhoff, 1869) (fig. 24a, c, e, g)
Distribución. Argentina: Salta y Tucumán; América del Sur: Bolivia, Brasil, Colombia, Ecuador, Perú y Venezuela (Atkinson, 2025; Córdoba y Atkinson, 2018; Córdoba et al., 2021, 2023, 2025; Martínez et al., 2019; Smith et al., 2017; Wood, 2007).
Xylosandrus crassiusculus Motschulsky, 1866* (fig. 24b, d, f, h)
Distribución. Argentina: Buenos Aires y Tucumán; América del Sur: Brasil, Guyana Francesa y Uruguay (Atkinson, 2025; Landi et. al., 2017; Córdoba y Atkinson, 2018; Córdoba et al., 2021, 2023, 2025; Martínez et al., 2019).
Comentarios. Probablemente es originaria de Asia tropical y subtropical, pero se ha extendido ampliamente en regiones cálidas y húmedas de todo el mundo.
Coptoborus villosulus (Blandford, 1898) (fig. 25a, c, e, g)
Distribución. Argentina: Tucumán; América del Sur: Bolivia, Brasil, Colombia, Ecuador, Guyana Francesa, Perú, Trinidad y Tobago y Venezuela (Atkinson, 2025; Córdoba y Atkinson, 2018; Córdoba et al., 2021, 2023, 2025; Smith y Cognato, 2021; Wood, 2007).
Euwallacea posticus (Eichhoff, 1869) (fig. 25b, d, f, h)
Distribución. Misiones y Tucumán; América del Sur: Bolivia, Brasil, Colombia, Ecuador, Guyana, Paraguay, Perú, Surinam, Trinidad y Tobago y Venezuela (Atkinson, 2018; Atkinson, 2025; Córdoba y Atkinson, 2018; Córdoba et al., 2021, 2023, 2025; Wood, 2007).

Figura 24. a, Vista dorsal de Xylosandrus curtulus (tomada de Atkinson, 2025); b, vista dorsal de X. crassiusculus (tomada de Atkinson, 2025); c, vista lateral de X. curtulus (tomada de Atkinson, 2025); d, vista lateral de X. crassiusculus (tomada de Atkinson, 2025); e, detalle pronoto de X. curtulus; f, detalle pronoto de X. crassiusculus (modificada de Atkinson, 2025); g, vista posterior de X. curtulus (tomada de Atkinson, 2025); h, vista posterior de X. crassiusculus (tomada de Atkinson, 2025).

Figura 25. a, Vista dorsal de Coptoborus villosulus (tomada de Atkinson, 2025); b, vista dorsal de Euwallacea posticus (tomada de Atkinson, 2025); c, vista lateral de C. villosulus (tomada de Atkinson, 2025); d, vista lateral de E. posticus (tomada de Atkinson, 2025); e, vista posterior de la antena de C. villosulus; f, vista posterior de la antena de E. posticus; g, vista anterior de la antena de C. villosulus; h, vista anterior de la antena de E. posticus.

Figura 26. a, Vista dorsal de Xyleborus ferrugineus (tomada de Atkinson, 2025); b, vista dorsal de X. bispinatus (tomada de Atkinson, 2025); c, vista lateral de X. ferrugineus (tomada de Atkinson, 2025); d, vista lateral de X. bispinatus (tomada de Atkinson, 2025); e, vista frontal de X. ferrugineus (tomada de Atkinson, 2025); f, vista frontal de X. bispinatus (tomada de Atkinson, 2025); g, vista posterior de X. ferrugineus (tomada de Atkinson, 2025); h, vista posterior de X. bispinatus (tomada de Atkinson, 2025).
Xyleborus ferrugineus (Fabricius, 1801) (fig. 26a, c, e, g)
Distribución. Argentina: Jujuy, Salta y Tucumán. América del Sur: Bolivia, Brasil, Chile, Colombia, Ecuador, Guyana Francesa, Guyana, Paraguay, Perú, Surinam, Trinidad y Tobago, Uruguay y Venezuela (Atkinson, 2025; Córdoba y Atkinson, 2018; Córdoba et al., 2021, 2023, 2025; Martínez et al., 2019; Smith et al., 2017; Atkinson, 2025).
Xyleborus bispinatus Eichhoff, 1868 (fig. 26b, d, f, h)
Distribución. Argentina: Tucumán; América del Sur: Bolivia, Brasil, Colombia, Ecuador, Guyana Francesa, Paraguay, Perú, Surinam, Trinidad y Tobago y Venezuela (Atkinson, 2025; Córdoba et al., 2021, 2023, 2025; Martínez et al., 2019; Smith et al., 2017).
Xyleborus biconicus Eggers, 1928 (fig. 27a, c, e, g)
Distribución. Argentina: Formosa y Misiones, Tucumán; América del Sur: Bolivia, Brasil, Guyana Francesa y Paraguay (Atkinson, 2025; Córdoba et al., 2023, 2025; Wood, 2007).
Xyleborus affinis Eichhoff, 1868 (fig. 27b, d, f, h)
Distribución. Argentina:Jujuy, Misiones, Salta y Tucumán; América del Sur: Bolivia, Brasil, Chile, Colombia, Ecuador, Guyana Francesa, Guyana, Paraguay, Perú, Surinam, Trinidad y Tobago, Uruguay y Venezuela (Atkinson, 2025; Córdoba y Atkinson, 2018; Córdoba et al., 2021, 2023, 2025; Martínez et al., 2019; Smith et al., 2017).
Xyleborus volvulus (Fabricius, 1775)* (fig. 28a, c, e, g)
Distribución. Argentina:Jujuy yMisiones; América del Sur: Bolivia, Brasil, Colombia, Ecuador, Guyana Francesa, Guyana, Paraguay, Perú, Surinam, Trinidad y Tobago, Uruguay y Venezuela (Atkinson, 2025; Córdoba y Atkinson, 2018; Córdoba et al., 2021, 2023, 2025; Martínez et al., 2019; Smith et al., 2017; Wood, 2007).
Xyleborus scaber Schedl, 1949 (fig. 28b, d, f, h)
Distribución. Argentina: Tucumán; América del Sur: Brasil (Atkinson, 2025; Córdoba et al., 2023, 2025).

Figura 27. a, Vista dorsal de Xyleborus biconicus (tomada de Atkinson, 2025); b, vista dorsal de X. affinis (tomada de Atkinson, 2025); c, vista lateral de X. biconicus (tomada de Atkinson, 2025); d, vista lateral de X. affinis (tomada de Atkinson, 2025); e, vista frontal de X. biconicus (tomada de Atkinson, 2025); f, vista frontal de X. affinis (tomada de Atkinson, 2025); g, vista posterior de X. biconicus (tomada de Atkinson, 2025); h, vista posterior de X. affinis (tomada de Atkinson, 2025).
Discusión
Atkinson (2025) enumera 199 especies de Scolytinae para la Argentina. De estas especies, 56 están presentes en Tucumán, lo cual representa aproximadamente 31% de las especies conocidas de la subfamilia para el país. Consideramos que esta cifra es muy baja en comparación con la fauna de otras regiones neotropicales. El número de especies tucumanas coincide con la abundancia de especies de la tribu Xyleborini documentadas en todo el territorio mexicano, siendo esta tribu uno de los grupos más diversos a nivel mundial (Pérez-Silva et al., 2021).
La diversidad de especies en la provincia de Tucumán, comparada con los países limítrofes ubicados aproximadamente a la misma latitud (Chile, Paraguay y Uruguay) es alta, ya que Atkinson (2025) reporta 52 especies para Chile, 46 para Paraguay y 14 para Uruguay. En Argentina, 10% de las especies son introducidas, mientras que en Uruguay más de la mitad (57%) son especies exóticas. Esto se debe al incremento de terrenos destinados a la plantación de especies forestales arbóreas en Uruguay y al crecimiento del comercio internacional, en particular el intercambio de embalajes de madera, lo que facilita el establecimiento de especies exóticas (Gómez et al, 2017b). En la provincia de Tucumán, 12% son especies introducidas, lo que puede deberse al bajo porcentaje de superficie forestal. La mayoría de estas especies fueron recolectadas en ambientes naturales, son especies establecidas en el país y su origen foráneo está bien documentado (Wood, 1982, 2007).

Figura 28. a, Vista dorsal de Xyleborus volvulus (tomada de Atkinson, 2025); b, vista dorsal de X. scaber (tomada de Atkinson, 2025); c, vista lateral de X. volvulus (tomada de Atkinson, 2025); d, vista lateral de X. scaber (tomada de Atkinson, 2025); e, vista frontal de X. volvulus (tomada de Atkinson, 2025); f, vista frontal de X. scaber (tomada de Atkinson, 2025); g, vista posterior de X. volvulus (tomada de Atkinson, 2025); h, vista posterior de X. scaber (tomada de Atkinson, 2025).
Aunque Wood (2007) realizó una revisión de los Scolytinae para América del Sur, donde se incluyen especies presentes en Argentina, las nuevas especies, los recientes registros y los cambios taxonómicos hacen necesarias claves actualizadas. Además, no se cuenta con claves para la identificación a nivel más local, para la provincia y el país. Uno de los problemas principales de la clave de tribus de Wood (2007) es que intenta seguir sus ideas sobre la filogenia de los grupos y muchas veces ignora características sencillas, empleando algunas más difíciles de interpretar. Como consecuencia, muchos de sus dilemas son demasiado largos y complejos, dificultando su interpretación. Otro problema es que sigue estrictamente un concepto dicotómico sin presentar una matriz de caracteres que esconde similitudes para el reconocimiento. Por ejemplo, en todos los géneros de la tribu Scolytini, la cabeza está descubierta en vista dorsal a pesar de la impresión que presenta la clave en el primer dilema. Hay otros ejemplos que se pueden citar. Aquí hemos intentado usar caracteres menos ambiguos, sin considerar su supuesto valor filogenético.
Las presentes claves taxonómicas, que incorporan los cambios, especies recientemente descritas y nuevos registros, constituyen una importante herramienta para la identificación rápida de las especies de Argentina y América del Sur, lo cual puede ser de gran utilidad en casos de invasión de los cultivos o para futuras investigaciones.
Agradecimientos
A Eduardo Agustín Mendoza (Área Biología Integrativa, Fundación Miguel Lillo) por su valiosa colaboración y asistencia en todas las colectas en el campo. A Pablo Pereyra (Instituto de Iconografía, Área de Zoología, Fundación Miguel Lillo) por su contribución en la toma de fotografías y edición de las mismas.
Referencias
Atkinson, T. H. (2017). Familia Curculionidae: Scolytinae y Platypodinae. En T. D. Cibrián (Ed.), Fundamentos de entomología forestal (pp. 269–278). Texcoco: Universidad Autónoma de Chapingo.
Atkinson, T. H. y Flechtmann, C. A. H. (2021). New species, new records and synonymy of Brazilian species of Hypothenemus Westwood, 1834 (Coleoptera: Curculionidae: Scolytinae). Insecta Mundi, 846, 1–33. https://doi.org/10.11646/zootaxa.4442.2.11
Atkinson, T. H. (2025). Bark and ambrosia beetles of the Americas. Recuperado el 21 marzo, 2025 de: http://www.barkbeetles.info
Bachman, A. O. y Lanteri, A. A. (2013). Catalog of the types of Curculionoidea (Insecta: Coleoptera) deposited at the Museo Argentino de Ciencias Naturales ‘Bernardino Rivadavia’, Buenos Aires. Revista del Museo Argentino de Ciencias Naturales, 15, 209–280. https://doi.org/10.22179/revmacn.15.183
Bosq, J. M. (1943). Segunda lista de coleópteros de la República Argentina dañinos a la agricultura (reedición de Ingeniería Agronómica, IV, 18–22, Buenos Aires 1942). Revista del Ministerio de Agricultura de la Nación, Dirección de Sanidad Vegetal, 4, 1–80.
Bruch, C. (1914). Catálogo sistemático de los coleópteros de la República Argentina, Pars VII. Revista del Museo de La Plata, 19, 401–441. https://doi.org/10.5962/bhl.title.8799
Córdoba, S. P. y Atkinson, T. H. (2018). New records of Scolytinae (Coleoptera: Curculionidae) from Argentina. The Coleopterists Bulletin, 72,376–379. https://doi.org/10.1649/0010-065x-72.2.376
Córdoba, S. P., Mendoza, E. A., Atkinson T. H. y Manzo, M. V. (2021). Diversidad y dinámica poblacional de Scolytinae (Coleoptera: Curculionidae) en plantaciones de palto y bosque natural circundante en el NW de Argentina. Dugesiana, 28, 115–130. https://doi.org/10.32870/dugesiana.v28i2.7151
Córdoba, S. P., Atkinson, T. H. y Mendoza, E. A. (2023). Checklist of the subfamily Scolytinae (Coleoptera: Curculionidae) in Tucumán province, Argentina. Zootaxa, 5353,501–532. https://doi.org/10.11646/zootaxa.5353.6.1
Córdoba, S. P., Atkinson, T. H. y Mendoza, E. A. (2025). Listado preliminar de Scolytinae (Coleoptera: Curculionidae) de la provincia de Tucumán (adiciones y correcciones) y sus plantas hospedantes de Argentina. Dugesiana, 32, 13–38. https://doi.org/10.32870/dugesiana.v32i1.7357
Costilla, M. A. y Coronel, N. B. (1994). El taladillo de la semilla del palto Pagiocerus fiorii Eggers, 1940 (Bostrichus frontalis Fbricius, 1801) (Coleoptera: Scolytidae). Revista Industrial y Agrícola de Tucumán, 71, 63–68.
Flechtmann, C. A. H. y Cognato, A. I. (2011). First report of Amasa truncata (Erichson) (Coleoptera: Curculionidae: Scolytinae) in Brazil. Coleopterists Bulletin, 65,417–421. https://doi.org/10.1649/072.065.0419
Gómez, D., Suárez, M. y Martínez, G. (2017a). Amasa truncata (Erichson) (Coleoptera: Curculionidae: Scolytinae): A new exotic ambrosia beetle in Uruguay. Coleopterists Bulletin, 71, 825–826. https://doi.org/10.1649/0010-065x-71.4.825
Gómez, D., Irigoyen, A., Balmelli, G., Viera, C. y Martínez, G. (2017b). Patterns in flight phenologies of bark beetles (Coleoptera: Scolytinae) in commercial pine tree plantations in Uruguay. Bosque, 38, 47–53. https://doi.org/10.4067/s0717-92002017000100006
Hayward, K. J. (1960). Insectos tucumanos perjudiciales. Revista Industrial y Agrícola de Tucumán, 42, 3–144.
Hulcr, J., Atkinson, T. H., Cognato, A. I., Jordal, B. H. y McKenna, D. D. (2015). Morphology, taxonomy and phylogenetics of bark beetles. En F. E. Vega y R. W. Hofstetter (Eds.), Bark beetles: biology and ecology of native and invasive species (pp. 41–84). New York: Species Academic Press. https://doi.org/10.1016/b978-0-12-417156-5.00002-2
Iturre, M. y Darchuck, E. (1996). Registro de escolítidos relacionados al género Eucalyptus en Santiago del Estero. Quebracho, 4, 11–16.
Johnson, A. J., Hulcr, J., Knížek, M., Atkinson, T. H., Mandelshtam, M. Y., Smith, S. M. et al. (2020). Revision of the bark beetle genera within the former Cryphalini (Curculionidae: Scolytinae). Insect Systematics and Diversity, 4, 1–81. https://doi.org/10.1093/isd/ixaa002
Jordal, B. H. y Smith, S. M. (2020). Scolytodes Ferrari (Coleoptera, Scolytinae) from Ecuador: 40 new species, and a molecular phylogenetic guide to infer species differences. Zootaxa, 4813, 1–67. https://doi.org/10.11646/zootaxa.4813.1.1
Kirkendall, L. R. (2018). Invasive bark beetles (Coleoptera, Curculionidae, Scolytinae) in Chile and Argentina, including two species new for South America, and the correct identity of the Orthotomicus species in Chile and Argentina. Diversity, 10, 2–20. https://doi.org/10.3390/d10020040
Kirkendall, L. R. y Jordal, B. H. (2006). Revision of the bark beetle genera within the former Cryphalini (Curculionidae: Scolytinae). Taxonomy, 4,1–81.
Kirkendall, L. R., Biederman, P. H. W. y Jordal, B. H. (2015). Evolution and diversity of bark and ambrosia beetles. En F. E. Vega y R. W. Hofstetter (Eds.), Bark beetles: Biology and ecology of native and invasive species (pp. 85–156). Cambridge, USA: Academic Press. https://doi.org/10.1016/b978-0-12-417156-5.00003-4
Knížek, M. y Smith, S. M. (2024). A new widely distributed invasive alien species of Amasa ambrosia beetles (Coleoptera: Curculionidae: Scolytinae: Xyleborini). Zootaxa, 5403,385–390. https://doi.org/10.11646/zootaxa.5403.3.8
Landi, L., Gómez, D., Braccini, C. L, Pereyra, V. A., Smith, S. M. y Marvaldi, A. E. (2017). Morphological and molecular identification of the Invasive Xylosandrus crassiusculus (Coleoptera: Curculionidae: Scolytinae) and its South American range extending into Argentina and Uruguay. Annals of the Entomological Society of America, 110, 344–349. https://doi.org/10.1093/aesa/sax032
Lombardero, M. J. (1995). Plantas huésped y escolítidos (Col.: Scolytidae) en Galicia (noroeste de la península Ibérica). Boletín de Sanidad Vegetal. Plagas, 21,357–370.
Martínez, M., Cognato, A. I., Guachambala, M. y Boivin, T. (2019). Bark and ambrosia beetles (Coleoptera: Curculioni-
dae: Scolytinae) diversity in natural and plantation forests
in Ecuador. Environmental Entomology, 48,603–613. https://doi.org/10.1093/ee/nvz037
Morris, J. L., Cottrell, S., Fettig, C. J., Hansen, W. D., Sherriff, R. L., Carter, V. A. et al. (2018). Managing bark beetle impacts on ecosystems and society: Priority questions to motivate future research. Frontiers in Ecology and the Environment, 16, 34–43. https://doi.org/10.1002/fee.1754
Pérez-De la Cruz, M., Hernández-May, M. A., De la Cruz-Pérez, A. y Sánchez-Soto, S. (2016). Scolytinae y Platypodinae (Coleoptera: Curculionidae) de dos áreas de conservación en Tabasco, México. Biología Tropical, 64,319–326. https://doi.org/10.15517/rbt.v64i1.15931
Pérez-Silva, M., Equihua-Martínez, A., Atkinson, T. H., Romero-Nápoles, J. y López-Buenfil, J. A. (2021). Claves ilustradas para la identificación de géneros y especies de la tribu Xyleborini (Curculionidae: Scolytinae) de México. Revista Mexicana de Biodiversidad, 92, e923817. https://doi.org/10.22201/ib.20078706e.2021.92.3817
Petrov, A. V. (2017). New data on Scolytini Latreille, 1804, mainly from Peru, with description of two new species of Cnemonyx Eichhoff, 1868 (Coleoptera: Curculionidae: Scolytinae). Koleopterologische Rundschau, 87, 325–334. https://doi.org/10.31857/s0367144523020119
Rainho, H. L., Silva, W. D., Leite, M. O. G. y Bento, J. M. S. (2018). Notes on the distribution of the exotic ambrosia beetle Amasa truncata (Erichson) (Coleoptera: Curculionidae: Scolytinae) in southeastern Brazil. Coleopterists Bulletin, 72, 870–872. https://doi.org/10.1649/0010-065x-72.4.870
Santoro, F. H. (1966). Panorama entomológico relacionado con la Silvicultura y la tecnología forestal en la República Argentina. Revista Forestal Argentina, 10, 52–59.
Smith, S. M., Petrov, A. V. y Cognato, A. I. (2017). Beetles (Coleoptera) of Peru: a survey of the familie (Curculionidae: Scolytinae). The Coleopterists Bulletin, 71, 77–94. https://doi.org/10.1649/0010-065x-71.1.77
Smith, S. M. y Cognato, A. I. (2021). A revision of the Neotropical genus Coptoborus Hopkins (Coleoptera, Curculionidae, Scolytinae, Xyleborini). Zookeys, 1044, 609–720. https://doi.org/10.3897/zookeys.144.62246
Viana, M. J. (1964). Datos ecológicos de Scolytidae argentinos (Coleoptera). Revista de la Sociedad Entomológica Argentina, 27, 119–130.
Wood, S. L. (2007). Bark and ambrosia beetles of South America (Coleoptera, Scolytidae). Monte L. Brigham Young University, Provo, Utah: Bean Life Science Museum. https://doi.org/10.1134/s001387380902016x
Wood, S. L. (1982). The bark and ambrosia beetles of North and Central America (Coleoptera: Scolytidae), a Taxonomic Monograph. Great Basin Naturalist Memoirs, 6, 1–1359.
Wood, S. L. y Bright, D. E. (1992). A catalog of Scolytidae and Platypodidae (Coleoptera), Part 2: Taxonomic index, volumes A and B. Provo, Utah: Great Basin Naturalist Memoirs.