Algae diversity and new records of Xanthophyceae and Eustigmatophyceae (Heterokontophyta) in the central region of Mexico
Alejandra Mireles-Vázquez a, b, * y Eberto Novelo b
a Universidad Nacional Autónoma de México, Posgrado en Ciencias del Mar y Limnología, Av. Universidad 3000, Ciudad Universitaria, Coyoacán, 04510 Ciudad de México, México
b Universidad Nacional Autónoma de México, Facultad de Ciencias, Departamento de Biología Comparada, Laboratorio Algas Continentales, Ecología y Taxonomía, Circuito Exterior s/n, Ciudad Universitaria, Coyoacán, 04510 Ciudad de México, México
*Autor para correspondencia: alemirelesv@ciencias.unam.mx (A. Mireles-Vázquez)
Recibido: 24 marzo 2025; aceptado: 25 agosto 2025
Resumen
Heterokontophyta incluye una gran variedad de algas con distintos niveles de organización, ambientes, presencia de pigmentos e incluso líneas evolutivas. En México se han registrado 72 especies de aguas continentales que pertenecen a las clases Xanthophyceae y Eustigmatophyceae desde distintos enfoques: florístico, ecológico, limnológico, morfométrico, químico y filogenético. Con el objetivo de conocer la diversidad de algas doradas en el centro de México y actualizar los registros en bases de datos especializadas nacionales, se recolectó material en 8 cuerpos de agua de la región central; en cada sitio se filtraron 10 L con una red de fitoplancton. De algunas muestras se desarrollaron cultivos que permitieron obtener imágenes en microscopio electrónico de barrido. Se realizó un análisis de similitud con el índice de Jaccard y un agrupamiento de los sitios usando variables ambientales. Se identificaron y caracterizaron 18 especies de algas de las clases Xanthophyceae (10) y Eustigmatophyceae (8), 6 de ellas son nuevos registros para el país. Los análisis muestran una caracterización de los sitios y una distribución de las especies muy particular, pues los valores de similitud son de 0.125 a 0.33. Con estos resultados actualizamos el panorama de las algas doradas en la región central de México.
Palabras clave: Algas continentales; Florística; Heterokontophyta
Abstract
Heterokontophyta includes a wide variety of algae with different levels of organization, environments, presence of pigments and even evolutionary lines. In Mexico, 72 species of inland waters belonging to the classes Xanthophyceae and Eustigmatophyceae have been recorded from different approaches: floristic, ecological, limnological, morphometric, chemical and phylogenetic. To understand the diversity of golden algae in the central region of Mexico and update the records in specialized national databases, material was collected in eight bodies of water in the central region, at each site 10 L were filtered with a phytoplankton net. Cultures were developed from some samples that allowed obtaining images with a scanning electron microscope. A similarity analysis was performed with the Jaccard index and a grouping of the sites using environmental variables. Eighteen species of algae from the classes Xanthophyceae (10) and Eustigmatophyceae (8) were identified and characterized, 6 of which are new records for the country. The analyses show a very particular characterization of the sites and distribution of the species, since the similarity values are from 0.125 to 0.33. With these results we update the panorama of golden algae in the central region and their distribution.
Keywords: Continental algae; Floristic; Heterokontophyta
Introducción
La división Heterokontophyta está constituida por algas con una gran heterogeneidad de niveles de organización, ambientes, distribución geográfica, pigmentos principales y accesorios, ultraestructura celular y líneas evolutivas. Dos de las clases de esta división son representantes muy similares: Xanthophyceae y Eustigmatophyceae (Yang et al., 2012), que por más de 100 años estuvieron clasificadas en un solo grupo, Heterokontae (Rybalka, 2015).
En México se han registrado 72 especies continentales de Xanthophyceae y Eustigmatophyceae. Estos taxones están distribuidos en 19 entidades federativas de México registradas en 45 publicaciones, 17 corresponden a tesis (8 de licenciatura, 7 de maestría y 2 de doctorado), 18 en revistas periódicas y 10 son capítulos o libros (fig. 1). Las fuentes consultadas describen generalmente 1 o 2 especies con algún enfoque: 1a) listado florístico (Alcocer y Escobar, 1992; Cameron, 1960; Esqueda-Lara et al., 2016; Figueroa, 2009; Figueroa et al., 2015; Garduño-Solórzano et al., 2009; Godínez-Ortega et al., 2001; Hernández-Morales et al., 2011; López-Adrián y Barrientos-Medina, 2005; López-Adrián y Catzim, 2010; Mendoza-González, 1985; Mendoza-González et al., 1985; Montejano-Zurita et al., 2000, 2004; Moreno-Ruiz, 2005; Moreno-Ruiz et al., 2008; Novelo et al., 2023; Núñez-Márquez y Reyes González, 1995; Ortega-Murillo et al., 2014; Quiroz-Castelán et al., 2007; Vázquez y Blanco-Pérez, 2011); 1b) listado con ilustraciones o datos relacionados a otras especies (Aguirre-Cavazos et al., 2018; Carmona-Jiménez et al., 2016; Godínez-Ortega et al., 2017; Hernández-Morales et al., 2008; Moreno-Ruiz, 1985; Novelo et al., 2009; Ortega, 1984; Valadez-Cruz, 1998); 1c) con descripciones y datos de las especies (Adrián-Serrano, 2014; Agredano, 2019; Amateco-Rivero, 2011; Carmona-Jiménez, 1990; Flechtner et al., 1998; Flores-Granados, 1980; García-Rodríguez y Tavera, 1998; García-Rodríguez, 2004; González-Barrera, 1991; Martínez, 2016; Mireles, 2019; Moreno y Palacios, 1987; Novelo, 1998, 2014; Ochoa, 2023; Osorio y López, 2005; Pedraza, 2020; Ponce et al., 2019; Rodríguez-Flores, 2014; Sámano-Bishop, 1934; Valadez-Cruz et al., 1996; Zariñana-Leguízamo, 1997); 2) ecológico (Alvarado-Villanueva, 2003; Bojorge et al., 2010; Cantoral et al., 1999; Carmona-Jiménez y Montejano-Zurita, 1993; Carmona-Jiménez et al., 2022; Flórez, 2011; Jiménez, 2010; López-Adrián et al., 2017; Mora-Navarro, 2004; Mora-Navarro et al., 2004, 2006; Rodríguez-Flores y Carmona, 2018; Tavera y Díez, 2009; Valadez-Cruz et al., 2015); 3) limnológicos (Banderas-Tarabay, 1994, 1997; Ramírez, 2010; Sánchez-Gómez y Lara-Villa, 1986; Schmitter-Soto et al., 2002); 4) morfométrico (Chávez et al., 2005); 5) químico (Favari et al., 2002; Pérez-Gutiérrez et al., 2008); 6) filogenia molecular (Bonilla-Rodríguez et al., 2013).
La caracterización morfológica de las clases Xanthophyceae (Allorge ex F.E. Fritsch, 1935) y Eustigmatophyceae (D.J. Hibberd et Leedale, 1971) es complicada por varias causas: las poblaciones son pequeñas en las algas microscópicas y las macroscópicas, con frecuencia, no forman estructuras reproductoras. Las células de las algas microscópicas son generalmente pequeñas (menores de 15 micrómetros) y no se observan fácilmente en aumentos bajos. Hay muchas similitudes morfológicas con géneros de Chrysophyceae y Chlorophyceae, y además frecuentemente son confundidas entre ellas.
Analizar y trabajar los cuerpos de agua con énfasis en algas doradas es un desafío, sin embargo, dará información necesaria para avanzar en el conocimiento de la distribución geográfica y ambiental en la que viven estas algas. La agrupación (clustering) como herramienta de clasificación de los sitios de muestreo, permite identificar conjuntos de datos similares, las propiedades que se atribuyen (datos ambientales) se analizan y a mayor diferencia entre ellos, más alejados se muestran en un dendrograma (Rodríguez et al., 2019). El índice de Jaccard ha sido una medida fundamental en estudios de diversidad como éste, pues evalúa la coincidencia de un conjunto de datos (distribución de especies) y revela valores de menor o mayor similitud (Jaccard, 1901), es muy común en la comparación de diversidad de especies entre sitios o ecosistemas (Magurran, 2004). El objetivo de este trabajo es documentar la diversidad de algas doradas en la región central de México, su distribución a través de la similitud de presencia y ausencia en los ambientes sitios y actualizar las bases de datos especializadas nacionales.
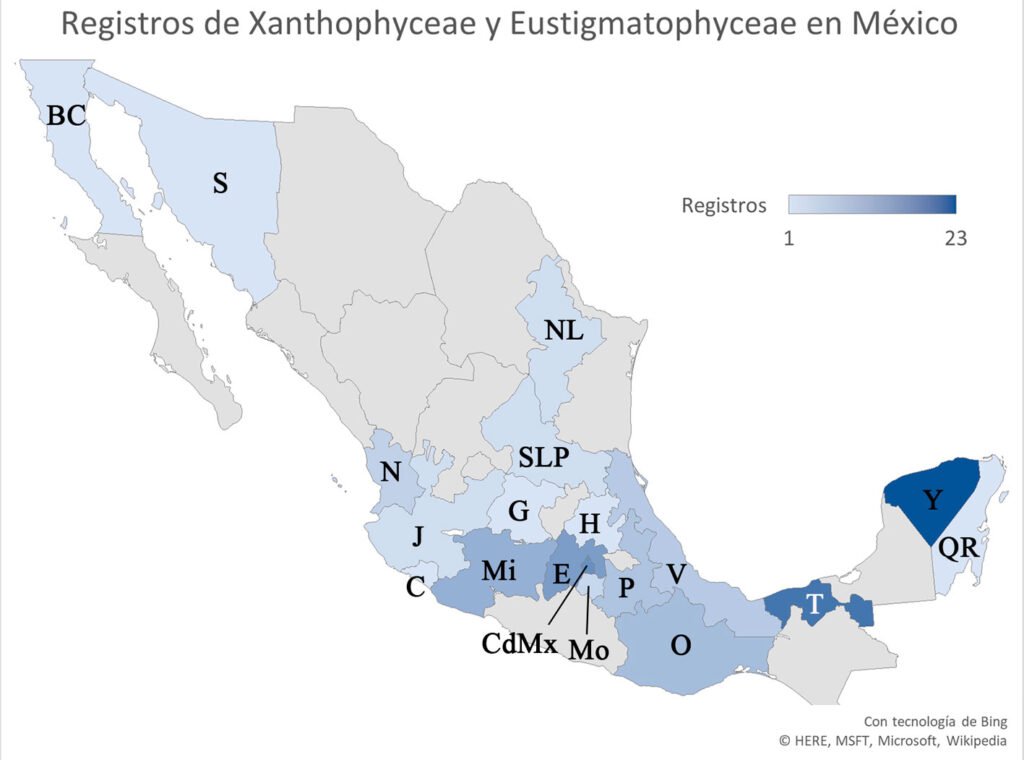
Figura 1. Registros de especies en México. BC: Baja California, C: Colima, CDMX: Ciudad de México, E: Estado de México, G: Guanajuato, H: Hidalgo, J: Jalisco, Mi: Michoacán, Mo: Morelos, N: Nayarit, NL: Nuevo León, O: Oaxaca, P: Puebla, Q: Quintana Roo, SLP: San Luis Potosí, S: Sonora, T: Tabasco, V: Veracruz, Y: Yucatán.
Materiales y métodos
Los cuerpos de agua muestreados en este trabajo corresponden a sitios con registros previos de especies de estas clases (Cantera Oriente, canal El Bordo, lago Huetzalín, presa Ignacio Ramírez) y otras localidades que se agregaron como posibles ambientes en donde podríamos encontrar las especies de interés (presa Requena, lagos Coatetelco, El Rodeo y Atlangatepec). En total, se muestrearon 8 lagos en la región central de México contemplando la Ciudad de México, Estado de México, Hidalgo, Morelos y Tlaxcala (fig. 2, tabla 1).
Tabla 1
Información sobre las localidades y fechas de colecta.
| Estado/ municipio | Cuerpo de agua | Número de localidad | Fecha de colecta | Muestra de herbario |
| Ciudad de México Xochimilco | Huetzalín | 1 | 13 de octubre de 2021 | FCME_CM971 |
| Coyoacán | Mexcalpique | 2 | 19 de octubre de 2021 | FCME_CM972-FCME_CM973 |
| Xochimilco | Canal El Bordo | 3 | 26 de octubre de 2021 | FCME_CM974-FCME_CM977 |
| Estado de México Mayorazgo | Presa Ignacio Ramírez | 4 | 16 de marzo de 2022 | FCME_EDM64-FCME_EDM65 |
| Hidalgo Entre Tepeji del Río de Ocampo y Tula de Allende | Presa Requena | 5 | 20 de marzo de 2023 | FCME_HGO090-FCME_HGO091 |
| Morelos Jojutla | Coatetelco | 6 | 26 de mayo de 2023 | FCME_MOR002 |
| Miacatlán | El Rodeo | 7 | 26 de mayo de 2023 | FCME_MOR003 |
| Tlaxcala Atlangatepec | Atlangatepec | 8 | 23 de junio de 2023 | FCME_TLX001-FCME_TLX002 |
Localidad 1: lago Huetzalín pertenece al Parque Ecológico Xochimilco (PEX), una zona de recuperación ubicada en Xochimilco con una superficie de 1.9 km2 (Tavera et al., 2018). Localidad 2: la Cantera Oriente (CO) área rodeada por una pared de basalto (con una altura de hasta 40 m) que alberga varios cuerpos de agua con una superficie total de 11,906.45 m2 (Lot, 2007), perteneciente a la Reserva Ecológica del Pedregal de San Ángel. Localidad 3: el canal El Bordo es uno de los componentes de la zona chinampera de Xochimilco establecida como área natural protegida desde 1992, inscrita en la lista de humedales de importancia internacional por la Convención Internacional sobre Humedales Ramsar en 2004 (Figueroa et al., 2015). Localidad 4: presa Ignacio Ramírez (municipio Mayorazgo, Estado de México) es el acuífero más importante de la zona pues cuenta con disponibilidad de agua subterránea. Localidad 5: presa Requena (Hidalgo) es indispensable para la regulación de los escurrimientos del río Tula (Ríos, 2009), además de que está contemplada en el programa de ordenamiento ecológico local del municipio de Tepeji del Río de Ocampo desde 2004 (Valdez, 2012). Localidad 6: lago Coatetelco recibe aportes de arroyos del municipio Miacatlán, es un espacio de gran importancia social y económica (Macedonio, 2024). Los lagos Coatetelco y El Rodeo (localidad 7) representan los principales recursos hídricos del estado de Morelos. Ambos están dentro del programa de ordenamiento ecológico con el objetivo de restaurar las funciones ecológicas del sitio y disminuir acciones antropogénicas (Conabio, 2020). Localidad 8: lago Atlangatepec, representa un recurso relevante dentro de su territorio, en Tlaxcala, pues es el más grande y es alimentado por el río Zahuapan, el cual representa un riesgo por la contaminación que presenta por la descarga de material urbano e industrial (López-Segovia et al., 2024).
En cada sitio se filtraron 10 L de agua con una red de fitoplancton (10 µm), este material se concentró en 250 mL y una alícuota de 20 mL se guardó como muestra de herbario y en otro frasco de 200 mL como material de cultivo y observación. El frasco de cultivo se mantuvo en hielo hasta llegar al laboratorio y observar el material vivo. El frasco que se incorporó a las muestras de herbario (FCME) se preservó usando formaldehído al 2.5%. Se tomaron datos de las variables fisicoquímicas: radiación fotosintéticamente activa (PAR, sensores HOBO Penclant Couple MR), temperatura, pH, conductividad, oxígeno disuelto y clorofila a con una sonda multiparamétrica (Hydrolab DS 5 MR).
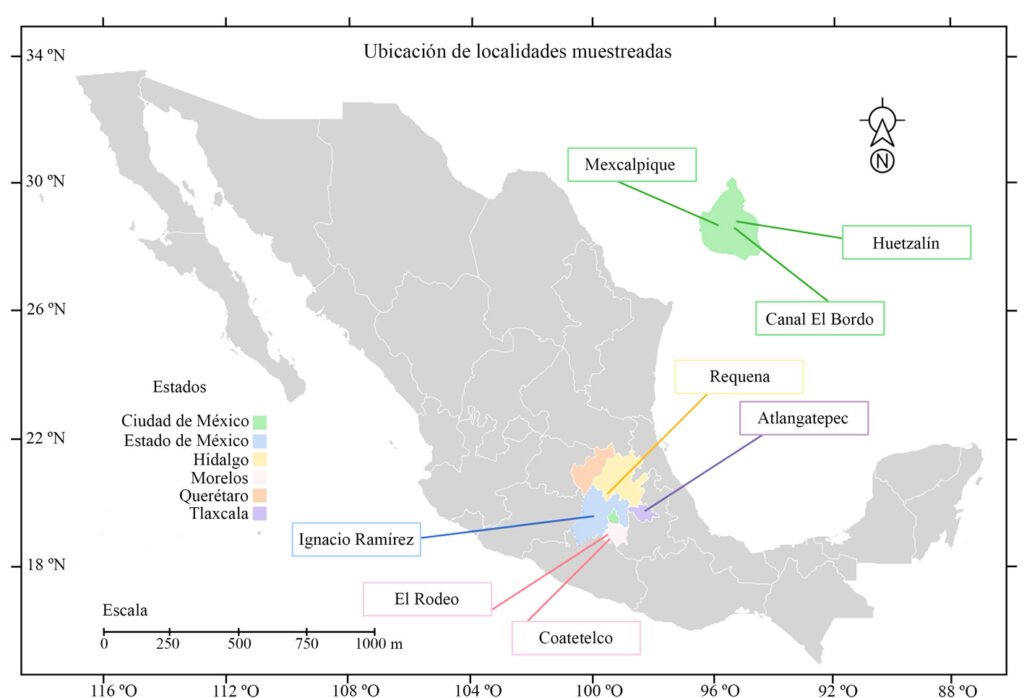
Figura 2. Ubicación de los lagos que se muestrearon en este estudio (Google Earth, 2025).
El cultivo de las especies se realizó en 2 medios de cultivo líquido: bold basal y bristol. El material filtrado se revisó y al identificar especies de interés se continuó con el aislamiento de ejemplares usando un capilar y material de succión. Los cultivos se ubicaron en condiciones de luz y oscuridad (16:8), con un promedio de 3,150 luxes y un intervalo de temperatura de 17-32 °C. Una parte del material de cultivo se procesó para fotografiarlo con microscopía electrónica de barrido. El procedimiento que se realizó usando glutaraldehído fue siguiendo a Takano y Hiroguchi (2005) para su observación. Los equipos utilizados fueron: Jeol JSM-5310LV y Hitachi SU1510.
Se realizaron preparaciones semipermanentes usando el material fijado (2.5%) y gelatina glicerinada (González-González y Novelo, 1986). La observación del material se realizó en un microscopio con contraste interdiferencial (Nikon 80i), para confirmar algunos caracteres morfológicos. Las fotografías se tomaron con una cámara Jenoptik adecuada al microscopio. Las fotografías y láminas se editaron para mejorar el contraste con el programa Photoshop (Adobe Photoshop [versión 26.8.1, 2025]).
En la identificación de las especies, las principales fuentes de consulta fueron: Bourrelly (1952, 1981), Ettl (1978), Ettl y Gärtner (1995); John et al. (2002), Pascher et al. (1925) y Starmach (1968). Y de manera particular se usaron: Bicudo et al. (2006: Characiopsis anabaenae, Chloridella cystiformis, Goniochloris mutica, Isthmochloron lobulatum, Pseudopolyedriopsis skujae, Tribonema minus); Hollerbach (1962: Pseudopolydriopsis skujae); Islam e Irfanullah (2001: Tetraplektron torsum); Krienitz et al. (1993: Pseudogoniochloris tripus); Krienitz et al. (2000: Nannochloropsis limnetica); Novelo et al. (2009: Botrydiopsis arhiza y Chloridella cystiformis).
Los datos de distribución geográfica y ambiental se obtuvieron de bdLACET (Novelo y Tavera, 2025), AlgaeBase (Guiry y Guiry 2025) y GBIF (Global Biodiversity Information Facility, 2025). El análisis de similitud con el índice de Jaccard se realizó con el programa PAST versión 4.17 (Hammer et al., 2001), construyendo una matriz de presencia y ausencia de las especies en los 8 sitios (con los parámetros establecidos en el programa). El análisis de agrupamiento (con distancia euclidiana, con el algoritmo UPGMA) se realizó utilizando los datos ambientales medidos en cada sitio de muestreo: temperatura (°C), pH, conductividad (µS), oxígeno disuelto (mg/L) y concentración de clorofila a (µg/L) (se realizó con los parámetros establecidos en el programa), los datos se transformaron con logaritmo base 10.
Resultados
Los datos de variables ambientales obtenidos en campo de los 8 lagos se presentan en la tabla 2, así como también la distribución de las especies por sitio y registro previos en México. El análisis de similitud con el índice de Jaccard se muestra en la tabla 3. Los valores obtenidos nos indican valores bajos de similitud en relación con las especies distribuidas en los sitios. Los valores obtenidos están en un intervalo de 0 a 0.33.
El agrupamiento de los sitios se representa en la figura 3. Los grupos que se formaron en el análisis son 3. El primer grupo (con los sitios más cercanos) es el que se representa con los números 2, 4 y 8, que corresponden a los sitios Mexcalpique (2), presa Ignacio Ramírez (4) y Atlangatepec (8); el siguiente grupo, con los sitios 1 (Huetzalín) y 7 (El Rodeo), y el último grupo con los sitios 5 (presa Requena), 6 (Coatetelco) y 3 (Bordo). En las muestras se identificaron en total 18 especies en la región central de México y corresponden a las 2 clases, de acuerdo con bases de datos actualizadas (bdLACET y AlgaeBase), 10 de ellas se clasifican en la clase Xanthophyceae y 8 en la clase Eustigmatophyceae.
Xanthophyceae P. Allorge ex F.E. Fritsch
Rhizochloridales Pascher
Stipitococcaceae Ettl
Stipitococcus W. et G. S. West
Stipitococcus capensis Prescott, 1937 (fig. 4)
Células solitarias, lorica con forma elipsoidal-ovoide ligeramente alargada, en la base presenta un pedúnculo corto que se adhiere a otras algas (encontradas sobre células de Stephanocyclus meneghinianus). Célula elipsoidal con un plastidio lobulado. Las células miden 7.8-9.7 µm de largo y 4.0-6.3 µm de ancho, con un pedúnculo corto de hasta 2.0 µm.
Distribución en México: Oaxaca, Ciudad de México (Xochimilco). Mundial: España, EUA e India.
Ambientes: estanques, lagos.
Formas de vida: planctónica, epífita y metafítica.
Referencias: Bourrelly, 1981; Ettl, 1978; Pascher et al., 1925; Starmach, 1968.
Tabla 2
Valores de variables fisicoquímicas obtenidos en campo en los 8 sitios de muestreo: 1) Huetzalín – PEX; 2) Mexcalpique – Cantera Oriente; 3) canal El Bordo – Xochimilco; 4) presa Ignacio Ramírez; 5) presa Requena; 6) Coatetelco; 7) El Rodeo; 8) Atlangatepec.
| Variable y especie/ sitio | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | Distribución en México |
| Temperatura (°C) | 24 | 16.4 | 15.4 | 24 | 19.4 | 32.8 | 29.9 | 26.1 | |
| pH | 8.7 | 8.1 | 6.9 | 9.1 | 9.5 | 8 | 8.3 | 9.2 | |
| Conductividad (µS) | 0 | 364 | 932 | 291 | 826 | 878 | 168 | 401 | |
| DO (mg/L) | 6.19 | 7.12 | 0.22 | 10.6 | 5.26 | 5.06 | 5.78 | 8.25 | |
| Clorofila a (µg/L) | 0.96 | 59.05 | 3.75 | 29.94 | 6.94 | 6.31 | 41.1 | 26.97 | |
| Stipitococcus capensis | x | CdMx, Oaxaca | |||||||
| Chloridella cystiformis | x | x | CdMx, Tabasco | ||||||
| Ellipsoidion oocystoides | x | Nuevo Registro | |||||||
| Monodus guttula | x | Nuevo Registro | |||||||
| Tetraplektron torsum | x | Michoacán, Yucatán. | |||||||
| Pseudogoniochloris tripus | x | x | Tabasco, Nayarit. | ||||||
| Isthmochloron lobulatum | x | Tabasco, Nayarit. | |||||||
| Pseudopolydriopsis skujae | x | Nuevo registro | |||||||
| Botrydiopsis arhiza | x | Jalisco | |||||||
| Tribonema minus | x | x | CdMx | ||||||
| Nannochloropsis limnetica | x | Nuevo registro | |||||||
| Characiopsis anabaenae | x | Nuevo registro | |||||||
| Goniochloris mutica | x | x | x | CdMx, Tabasco, Nayarit. | |||||
| G. iyengarii | x | x | x | Tabasco | |||||
| Pseudostaurastrum limneticum | x | Estado de México | |||||||
| Tetraedriella acuta | x | Tabasco | |||||||
| Trachydiscus minutus | x | Tabasco | |||||||
| T. lenticularis | x | Nuevo registro |
Tabla 3
Valores de similitud (índice de Jaccard).
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | |
| 1 | 1 | 0.16666667 | 0.14285714 | 0 | 0 | 0 | 0 | 0.14285714 |
| 2 | 0.16666667 | 1 | 0 | 0 | 0 | 0.14285714 | 0 | 0 |
| 3 | 0.14285714 | 0 | 1 | 0 | 0 | 0.125 | 0 | 0.33333333 |
| 4 | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 0 |
| 5 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 0 |
| 6 | 0 | 0.14285714 | 0.125 | 0 | 0 | 1 | 0 | 0.125 |
| 7 | 0 | 0 | 0 | 0 | 0 | 0 | 1 | 0 |
| 8 | 0.14285714 | 0 | 0.33333333 | 0 | 0 | 0.125 | 0 | 1 |
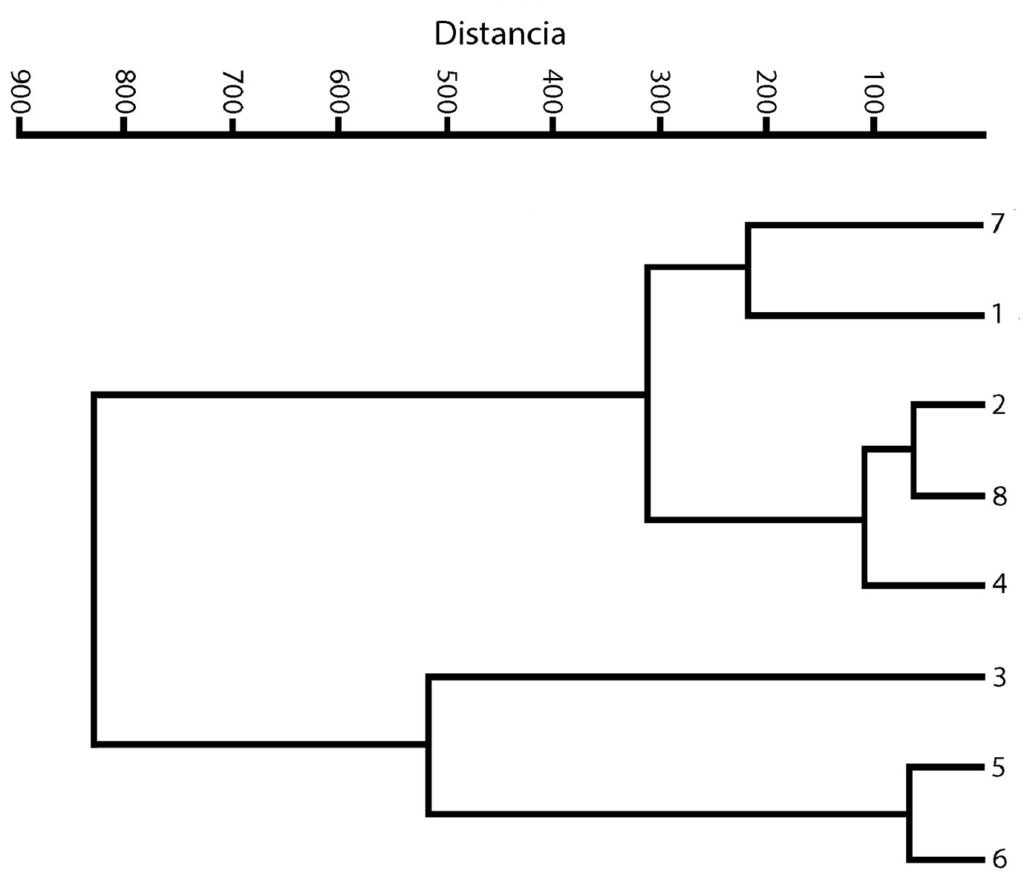
Figura 3. Dendrograma. Agrupamiento de los 8 sitios recolectados.
Mischococcales F.E. Fritsch
Pleurochloridaceae Pascher
Género Chloridella Pascher
Chloridella cystiformis Pascher, 1937 (figs. 5, 6)
Células solitarias, generalmente esféricas con pared lisa a veces amarillenta y gruesa, 2-4 plastidios discoidales, parietales. Las células miden 4.8-9.3 µm de diámetro.
Distribución en México: Ciudad de México (Cantera Oriente, PEX), Tabasco. Mundial: Alemania, Brasil, España, Eslovaquia, EUA, Polonia, República Checa, Rusia y Ucrania.
Ambientes: estanques y lagos.
Forma de vida: metafítica.
Referencias: Bicudo et al., 2006; Bourrelly, 1981; Ettl, 1978; Novelo et al., 2009; Pascher et al., 1925.
Nota: se encuentra en grandes cantidades en cuerpos de agua con un alto contenido de hierro y valores ácidos de pH (Ettl, 1978).
Ellipsoidion Pascher
Ellipsoidion oocystoides Pascher, 1938 (figs. 7, 8)
Células elipsoidales con extremos redondeados, generalmente 1.5 veces más largas que anchas, pared celular lisa, un plastidio laminar parietal. Las células miden 5.8-6.5 µm de largo y 2.9-3.8 µm de ancho.
Distribución en México: primer registro en Estado de México (presa Ignacio Ramírez) y México. Mundial: Alemania, Australia, Austria, Brasil, Corea del Norte, Eslovaquia, España, Islandia, Japón, República Checa, Rumania, Rusia y Tayikistán.
Ambientes: lagos y suelos.
Formas de vida: metafítica, edáfica.
Nota: común en aguas y suelos ácidos (Ettl, 1978).
Referencias: Bourrelly 1981; Ettl, 1978; Starmach, 1968.

Figuras 4-9. 4, Stipitococcus capensis; 5, Chloridella cystiformis; 6, C. cystiformis (MEB); 7, Ellipsoidion oocystoides; 8, E. oocystoides (MEB); 9, Monodus guttula (cultivo). Barra = 10 µm.
Monodus Chodat
Monodus guttula Pascher, 1938 (figs. 9-11)
Células solitarias globosas u ovadas, puntiagudas en un extremo, ligeramente curvas, pared lisa y delgada, un plastidio laminar parietal. Las células miden 3.8-4.9 µm de largo y 2.2-2.9 µm de ancho.
Distribución en México: primer registro en Ciudad de México (Cantera Oriente). Mundial: Alemania, Bulgaria, Eslovaquia, España, Islas Shetland del Sur, Moldavia, República Checa, Rumania y Rusia.
Ambientes: lagos.
Formas de vida: metafítica.
Nota: se encuentran en lugares húmedos y zanjas en las cordilleras entre Alemania y la República Checa (Ettl, 1978).
Referencia: Bourrelly, 1981; Ettl, 1978; Pascher et al., 1925, Starmach, 1968.
Tetraplektron Fott
Tetraplektron torsum (Turner) Dedusenko Ščegoleva, 1962 (fig. 12)
Células solitarias, tetraédricas aplanadas, cada lado termina en una espina, un lado enmascara otro, pared celular lisa y gruesa, varios plastidios discoidales. Las células miden 44.2- 46.6 µm de largo y 22.1-22.9 µm de ancho.
Distribución en México: Morelos (El Rodeo), Michoacán y Yucatán. Mundial: Alemania, Australia, Bangladesh, Brasil, Costa de Marfil, EUA, Italia, Myanmar, Países Bajos, Paraguay, Suecia y Ucrania.
Ambientes: lagos.
Formas de vida: Planctónica, perifítica y metafítica.
Referencias: Bourrelly, 1981; Ettl, 1978; Islam e Irfanullah, 2001; John et al., 2002; Starmach, 1968.
Pseudogoniochloris (Pascher) Krienitz, Hegewald, Reymond et Peschke
Pseudogoniochloris tripus (Pascher) Krienitz, Hegewald, Reymonds et Peschke, 1993 (fig. 13).
Células triangulares irregulares (ligeramente torcidas) con bordes agudos, lados cóncavos, pared celular lisa o ligeramente ornamentada, 3-5 plastidios (puede haber más) discoidales, parietales. Las células miden 19.5-28.3 µm por lado.
Distribución en México: Ciudad de México (Xochimilco), Tlaxcala (Atlangatepec), Tabasco y Nayarit. Mundial: Alemania, Argentina, Australia, Austria, Bangladesh, Bélgica, Bielorrusia, Botsuana, Brasil, China, Eslovaquia, EUA, Estonia, Francia, India, Irlanda, Israel, Japón, Países Bajos, Paraguay, Reino Unido, República Checa, Rumania, Rusia, Suecia, Sudáfrica, Turquía y Ucrania.
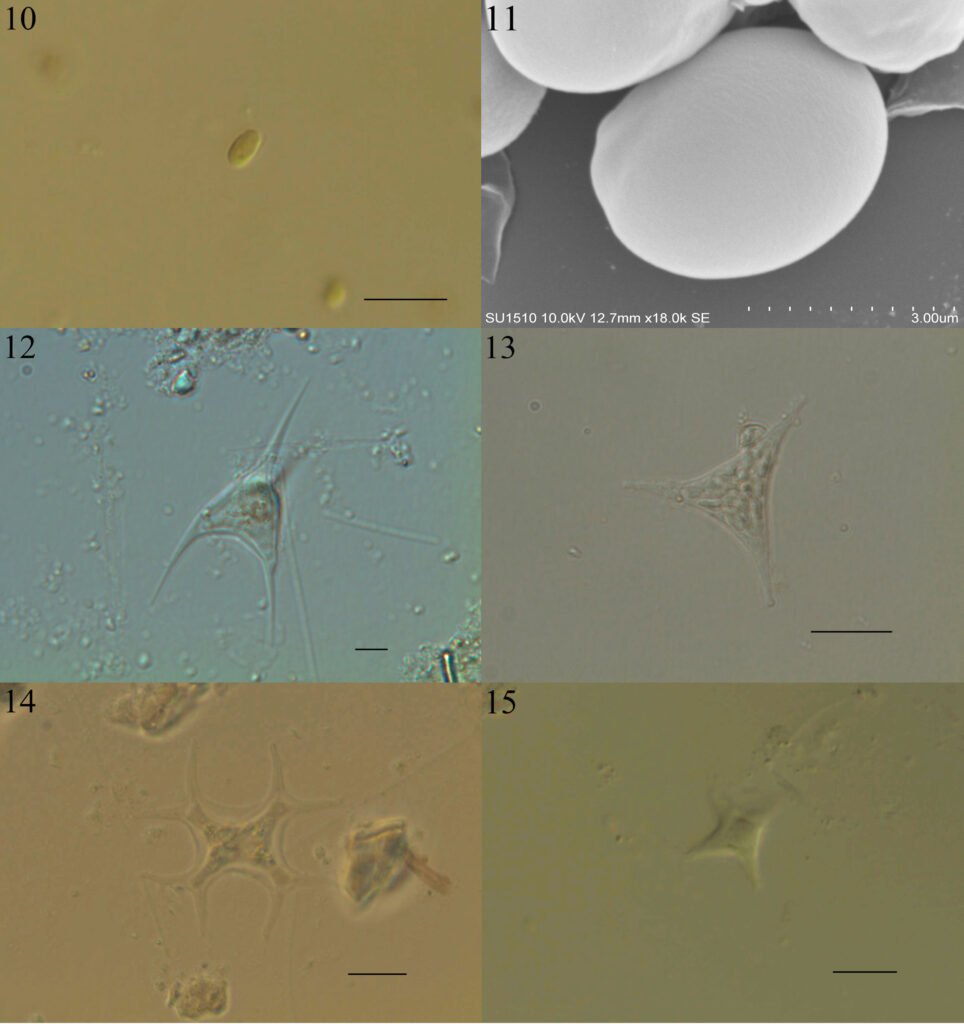
Figuras 10-15. 10, Monodus guttula (campo); 11, M. guttula (MEB); 12, Tetraplektron torsum; 13, Pseudogoniochloris tripus; 14: Isthmochloron lobulatum; 15, Pseudopolyedriopsis skujae. Barra = 10 µm.
Ambientes: lagos.
Formas de vida: planctónica y metafítica.
Referencias: Bicudo et al., 2006; Bourrelly 1952, 1981; Ettl, 1978; Krienitz et al., 1993; Starmach, 1968.
Isthmochloron Skuja
Isthmochloron lobulatum (Nägeli) Skuja, 1948 (fig. 14)
Células solitarias, cuadrangulares con lados cóncavos que se dividen dicotómicamente al final, pared celular lisa, varios plastidios discoidales, parietales. Las células miden 7.8-11.7 en la parte central, sin brazos y miden 28.2-34.7 µm de cada lado con brazos.
Distribución en México: Morelos (Coatetelco), Tabasco y Nayarit. Mundial: en los 5 continentes.
Ambientes: lagos.
Formas de vida: metafítica y planctónica.
Referencias: Bicudo et al., 2006; Bourrelly 1952, 1981; Ettl, 1978; John et al., 2002; Starmach, 1968.
Pseudopolyedriopsis Gollerbach
Pseudopolyedriopsis skujae Gollerbach, 1962 (fig. 15)
Células solitarias, aplanadas con 5 proyecciones angulosas, pared celular gruesa, ornamentación muy fina, varios plastidios discoidales parietales. Las células miden 9.3-17.1 µm de cada lado. Presentan 2-4 espinas de 13.2-18.6 µm en cada proyección.
Distribución en México: primer registro en México, Ciudad de México (Xochimilco). Mundial: Alemania, Australia, Bélgica, Bielorrusia, Brasil, EUA, Estonia, Francia, Países Bajos y Suecia.
Ambientes: lagos.
Formas de vida: metafítica.
Nota: los ejemplares observados sólo presentan espinas en campo, no en los cultivos.
Referencias: Bicudo et al., 2006; Bourrelly, 1981; Ettl, 1978; Hollerbach, 1962; Starmach, 1968.
Botrydiopsidaceae D.J. Hibberd
Botrydiopsis Borzì
Botrydiopsis arhiza Borzì, 1895 (figs. 16-18)
Células esféricas, generalmente en grupos unidos por mucílago incoloro o pardo, pared celular gruesa a muy gruesa, varios plastidios discoidales o rectangulares. Las células miden 13.6-23.5 µm de diámetro.
Distribución en México: Ciudad de México (Cantera Oriente), Jalisco. Mundial: EUA, Japón, India, Países Bajos, Portugal, Reino Unido, Rusia, Suecia y Ucrania.
Ambientes: suelos, lagos, arenas y charcos.
Formas de vida: edáfica, planctónica y metafítica.
Referencias: Bourrelly, 1981; Ettl, 1978; John et al., 2002; Novelo et al., 2009; Pascher et al., 1925; Starmach, 1968.
Tribonematales Pascher
Tribonemataceae Pascher
Tribonema Derbès et Solier
Tribonema minus Wille (Hazen), 1902 (fig. 19)
Filamentos uniseriados, cortos, rectos o curvos. Células cilíndricas con septos definidos y sin constricción, pared celular lisa, 2 a 3 plastidios laminares, parietales. Las células miden 4.4-5.9 µm de ancho y 17.5-26.3 µm de largo.
Distribución en México: Ciudad de México (Cantera Oriente). Mundial: Alemania, Arabia Saudita, Austria, Brasil, Canadá, España, EUA, Estonia, Grecia, Hungría, Nigeria, Países Bajos, Polonia, Reino Unido, Suecia, Ucrania y Uzbekistán.
Ambientes: ríos, arroyos, lagos, humedales, charcos, estanques, embalses y turberas.
Formas de vida: bentónica, metafítica, planctónica.
Referencias: Bicudo et al., 2006; Bourrelly, 1981; Ettl, 1978; Ettl y Gärtner, 1995; John et al., 2002; Starmach, 1968.
Eustigmatophyceae D.J. Hibberd et Leedale
Eustigmatales D.J. Hibberd
Monodopsidaceae D.J. Hibberd
Nannochloropsis D.J. Hibberd
Nannochloropsis limnetica Krienitz, Hepperle, Stich et Weiler, 2000 (figs. 20, 21)
Células esféricas, ovaladas o en forma de gota, pared celular lisa, 1-2 plastidios discoidales, parietales. Las células miden 3.1-3.4 µm de diámetro.
Distribución en México: Ciudad de México (Cantera Oriente). Mundial: Alemania, Canadá, China, Curazao, Dinamarca, Eslovenia, EUA, Finlandia, Francia, Grecia, Israel, Noruega, Polonia, Reino Unido, Rusia y Suecia.
Ambientes: lagos.
Forma de vida: metafítica.
Referencias: Krienitz et al., 2000.
Characiopsidaceae Pascher
Characiopsis Borzì
Characiopsis anabaenae Pascher, 1938 (figs. 22, 23)
Células solitarias, pequeñas, fusiformes, con un lado más convexo que el otro, terminación aguda de un extremo en donde se encuentra el disco basal, pared celular lisa, 2 plastidios laminares. Las células miden 10.7-18.6 µm de largo y 2.0-5.9 µm de ancho.
Distribución en México: primer registro en México, Hidalgo (Presa Requena). Mundial: Afganistán, Alemania, Brasil, Países Bajos, Portugal, Rumania, Rusia y Ucrania.
Ambientes: lagos.
Forma de vida: metafítica.
Referencias: Bicudo et al., 2006; Bourrelly, 1981; Ettl, 1978; Ettl y Gärtner, 1995; Starmach, 1968.
Goniochloridales K.P. Fawley, M. Eliás et M.W. Fawley
Goniochloridaceae
Goniochloris Pascher
Goniochloris mutica (A. Braun) Fott, 1960 (fig. 24)
Células solitarias, triangulares regulares con bordes redondeados, lados cóncavos, pared celular ornamentada con pequeñas verrugas, 2-3 plastidios discoidales. Las células miden 5.8-9.8 µm de cada lado.
Distribución en México: Ciudad de México (Xochimilco), Tlaxcala (Atlangatepec), Tabasco y Nayarit. Mundial: Alemania, Australia, Argentina, Bangladesh, Bélgica, Bielorrusia, Botswana, Brasil, Burindi, Canadá, China, Costa de Marfil, Eslovaquia, España, EUA, Estonia, Francia, India, Irak, Irán, Israel, Italia, Niger, Nueva Zelanda, Países Bajos, Portugal, Reino Unido, República Checa, Rumania, Rusia, Sudán, Suecia, Taiwán, Tayjikistán, Turquía y Ucrania.
Ambientes: humedales y lagos.
Formas de vida: planctónica y metafítica.
Referencias: Bicudo et al., 2006; Bourrelly 1952, 1981; Ettl, 1978; John et al., 2002; Starmach, 1968.
Goniochloris iyengarii (Ramanathan) Ettl, 1977 (fig. 25)
Células solitarias, triangulares con terminaciones agudas, lados ligeramente cóncavos, pared celular gruesa con ornamentación escrobiculada, varios plastidios discoidales, parietales. Las células miden 22.3-26.4 µm de cada lado.
Distribución en México: Ciudad de México (Xochimilco), Morelos (Coatetelco), Tlaxcala (Atlangatepec), Tabasco. Mundial: Alemania, Brasil, Francia (Guadaloupe), India y Países Bajos.
Ambientes: charcos y lagos.
Formas de vida: metafítica.
Referencias: Bourrelly 1981; Ettl, 1978; John et al., 2002; Starmach, 1968.
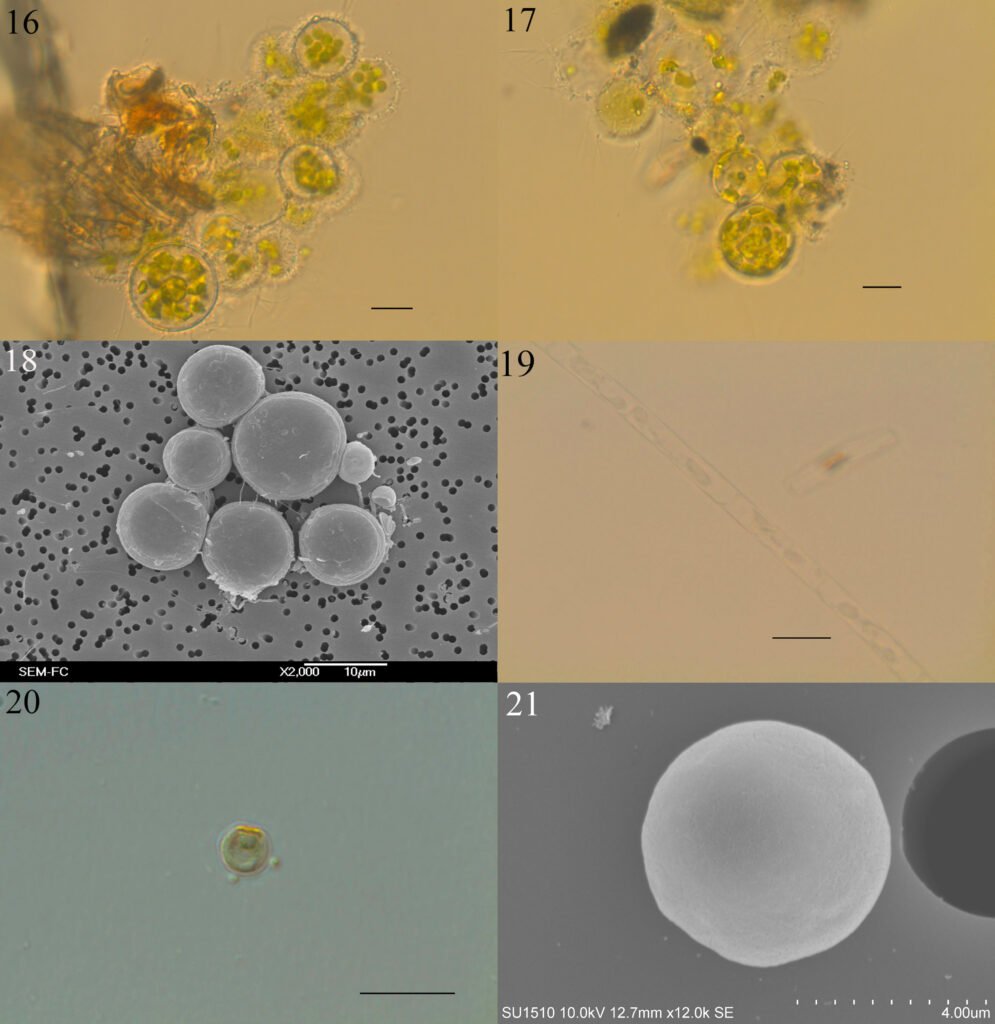
Figuras 16-21. 16, Botrydiopsis arhiza (campo); 17, B. arhiza (cultivo); 18, B. arhiza (MEB); 19, Tribonema minus; 20, Nannochloropsis limnetica; 21, N. limnetica (MEB). Barra = 10 µm.
Pseudostaurastrum Chodat
Pseudostaurastrum limneticum (Borge) Guiry, 2021 (fig. 26)
Células solitarias, tetraédricas con cuerpo central ligeramente amplio que termina en 4 brazos radiados, bifurcados en los extremos, pared celular lisa y gruesa, varios plastidios discoidales y parietales. Las células miden 29.3-34.9 µm de cada lado.
Distribución en México: Tlaxcala (Atlangatepec) y Estado de México. Mundial: Alemania, Argentina, Australia, Bangladesh, Bioelorrusia, Brasil, Canadá, China, Cuba, España, EUA, Estonia, India, Irak, Irlanda, Israel, Japón, Latvia, Mianmar, Nueva Zelanda, Países Bajos, Paquistán, Portugal, Reino Unido, República Checa, Rumania, Rusia, Sudán, Suecia, Taiwán, Turquía, Ucrania y Venezuela.
Ambientes: lagos.
Formas de vida: planctónica y metafítica.
Referencias: Bourrelly, 1981; Ettl, 1978; John et al., 2002; Starmach, 1968.
Tetraedriella Pascher
Tetraedriella acuta Pascher, 1930 (fig. 27)
Células solitarias, tetraédricas, con lados convexos y bordes ligeramente afilados, pared celular gruesa ornamentada en forma de panal con bordes aún más engrosados, 4 plastidios discoidales. Las células miden 10.3-13.7 µm de cada lado.
Distribución en México: Tabasco y Ciudad de México (Xochimilco). Mundial: Alemania, Brasil, Bulgaria, Costa de Marfil, España, Estonia, Francia, Países Bajos y República Checa.

Figuras 22-27. 22, Characiopsis anabaenae; 23, C. anabaenae (MEB); 24, Goniochloris mutica, 25; G. iyengarii, 26; Pseudostaurastrum limneticum, 27; Tetraedriella acuta. Barra = 10 µm.
Ambientes: lagos.
Formas de vida: metafítica.
Nota: valores ácidos de pH (Ettl, 1978).
Referencias; Bourrelly, 1981; Ettl, 1978; Starmach, 1968.
Trachydiscus Ettl
Trachydiscus minutus (Bourrelly) Ettl, 1964 (fig. 28)
Células solitarias, pentagonales redondeadas en los ángulos, pared celular delicadamente ornamentada, 4 a 5 plastidios discoidales. Las células miden 6.8-9.8 µm de diámetro.
Distribución en México: Tlaxcala (Atlangatepec) y Tabasco. Mundial: Argentina, Australia, Bélgica, Bulgaria, Canadá, China, Colombia, Corea del Sur, EUA, Finlandia, Francia, Grecia, Polonia, Reino Unido, República Checa, Suecia, Turquía y Ucrania.
Ambientes: estanques, lagos.
Formas de vida: planctónica, metafítica.
Referencias: Bourrelly 1952, 1981; Ettl, 1978; Starmach, 1968.
Trachydiscus lenticularis Ettl, 1964 (fig. 29)
Células solitarias, lenticulares, biconvexas, pared celular ornamentada con verrugas pequeñas, 3 plastos discoidales. Las células miden 8.6-9.8 µm de diámetro.
Distribución en México: primer registro en México, Tlaxcala (Atlangatepec). Mundial: Alemania, Bélgica, España, Francia, Irlanda, Países Bajos, República Checa y Reino Unido.
Ambientes: estanques, lagos.
Formas de vida: planctónica, metafítica.
Referencias: Bourrelly 1952, 1981; Ettl, 1978; Starmach, 1968.
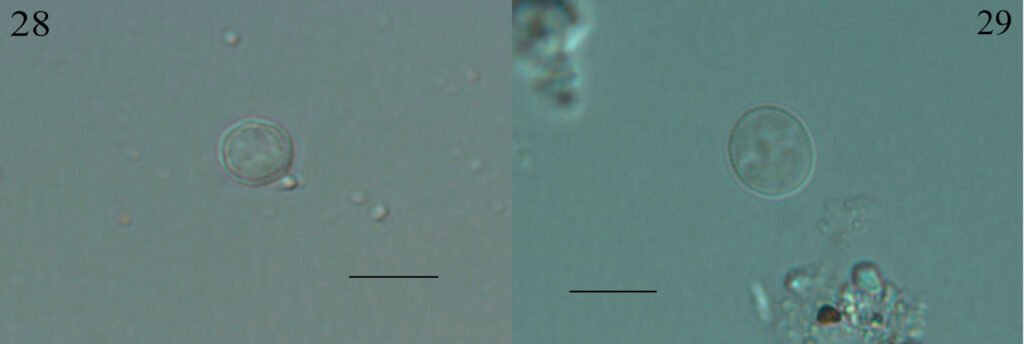
Figuras 28-29. 28, Trachydiscus minutus; 29, T. lenticularis. Barra = 10 µm.
Discusión
Los registros previos de especies de las Xanthophyceae y Eustigmatophyceae en los sitios seleccionados de la región central de México se muestran en la tabla 4. En la Ciudad de México, de las 8 especies registradas, confirmamos la presencia actual de 3 de ellas, Botrydiopsis arhiza, Chloridella cystiformis y Tribonema minus. B. arhiza ha sido reportada en 3 trabajos, el primero, en el catálogo de algas de Ortega (1984); el segundo, como un taxón a comparar que se encuentra por periodos en distintos cuerpos de agua siendo parte de distintas comunidades: fitoplancton, metafiton y perifiton (Novelo et al., 2009); nosotros la encontramos en un cuerpo de agua estancado dentro de la Cantera Oriente, en octubre, formando un crecimiento evidente en la superficie casi monoespecífico de fitoplancton; el tercer registro, menciona la especie como parte de las algas de la cuenca de la ciudad (Figueroa, 2009). Previamente registrada en EUA, varios países de Europa, Rusia, Japón e India.
C. cystiformis fue registrada por primera vez en la Cantera Oriente como una especie de ambientes templados y ácidos (Novelo et al., 2009); en este trabajo se registra en el mismo sitio, lago Mexcalpique, en el metafiton, corroborando su presencia y crecimiento en la misma comunidad, sin embargo, las condiciones no son similares pues los valores de pH no son ácidos (como se ha registrado previamente en localidades de Europa), sino básicos en el sitio donde la observamos (tabla 2), además también la encontramos en el lago Huetzalín (PEX) y en sitios con valores de pH básico.
En el caso de T. minus, se ha reportado en más ocasiones, ejemplo de la desigualdad de trabajos que registran especies de mayor talla, en este caso filamentosas que especies unicelulares, en canales de Xochimilco (Figueroa, 2009; Figueroa et al., 2015; Flores, 1980; González-Barrera, 1991) y en Cantera Oriente (Ponce et al., 2019). Esta especie ha sido registrada previamente en localidades frías de Europa, pero también en templadas o cálidas como EUA y Brasil.
Como nuevos registros de la Ciudad de México se tienen a Monodus guttula y Pseudopolydriopsis skujae. La primera descrita para el lago Mexcalpique en la Cantera Oriente, con registros previos en Europa y la segunda para el canal El Bordo en Xochimilco, presente en Europa y en Brasil. Por último, algunos registros que no estaban reportados en las zonas seleccionadas, pero sí en el país son: Stipitococcus capensis, en el Bordo, en Xochimilco, con registros en Europa, Norteamérica y Asia, en México se había descrito en Oaxaca. Pseudogoniochloris tripus, previamente registrado en Tabasco (Agredano, 2019; Mireles, 2019; Pedraza, 2020) y Nayarit (Ochoa, 2023), de amplia distribución mundial, se encontró en el canal Bordo; Nannochloropsis limnetica, se registra en el lago Mexcalpique, es una especie que ha proliferado en muchos ambientes en el mundo, ahora como primer registro en Cantera Oriente. En el lago Huetzalín, se observaron en el metafiton a Goniochloris mutica, con registros previos en los canales de Xochimilco (Tavera y Diez, 2009), Tabasco (Mireles, 2019) y Nayarit (Ochoa, 2023) y amplia distribución mundial; así como a G. iyengarii con registro anterior en Tabasco (Mireles, 2019) y con poca distribución mundial; y a Tetraedriella acuta, con registro previo en Tabasco (Mireles, 2019), en Europa y Brasil.
Tabla 4
Especies registradas previamente en las zonas de la región central de México.
| Estado (número de especies registradas) | Especie | Referencias |
| CdMx (8) | Botrydiopsis arhiza Borzì | Ortega, 1984 Novelo et al., 2009 Figueroa, 2009 |
| Characiopsis naegelii (A. Braun) Lemmermann | Ortega, 1984, Figueroa, 2009 | |
| Tabla 4. Continúa | ||
| Estado (número de especies registradas) | Especie | Referencias |
| Chloridella cystiformis Pascher | Novelo et al., 2009 | |
| Dichotomosiphon tuberosus (A. Braun) Ernest | Figueroa, 2009 Cantoral et al., 1999 | |
| Ducelleria chodatii (Ducellier) Teiling | Godínez-Ortega et al., 2017 | |
| Gloeobotrys limneticus (G.M. Smith) Pascher | Ortega, 1984 Figueroa, 2009 | |
| Ophiocytium capitatum Wolle | Figueroa et al., 2015 Figueroa, 2009 Flores-Granados, 1980 | |
| Tribonema minus (Wille) Hazen | Figueroa, 2009 Flores-Granados, 1980 González-Barrera, 1991 Figueroa et al., 2015 Ponce et al., 2019 | |
| Estado de México (10) | Bumilleriopsis brevis (Gerenck) Printz | Moreno y Palacios, 1987 |
| Characiopsis longipes (Rabenhorst) Borzì | Banderas-Tarabay, 1994 Banderas-Tarabay, 1997 | |
| Chlorocloster pyreniger Pascher | Favari et al., 2002 | |
| Ophiocytium capitatum Wolle | Chávez et al., 2005 | |
| O. cochleare (Eichwald) A. Braun | Mendoza, 1985 Ortega, 1984 Chávez et al., 2005 Figueroa, 2009 | |
| O. lagerheimii Lemmermann | Chávez et al., 2005 | |
| O. majus Nägeli | Chávez et al., 2005 | |
| O. parvulum (Perty) A. Braun | Zariñana-Leguízamo, 1997 Chávez et al., 2005 | |
| Vaucheria bursata (O.F. Müller) C. Agardh | Bojorge et al., 2010 Ramírez, 2010 Rodríguez-Flores, 2014 Rodríguez-Flores y Carmona, 2018 | |
| V. geminata (Vaucher) de Candolle | Ortega, 1984 Mendoza, 1985 Figueroa, 2009 Garduño-Solórzano et al., 2009 Ceballos et al., 2009 | |
| Morelos (3) | Ophiocytium capitatum Wolle | Flórez, 2011 |
| Tribonema bombycinum (C.A. Agardh) Derbés et Solier | García-Rodríguez y Tavera, 1998 Quiroz-Castelán et al., 2007 García-Rodríguez, 2004 | |
| Vaucheria sessilis f. clavata (De Candolle) Heering | Valadez-Cruz et al., 1996 Valadez-Cruz, 1998 | |
| Ducelleria chodatii (Ducellier) Teiling | Godínez-Ortega et al., 2017 |
De los registros en el Estado de México (10) no corroboramos ninguna de las especies de la tabla 4. Favari et al. (2002) reportan para la presa Ignacio Ramírez a Chlorocloster pyreniger, en este estudio con la observación de material de campo tanto vivo como fijado, no se corroboró su presencia. En el caso de Ellipsoidion oocystoides, se registra por primera vez en el país, con reportes previos en zona templada de Europa, Japón y zonas tropicales como Brasil, Australia y Nueva Zelanda.
Para la presa Requena, Hidalgo, no existían registros publicados sobre este grupo de algas, en la revisión de las muestras de este estudio encontramos a Characiopsis anabaenae, primer registro para México, previamente descrito en Europa, Asia y Brasil.
En Morelos, los 4 registros previos de algas doradas no se corroboraron, incluso en el sitio que visitamos, El Rodeo. En el lago Coatetelco identificamos Goniochloris mutica (mencionada para Huetzalín) e Isthmochloron lobulatum que ya tenía registros previos en Tabasco (Mireles, 2019) y Nayarit (Ochoa, 2023) y con amplia distribución mundial. En el lago El Rodeo, también identificamos a I. lobulatum y Tetraplektron torsum, esta última se había registrado en Michoacán (Martínez, 2016) y Yucatán (López-Adrián y Catzim, 2010), en parte de Europa, Sudamérica y Asia. Pseudostaurastrum limneticum, previamente registrada en el Estado de México (Jiménez, 2010) y con amplia distribución mundial.
En Tlaxcala, en el lago Atlangatepec, identificamos 6 especies: Pseudogoniochloris tripus, Goniochloris mutica, G. iyengarii, Pseudostaurastrum limneticum, Trachydiscus minutus y T. lenticularis. T. minutus, con registro previo en Tabasco (Pedraza, 2020), Europa y Argentina, muy escasos son los trabajos con esta especie. Mientras, que T. lenticularis, es primer registro en México y solo se ha reportado en ambientes fríos de Europa, Alemania, Bélgica, España, Francia, Irlanda, Países Bajos, República Checa y Reino Unido (Ettl, 1978; Starmach, 1968).
En relación con los sitios de muestreo y las variables ambientales, el dendrograma obtenido muestra que los sitios más parecidos son: Mexcalpique, presa Ignacio Ramírez y Atlangatepec (localidades 2, 4 y 8, respectivamente), esto resulta así pues los valores ambientales son cercanos en 3 variables, conductividad, oxígeno disuelto y concentración de clorofila a. Los sitios: Huetzalín y El Rodeo (1 y 7, respectivamente) presentan valores cercanos de pH y de oxígeno disuelto. Finalmente, el último grupo, Bordo, presa Requena y Coatetelco (3, 5 y 6 respectivamente), presentan valores cercanos de conductividad y de concentración de clorofila a.
La distribución de las especies utilizando una matriz de presencia/ausencia y aplicando el índice de Jaccard, dio como resultado valores entre 0 y 0.33, estos valores indican una similitud de especies nula o baja entre los sitios (Magurran, 2004). Huetzalín (1) muestra valores 0 con la presa Ignacio Ramírez (4), Presa Requena (5), Coatetelco (6) y El Rodeo (7), un valor de 0.14286 con los lagos El Bordo (3) y Atlangatepec (8) y un valor de 0.167 con Mexcalpique, esto indica una similitud bastante baja, pues solo comparten una especie (Goniochloris mutica) y la mayoría de las especies son diferentes entre sitios. Los valores 0, nos indican que los elementos son 100% diferentes, mientras que en los otros sitios son casi 90% diferentes. Los sitios que muestran los valores más altos (0.334) son El Bordo (3) y Atlangatepec (8), esto es debido a que comparten la presencia de 3 especies (Pseudogoniochloris tripus, Goniochloris mutica y Goniochloris iyengarii). La presencia de especies en cada sitio prácticamente es única, esto se explica por la variación en las condiciones ambientales que pueden limitar el crecimiento de algunas especies y la distancia entre los sitios es lo suficiente para no compartir especies (Magurran, 2004).
Se esperaba que los grupos que se formaron en el dendrograma coincidieran con los sitios con más similitud con la presencia de especies, sin embargo, no ocurrió, lo que nos indica que son conjuntos casi únicos (Real y Vargas, 1996).
Todas las algas son un reto en su identificación, las algas doradas presentadas en este trabajo son un ejemplo de la diversidad que aún desconocemos en distintos sitios del país, seguir estudiando la flora dorada es indispensable en el avance de una solución taxonómica, en un contexto integral.
Agradecimientos
Al Posgrado en Ciencias del Mar y Limnología, UNAM, por los estudios dirigidos a la obtención del grado de Doctor. Al apoyo recibido de Conahcyt (beca con clave 2020-000026-02NACF). A Guadalupe Vidal Gaona por su apoyo en el laboratorio y en campo. A Beatriz Lira Hernández por su apoyo en campo. A Silvia Espinosa Matías de la Facultad de Ciencias por el procesamiento de muestras y obtención de imágenes con el microscopio electrónico de barrido Jeol JSM-5310LV. A María Berenit Mendoza Garfias del Laboratorio Nacional de Biodiversidad del Instituto de Biología por su servicio en el procesamiento de muestra y obtención de imágenes con el microscopio electrónico de barrido Hitachi SU1510. A los revisores, que nos dieron sugerencias para mejorar el manuscrito.
Referencias
Adrián-Serrano, J. (2024). Estudio de la biodiversidad fitoplanctónica del Canal Japón, Xochimilco, México D. F. (Tesis). Facultad de Ciencias, Universidad Nacional Autónoma de México. Ciudad de México.
Agredano, Z. O. (2019). Ficoflora de la laguna El Camarón en Villahermosa, Tabasco, México (Tesis). Facultad de Ciencias, Universidad Nacional Autónoma de México. Ciudad de México.
Aguirre-Cavazos, D. E., Moreno-Limón, S. y Salcedo-Martínez, S. M. (2018). Especies de algas de ríos de Nuevo León, México. Nuevos registros para el estado. Polibotánica, 46, 1–25. https://doi.org/10.18387/polibotanica.46.1
Alcocer, J. y Escobar-Briones, E. (1992). The aquatic biota of the now extinct lacustrine complex of Mexico basin. Freshwater forum, 2, 171–183.
Alvarado-Villanueva, R. (2003). Dinámica estacional y circadiana del fitoplancton en el Lago Zirahuén, Michoacán, México (Tesis de maestría). Facultad de Biología, Universidad Michoacana de San Nicolás de Hidalgo. Morelia.
Amateco-Rivero, F. S. (2011). Composición del fitoplancton del lago de Catemaco, Veracruz, México (Tesis). Facultad de Estudios Superiores Iztacala, Universidad Nacional Autónoma de México. Estado de México.
Banderas-Tarabay, A. G. (1994). Limnología del lago El Sol, Nevado de Toluca, México (Tesis doctoral). Facultad de Ciencias, Universidad Nacional Autónoma de México. México D.F.
Banderas-Tarabay, A. G. (1997). Phycoflora of the tropical high-mountain lake El Sol, Central Mexico, and some biogeographical relationships. Hydrobiologia, 354, 17–40. https://doi.org/10.1023/A:1003082500767
Bicudo, D. C., Bicudo, C. E. M., Oliveira, A. M., Ferragut, C., Fonseca, B. M., Lopes, M. R. M. et al. (2006). Criptógamos do Parque Estadual das Fontes de Ipiranga, São Paulo, S.P. Algas, 21: Xanthophyceae. Hoehnea, 33, 291–316.
Bojorge, G. M. G., Carmona, J. J., Beltrán, M. Y. y Cartajena, A. M. G. (2010). Temporal and spatial distribution of macroalgal communities of mountain streams in Valle de Bravo Basin, central Mexico. Hydrobiologia, 641, 159–169. https://doi.org/10.1007/s10750-009-0074-5
Bonilla-Rodríguez, M., Garduño Solórzano, G., Martínez-García, M., Campos, J. E., Monsalvo Reyes, A. C. y Quintanar-Zúñiga, R. E. (2013). Vaucheria zapotecana (Xanthophyceae), a new species from Oaxaca, Mexico. Phycologia, 52, 550–556. https://doi.org/10.2216/13-162.1
Bourrelly, P. (1952). Xanthophycées rares ou nouvelles. Bulletin du Museum National d´Histoire Naturelle, Série 2, 23, 666–672.
Bourrelly, P. (1981). Les algues d’eau douce. Initiation à la Systématique. II. Les algues jaunes et brunes. Chrysophycées, Phéophycées, Xanthophycées et Diatomées. París: Société Nouvelle des Éditions Boubée.
Cameron, R. E. (1960). Communities of soil algae ocurring in the Sonoran Desert in Arizona. Journal of the Arizona Academy of Sciences, 1, 85–88.
Cantoral, U. E. A., Carmona, J. J., González-González, J. y Montejano, Z. G. (1999). Algas indicadoras de la calidad del agua en el río la Magdalena, Delegación Magdalena Contreras, Distrito Federal, México. En D. Ponce-N. y M. V. Alegre (Eds.), Consejo de estudios para la restauración y valoración ambiental (aire-agua) (pp. 299–332). Ciudad de México: Gobierno del Distrito Federal.
Carmona-Jiménez, J. (1990). Ficoflora de manantiales de la Huasteca Postosina (Tesis). Facultad de Ciencias, Universidad Nacional Autónoma de México, México.
Carmona-Jiménez, J. y Montejano-Zurita, G. (1993). Carac-
terización ficológica en manantiales de la cuenca baja del sistema hidrológico de Pánuco, México. Boletín de la Sociedad Botánica de México, 53, 21–41. https://doi.org/10.17129/botsci.1414
Carmona-Jiménez, J., Ramírez-Rodríguez, R., Bojorge-García, M., González-Hidalgo, B. Y. y Cantoral-Uriza, E. A. (2016). Estudio del valor indicativo de las comunidades de algas bentónicas: una propuesta de evaluación y aplicación en el río Magdalena, Ciudad de México. Revista Internacional de Contaminación Ambiental, 32, 139–152. https://doi.org/10.20937/RICA.2016.32.02.01
Carmona-Jiménez, J. Salinas-Camarillo, V. H. y Caro-Borrego, A. (2022). The Macroalgae Ecological Quality Index (MEQI) in the Basin of Mexico: a proposal of aquatic bioindicators for peri-urban rivers. Revista Mexicana de Biodiversidad, 93, 1–17. https://doi.org/10.22201/ib.20078706e.2022.93.3899
Ceballos, G., List, K., Garduño-Solórzano, G., López-Cano, R., Muñozcano-Quintanar, M. J., Collado, E. & San Román, J. E. (Eds.). (2009). La diversidad biológica del Estado de México. Estudio de estado. Toluca de Lerdo: Gobierno del Estado de México.
Chávez, V., Zariñana, L., Novelo, E. y Tavera, R. (2005). Variación morfológica de algunas especies de Ophiocytium Nägeli (Xanthophyceae) de cuerpos de agua temporales del Estado de México. Hidrobiológica, 15, 311–320.
Comisión Nacional para el Conocimiento y Uso de la Biodiversidad (Conabio). (2020). Sexto informe nacional al convenio sobre la diversidad biológica. Conabio. https://www.biodiversidad.gob.mx/media/1/planeta/internacional/files/6IN_WEB_CLOSE.pdf
Esqueda-Lara, K., Sánchez, A. D. J., Valdés-Lagunes, G., Salcedo, M. Á., Franco-Torres, E. Y. y Florido, R. (2016). Fitoplancton en el humedal tropical Chaschoc en la cuenca baja del río Usumacinta. Revista Mexicana de Biodiversidad, 87, 1177–1188. https://doi.org/10.1016/j.rmb.2016.10.015
Ettl, H. (1978). Xanthophyceae. Teil 1. Stuttgart: Gustav Fischer Verlag.
Ettl, H. et Gärtner, G. (1995). Syllabus der Boden, Luft- und Flechtenalgen. Stuttgart: Gustav Fischer Verlag.
Favari, L., López, E., Martínez-Tabché, L. y Diaz-Pardo, E. (2002). Effect of insecticides on plankton and fish of Ignacio Ramírez Reservoir (Mexico): a biochemical and biomagnification study. Ecotoxicology and Environmental Safety, 51, 177–186. https://doi.org/10.1006/eesa.2002.2142
Figueroa, T. M. G. (2009). Algas de la cuenca de México. (Serie Académicos, CBS, UAM-Xochimilco). México D.F.: Universidad Autónoma Metropolitana. Unidad Xochimilco.
Figueroa, T. M. G., Arana-Magallón, F., Almanza-Encarnación, S., Ramos-Espinosa, M. G. y Ferrara-Guerrero, M. J. (2015). Microalgas del área natural protegida ejidos de Xochimilco y San Gregorio Atlapulco, México. Ciencia UAT, 9, 15–29.
Flechtner, V. R., Johansen, J. R. et Clark, W. H. (1998). Algal composition of microbiotic crusts from the central desert of Baja California, México. Great Basin Naturalist, 58, 295–311. https://doi.org/10.2307/41713069
Flores-Granados, C. (1980). Variaciones estacionales en la composición florística del fitoplancton de dos canales de Xochimilco, D.F. México (Tesis). Escuela Nacional de Ciencias Biológicas, Instituto Politécnico Nacional. México D.F.
Flórez, M. A. E. (2011). Composición y variación temporal de los grupos funcionales fitoplanctónicos en un embalse tropical (Tesis de maestría). Posgrado en Ciencias del Mar y Limnología (Limnología), Universidad Nacional Autónoma de México. México D.F.
García-Rodríguez, J. (2004). Distribución espacio tiempo del fitoplancton del lago Zempoala, Morelos, México durante un ciclo anual (Tesis de maestría). Facultad de Ciencias, Universidad Nacional Autónoma de México. México D.F.
García-Rodríguez, J. y Tavera, R. (1998). Fitoplancton del Lago Zempoala. Boletín de la Sociedad Botánica de México, 63, 85–100. https://doi.org/10.17129/botsci.1570
Garduño-Solórzano, G., Oliva-Martínez, M. G. y Ortega, M. (2009). Algas. En G. Ceballos, R. List, G. Garduño-Solórzano, R. López-Cano, M. J. Muñozcano-Quintanar, E. Collado et al. (Eds.), La diversidad biológica del Estado de México. Estudio de estado (pp. 153–161). Toluca de Lerdo: Gobierno del Estado de México.
Godínez-Ortega, J. L., Ortega, M. M., Garduño, G., Oliva, M. G. y Vilaclara, G. (2001). Traditional knowledge of Mexican continental algae. Journal of Ethnobiology, 21, 57–88.
Godínez-Ortega, J. L., Oliva-Martínez, M. G., Escobar-Oliva, M. A. y Mendoza-Garfias, B. (2017). Diversidad algal del Parque Nacional Lagunas de Zempoala, México, excepto diatomeas. Hidrobiológica, 27, 45–58. https://doi.org/10.24275/uam/izt/dcbs/hidro/2017v27n1/Godinez
GBIF: The Global Biodiversity Information Facility. (2024). What is GBIF? Recuperado el 10 de diciembre, 2024 de: https://www.gbif.org/what-is-gbif
González-Barrera, A. (1991). Contribución al estudio ficológico estacional de la laguna de Tlila y canales adyacentes, Xochimilco, México, D.F. (Tesis). Facultad de Ciencias, Universidad Nacional Autónoma de México. México D.F.
González-González, J. y Novelo, E. (1986). Algas. En A. Lot y F. Chiang (Eds.). Manual de herbario. Administración y manejo de colecciones, técnicas de recolección y preparación de ejemplares botánicos (pp. 47–54). Consejo Nacional de Flora de México, México D.F.
Guiry, M. D. y Guiry, G. M. (2025). AlgaeBase. World-wide electronic publication, University of Galway. Recuperado el 03 de marzo, 2025 de: https://www.algaebase.org
Hammer, Ø., Harper, D. A. T. y Ryan, P. D. (2001). PAST: Paleontological Statictics software package for education and data análisis. Paleontologia Electronica, 4, 9.
Hernández-Morales, R., Ortega-Murillo, M. R., Alvarado-Villanueva, R., Sánchez-Heredia, J. D. y Medrano-Zarco, F. (2008). Variación anual del fitoplancton en el lago cráter la Alberca de Tacámbaro, Michoacán, México. Biológicas, 10, 5–17.
Hernández-Morales, R., Ortega-Murillo, R., Sánchez, J. D., Alvarado-Villanueva, R. y Aguilera, M. S. (2011). Distribución estacional del fitoplancton en un lago cálido monomíctico en Michoacán, México. Biológicas, 13, 21–28.
Hollerbach, M. M. (1962). De vi taxonomica Polyedriopsis spinulosae Schmidle et genere novo Xanthophytorum pseudopolyedriopsis Hollerb. notula. Botanicheskij Mater-
ialy, 15, 62–67.
Islam, A. K. M. N. e Irfanullah, H. M. (2001). Some new records of algae for Bangladesh: Cyanarcus, Chloremys, Myrmecia, Selenodictyum, Tetraplektron, and Pseudostaurastrum. Bangladesh. Journal of Plant Taxonomy, 8, 1–7.
Jaccard, P. (1901). Étude comparative de la distribution florale dans une portion des Alpes et des Jura. Bulletin of the New York Botanical Garden, 3, 1–46. https://doi.org/10.5169/SEALS-266450
Jiménez, A. G. (2010). Variaciones en la dominancia de grupos fitoplanctónicos en la capa de mezcla/zona trofogénica de un embalse tropical eutrófico con cambios significativos de nivel (Tesis de maestría). Posgrado en Ciencias del Mar y Limnología. Universidad Nacional Autónoma de México. México D.F.
John, D. M., Whitton, B. A. y Brook, A. J. (2002). The freshwater algal flora of the British Isles: an identification guide to freshwater and terrestrial algae. Cambridge University Press. U.K.
Krienitz, L., Hegewald, E., Reymond, O. L. y Peschke, T. (1993). Variability of LM, TEM and SEM characteristics of Pseudogoniochloris tripus gen. et comb. nov. (Xanthophyceae). Archiv für Hydrobiologie Supplement, 97, 67–82.
Krienitz, L., Hepperle, D., Stich, H. B. y Weiler, W. (2000). Nannochloropsis limnetica (Eustigmatophyceae), a new species of picoplankton from freshwater. Phycologia, 39, 219–227. https://doi.org/10.2216/i0031-8884-39-3-219.1
López-Adrián, S. J. y Barrientos-Medina, R. C. (2005). Diversidad y distribución del fitoplancton de agua dulce en la península de Yucatán, México. Ibugana. Boletín IBUG, 13, 3–13.
López-Adrián, S. J. y Catzim, C. L. A. (2010). Microalgas dulceacuícolas. En R. Durán García y M. E. Méndez González (Eds.), Biodiversidad y desarrollo humano en Yucatán (pp. 185–186). Mérida: CICY/ PPD-FMAM/ Conabio/ SEDUMA.
López-Adrián, S. J., Barrientos-Medina, R. C., Tavera, R. y Novelo, E. (2017). Ficoflora de la zona urbana y conurbada de Yucatán. En S. J. López-Adrián y E. Novelo-Maldonado (Eds.), Microalgas de la península de Yucatán (pp. 28–38). Mérida: Edición privada.
López-Segovia, E., Pérez-Díaz, J., Del Moral-Flores, L. F. y Hernández-Arellano, T. (2024). New records on the distribution of the Mexclapique, Girardinichthys viviparus (Bustamante, 1837) (Cyprinodontiformes, Goodeidae), an endangered species in Mexico. Neotropical Biology and Conservation, 19, 347–359. https://doi.org/10.3897/neotropical.19.e126767
Lot, A. (2007). Guía ilustrada de la Cantera Oriente. Caracterización ambiental e inventario biológico. México D.F.: Secretaría Ejecutiva de la Reserva Ecológica del Pedregal de San Ángel, Coordinación de la Investigación Científica, UNAM.
Macedonio, F. J. (2024). El lago de Coatetelco como patrimonio biocultural. En A. García-Flores, H. Colín-Bahena y J. M. Rivas-González (Coord.), Conocer para conservar: estudios de la diversidad biocultural en Coatetelco, Morelos (pp. 47–66). Cuernavaca: Universidad Autónoma del Estado de Morelos.
Magurran, A. E. (2004). Measuring biological diversity. London: Blackwell Publishing.
Martínez, M. M. (2016). Estructura de la microflora planctónica y perifítica en el lago de Cuitzeo (Tesis de maestría). Universidad Michoacana de San Nicolás de Hidalgo, Morelia. México.
Mendoza-González, A. C. (1985). Estudio florístico ficológico estacional de la laguna Victoria o de Santiago Tilapa, México. Phytologia, 58, 479–487.
Mendoza-González, A. C., Huerta-Múzquiz, L. y Flores-Granados, C. (1985). Estudio florístico del fitoplancton del lago Ziruahuén, Michoacán, México. Phytologia, 59, 1–8.
Mireles, V. A. (2019). Aspectos ecológicos de algas metafíticas en dos lagos de Tabasco, México (Tesis de maestría). Posgrado en Ciencias del Mar y Limnología. Universidad Nacional Autónoma de México. México D.F.
Montejano-Zurita, G., Carmona-Jiménez, J. y Cantoral-Uriza, E. A. (2000). Algal communities from calcareous springs in La Huasteca, central Mexico: a synthesis. En M. Munawar, S. G. Lawrence, I. F. Munawar y D. F. Malley (Eds.), Aquatic ecosystems of Mexico. Status and scope (pp. 135–149). Leiden: Backhuys Pub.
Montejano-Zurita, G., Cantoral-Uriza, E. A. y Carmona-Jiménez, J. (2004). Algas de ambientes lóticos en la cuenca baja del río Pánuco. En I. Luna, J. J. Morrone y D. Espinosa (Eds.), Biodiversidad de la Sierra Madre Oriental (pp. 111–126). Las Prensas de Ciencias, México D.F.: Universidad Nacional Autónoma de México.
Mora-Navarro, M. R. (2004). Fitoplancton del lago de Chapala, Jalisco-Michoacán, México (Tesis doctoral). Centro Universitario de Ciencias Biológicas y Agropecuarias, Universidad de Guadalajara.
Mora-Navarro, M. d. R., Vázquez-García, J. A. y Vargas, Y. L. (2004). Ordenación de comunidades de fitoplancton en el lago de Chapala, Jalisco-Michoacán, México. Hidrobiológica (Iztapalapa), 14, 91–103.
Mora-Navarro, M. R., Vázquez-García, J. A., Guzmán-Arroyo, M., Mora-Navarro, M. A., Núñez-Márquez, I. G. y Reyes-González, M. E. (2006). Fitoplancton del lago de Chapala, Jalisco-Michoacán, México. En M. R. Mora-Navarro, J. A. Vázquez-García, Y. L. Vargas-Rodríguez y R. M. Hernández-Herrera (Eds.), Algas del occidente de México. Florística y ecología (pp. 8–29). Guadalajara: Universidad de Guadalajara (CUCBA)/ Fundación Gonzalo Río Arronte/ Sociedad Ficológica de México.
Moreno, C. R. y Palacios, D. C. E. (1987). Estudio ficoflorístico preliminar en la presa de La Concepción, Tepotzotlán, Estado de México (Tesis). Facultad de Estudios Superiores-Iztacala, Universidad Nacional Autónoma de México. México.
Moreno-Ruiz, J. L. (1985). Contribución al estudio básico (análisis inicial de la diversidad alimenticia) de Ictiobus merinionalis Günter (Cypriniformes: Catastomidae), en algunas localidades de la cuenca baja del río Papaloapan (Tesis). Facultad de Ciencias, Universidad Nacional Autónoma de México. México D.F.
Moreno-Ruiz, J. L. (2005). Fitoplancton. En J. Bueno, F. Álvarez y S. Santiago (Eds.), Biodiversidad del estado de Tabasco (pp. 33–63). México D.F.: Conabio/ Instituto de Biología, UNAM.
Moreno-Ruiz, J. L., Tapia-García, M., González-Macías, M. C. y Figueroa-Torres, M. G. (2008). Fitoplancton del río Tehuantepec, Oaxaca, México y algunas relaciones biogeográficas. Revista de Biología Tropical, 56, 27–54.
Novelo, E. (1998). Floras ficológicas del Valle de Tehuacán, Puebla (Tesis doctoral). Facultad de Ciencias, Universidad Nacional Autónoma de México. México D.F.
Novelo, E. (2014). Heterokontophyta Hoek. Flora del Valle de Tehuacán-Cuicatlán. Instituto de Biología, Universidad Nacional Autónoma de México. México D.F.
Novelo, E. y Tavera, R. (2025). BdLACET Base de datos de algas continentales. Facultad de Ciencias. Universidad Nacional Autónoma de México. México D.F. Consultado el 19 de octubre, 2024 en: https://bdlacet.mx/
Novelo, E., Tavera, R. y Lira, B. (2023). Un estudio a largo plazo de la flora algal en lagos urbanos. Revista Mexicana de Biodiversidad, 94, e945149. https://doi.org/10.22201/ib.20078706e.2023.94.5149
Novelo, E., Ponce, M. E. y Ramírez, R. (2009). Las microalgas de la Cantera Oriente. En A. Lot y Z. Cano-Santana (Eds.), Biodiversidad del ecosistema del Pedregal de San Ángel (pp. 71–79). Libro conmemorativo del 25 aniversario de la Reserva Ecológica de Ciudad Universitaria (1983-2008). México D.F: Universidad Nacional Autónoma de México.
Núñez-Márquez, I. G. y Reyes-González, M. E. (1995). Contribución al conocimiento del fitoplancton del lago de Chapala, Jalisco, México, durante el período de febrero a mayo de 1989, 90 y 91 (Tesis). Universidad de Guadalajara, CUCBA, División de Ciencias Biológicas y Ambientales.
Ochoa, Z. G. G. (2023). Ficoflora de sistemas lóticos y lénticos de Nayarit (Tesis de maestría). Universidad Autónoma de Nayarit. Tepic.
Ortega, M. M. (1984). Catálogo de algas continentales recientes de México. México D.F: Universidad Nacional Autónoma de México.
Ortega-Murillo, M. R., Aguilar-Gómez, M. E., Alvarado-Villanueva, R., Hernández-Morales, R. y Díaz-Martínez, N. T. (2014). Riqueza específica de las microalgas de la subcuenca del río Cupatitzio, Michoacán, México. Boletín de la Sociedad Mexicana de Ficología, 4, 10–20.
Osorio, S. J. J. y López, P. R. (2005). Diversidad y distribución del fitoplancton de la laguna El Balsón, Tabasco, México (Tesis). División Académica de Ciencias Biológicas. Universidad Juárez Autónoma de Tabasco. Villahermosa.
Pascher, A., Schiller, J. y Migula, W. (1925). Heterokontae, Phaeophyta, Rhodophyta, Charophyta. Die Süsswasserflora Deutschlands, Österreichs und der Schweiz, Heft 11. Jena. https://doi.org/10.5962/bhl.title.21607
Pedraza, A. C. I. (2020). Relación de la comunidad fitoplanctónica y los factores abióticos del lago Cantemual en Tabasco (Tesis de maestría). Posgrado en Ciencias del Mar y Limnología, Universidad Nacional Autónoma de México. México D.F.
Pérez-Gutiérrez, R. M., Martínez-Flores, A., Vargas-Solís, R. y Jiménez, J. (2008). Two new antibacterial norabietane diterpenoids from cyanobacteria, Microcoleus lacustris. Journal of Natural Medicines, 62, 328–331. https://doi.org/10.1007/s11418-008-0238-z
Ponce, M. M. E., Ramírez, R. R. y Ramírez, V. M. (2019). Algas de la Cantera Oriente, Reserva Ecológica del Pedregal de San Ángel. Guía de campo y laboratorio. Las Prensas de Ciencias, Universidad Nacional Autónoma de México, México.
Quiroz-Castelán, H., Molina-Astudillo, F. I., García-Rodríguez, J. y Díaz-Vargas, M. (2007). Los lagos Zempoala y Tonatiahua del Parque Nacional Lagunas de Zempoala, Morelos. En G. De la Lanza-Espino y S. Hernández-Pulido (Eds.), Las aguas interiores de México: conceptos y casos (pp. 141–167). México D.F.: AGT Editor, S.A.
Ramírez, L. J. E. (2010). Caracterización del ecosistema de ribera y su valor indicador del estado ecológico en la subcuenca Valle de Bravo-Amanalco, Estado de México (Tesis de maestría). Posgrado en Ciencias del Mar y Limnología, Universidad Nacional Autónoma de México. México D.F.
Real, R. y Vargas, J. M. (1996). The probabilistic basis of jaccard’s index of similarity. Systematic Biology, 45, 380–385. https://doi.org/10.1093/sysbio/45.3.380
Ríos, T. R. M. (2009). Composición química de las aguas del cauce Tula-Moctezuma-Claro, estado de Hidalgo (Tesis de maestría). Colegio de Postgraduados, Campus Montecillo. Texcoco, Estado de México.
Rodríguez, M. Z., Comin, C. H., Casanova, D., Bruno, O. M., Amancio, D. R., Costa, L. et al. (2019). Clustering algorithms: a comparative approach. Plos One, 14, e0210236. https://doi.org/10.1371/journal.pone.0210236
Rodríguez-Flores, R. (2014). Diversidad y distribución de algas macroscópicas en ríos de alta montaña de la cuenca de México (Tesis). Facultad de Ciencias, Universidad Nacional Autónoma de México. México D.F.
Rodríguez-Flores, R. y Carmona, J. J. (2018). Ecology and distribution of macroscopic algae communities in streams from the Basin of Mexico. Botanical Sciences, 97, 63–75. https://doi.org/10.17129/botsci.1237
Rybalka, N. (2015). Assessing phylogenetic delineations of taxa of filamentous Xanthophyceae (Stramenopiles) using DNA sequence analyses and morphology. (Ph.D. dissertation). Kiel University. Kiel.
Sámano-Bishop, A. (1934). Contribución al conocimiento de las algas verdes de los lagos del Valle de México. Anales del Instituto de Biología. Universidad Nacional Autónoma de México, 5, 149–173.
Sánchez-Gómez, S. P. y Lara-Villa, M. A. (1986). Análisis fitoplanctónico e hidrológico de un cuerpo de agua dulce tropical: laguna de Amela, Colima, México (Tesis). Escuela Nacional de Estudios Profesionales-Zaragoza. Universidad Nacional Autónoma de México. México D.F.
Schmitter-Soto, J. J., Comín, F. A., Escobar-Briones, E., Herrera-Silveira, J., Alcocer, J., Suárez-Morales, E. et al. (2002). Hydrogeochemical and biological characteristics of cenotes in the Yucatán Peninsula (SE Mexico). Hydrobiologia, 467, 215–228. https://doi.org/10.1023/A:1014923217206
Starmach, K. (1968). Flora slodkowodna Polski [Freshwater flora of Poland]. Volume 7. Chrysophyta III. Xanthophyceae Ròżnowiciowe. Varsovia: Państwowe Wydawn.
Takano, Y. y Horiguchi, T. (2005). Acquiring scanning electron microscopical, light microscopical and multiple gene sequence data from a single dinoflagellate cell. Journal of Phycology, 42, 251–256. https://doi.org/10.1111/j.1529-8817.2006.00177.x
Tavera, R. y Diez, B. (2009). Multifaceted approach for the analysis of the phototrophic microbial community in a freshwater recreational area of Xochimilco, México. Hydrobiologia, 636, 353–368. https://doi.org/10.1007/s10750-009-9965-8
Tavera, R., Novelo, E. y Orozco, C. (2018). Las diatomeas del Parque Ecológico de Xochimilco, México ¿Qué tan importante es la flora de un grupo de un pequeño lugar? Cymbella, 4, 3–46. https://cymbella.fciencias.unam.mx/articulos/V4/01/Las_diatomeas_del_Parque_Ecologico_de_Xochimilco_Mexico.html
Valadez-Cruz, F. (1998). Empleo de crecimientos algales para la caracterización de ambientes lóticos en la cuenca baja del río Amacuzac, Morelos (Tesis de maestría). Facultad de Ciencias, Universidad Nacional Autónoma de México.
Valadez-Cruz, F., Carmona, J. J. y Cantoral, U. E. (1996). Algas de ambientes lóticos en el Estado de Morelos, México. Anales del Instituto de Biología, Serie Botánica, 67, 227–282. https://repositorio.unam.mx/contenidos/28749
Valadez-Cruz, F., Rosiles-González, G. y Ortega-Rubio, A. (2015). Potenciales bioindicadores del elenco ficológico de la Reserva de la Biosfera Sian Ka’an. En A. Ortega-Rubio, A. M. J. Pinkus-Rendón e I. C. Espitia-Moreno (Eds.). Las áreas naturales protegidas y la investigación científica en México (pp. 285–314). La Paz: Centro de Investigaciones Biológicas del Noroeste/ Universidad Autónoma de Yucatán/ Universidad Michoacana de San Nicolás de Hidalgo.
Valdez, S. Z. (2012). Diagnóstico ambiental en las inmediaciones del embalse Requena, municipio de Tepeji del Río, Hidalgo (Tesis). Facultad de Estudios Superiores – Iztacala, Universidad Nacional Autónoma de México. Estado de México.
Vázquez, G. y Blanco-Pérez, R. (2011). Microalgas dulceacuícolas. En Comisión Nacional para el Conocimiento y uso de la Biodiversidad (Ed.), La biodiversidad en Veracruz. Estudio de estado (pp. 77–88). México D.F.: Comisión Nacional para el Conocimiento y uso de la Biodiversidad/ Gobierno del Estado de Veracruz/ Universidad Veracruzana/ Instituto de Ecología, A.C.
Yang, E. C., Boo, G. H., Kim, H. J., Cho, S. M., Boo, S. M., Andersen, R. A. et al. (2012). Supermatrix data highlight the phylogenetic relationships of photosynthetic Stramen-
opiles. Protist, 163, 217–231. https://doi.org/10.1016/j.protist.2011.08.001
Zariñana-Leguízamo, M. L. 1997. Variación estacional de Ophiocytium parvulum (Perty) A. Braun 1855 en un sistema acuático inestable en el municipio de El Oro, Estado de México (Tesis). Facultad de Ciencias, Universidad Nacional Autónoma de México. México D.F.