In vitro propagation and adaptation of plants to ex vitro conditions of Kroenleinia grusonii (Cactaceae)
Dolores Adilene García-González, Juan Pedro Flores-Margez y Pedro Osuna-Ávila *
Universidad Autónoma de Ciudad Juárez, Instituto de Ciencias Biomédicas, Av. Benjamín Franklin Núm. 4650, Zona Pronaf Condominio La Plata, 32310 Ciudad Juárez, Chihuahua, México
*Autor para correspondencia: posuna@uacj.mx (P. Osuna-Ávila)
Recibido: 23 mayo 2025; aceptado: 14 octubre 2025
Resumen
Kroenleinia grusonii (Hildm.) Lodé, es una cactácea endémica del centro de México que enfrenta riesgos como la colecta ilegal o la modificación de su hábitat natural y se encuentra catalogada como en peligro de extinción. El objetivo de este trabajo fue evaluar concentraciones de 6-bencilaminopurina (BAP) sola o combinada con ácido indolacético (AIA) en la formación de brotes de K. grusonii e inducir la formación de raíces para valorar la adaptación de plantas a condiciones ex vitro. La inducción de brotes fue con BAP (0, 1.0, 2.0 y 3.0 mg/L), AIA (0.5 mg/L) y BAP (0, 1.0, 2.0 y 3.0 mg/L) + AIA (0.5 mg/L). Se aplicó AIA 0, 1.0, 2.0 y 3.0 mg/L para enraizamiento y la adaptación ex vitro de las plantas fue con musgo de turba y con una mezcla de musgo de turba y suelo natural (1:1). El mejor tratamiento fue BAP 3.0 mg/L con 5.13 ± 0.9150 brotes por explante. Se obtuvo 89 ± 0.03% de brotes enraizados y la sobrevivencia ex vitro fue de 68.75% en musgo de turba con suelo natural (1:1). Se estableció un protocolo para la propagación clonal de K. grusonii, lo cual representa una contribución para su conservación ex situ.
Palabras clave: Ácido indol-3-acético; 6-bencilaminopurina; Brotes; Cactus; Endémica; Enraizamiento
Abstract
Kroenleinia grusonii (Hildm.) Lodé, is a cactus endemic to central Mexico, that faces risks such as illegal collection or modification of its natural habitat and is listed as endangered. The objective of this work was to evaluate different concentrations of 6-benzylaminopurine (BAP) alone or combined with indoleacetic acid (IAA) in K. grusonii and to induce root formation to assess plant adaptation to ex vitro conditions. Shoot induction was with BAP (0, 1.0, 2.0 and 3.0 mg/L), IAA (0.5 mg/L) and BAP (0, 1.0, 2.0 and 3.0 mg/L) + IAA (0.5 mg/L). AIA 0, 1.0, 2.0 and 3.0 mg/L was applied for rooting and the ex-vitro adaptation of the plants was with peat moss and a mix with peat moss with natural soil (1:1). The best treatment was BAP 3.0 mg/L with 5.13 ± 0.9150 shoots per explant. 89 ± 0.03% of rooted shoots were obtained and the ex-vitro survival was 68.75% in peat moss substrate with natural soil (1:1). A protocol for the clonal propagation of K. grusonii was established, which represents a contribution to its ex-situ conservation.
Keywords: Indole-3-acetic acid; 6-bencylaminoourine; Shoots; Cactus; Endemic; Rooting
Introducción
Kroenleinia grusonii (Hildm.) Lodé (Cactaceae), también conocida como la biznaga barril de oro, es una especie que se utiliza con fines ornamentales, gastronómicos y agropecuarios (Rodríguez et al., 2021). La especie se distribuye principalmente en el centro de México en los estados de Guanajuato, Querétaro, Hidalgo, San Luis Potosí y Zacatecas (Lodé, 2014). Se encuentra en riesgo de desaparecer debido a la destrucción de su hábitat natural, ya que sus poblaciones se encuentran en deterioro por la colecta ilegal, el desarrollo urbano y la construcción de carreteras, entre otros factores (Pérez-Molphe-Balch et al., 2015; Villavicencio-Gutiérrez et al., 2023). Kroenleinia grusonii es un taxón endémico y debido a las adversidades que enfrenta, se encuentra enlistado en la NOM-059-SEMARNAT-2010 bajo la categoría en peligro de extinción (Semarnat, 2019). La UICN (Unión Internacional para Conservación de la Naturaleza) la cataloga como especie en peligro (Guadalupe-Martínez et al., 2013). En consecuencia, es necesario implementar estrategias que permitan la propagación de esta especie para su conservación y protección sin afectar a las poblaciones naturales.
La propagación de las cactáceas se realiza, principalmente, mediante semillas; sin embargo, es necesario buscar otras formas (Manzo et al., 2022), en particular, cuando las especies se encuentran bajo algún estatus de riesgo y no es posible obtener suficientes semillas para iniciar protocolos de propagación (Pérez-Molphe-Balch et al., 2015). Una alternativa es el uso de herramientas biotecnológicas, como el cultivo de tejidos vegetales. Con esta técnica es posible la propagación clonal manteniendo la estabilidad genética clonal y obtener un gran número de plantas con fines de conservación ex situ (Torres-Silva et al., 2021).
Esta herramienta ofrece obtener una rápida multiplicación vegetativa comparado con la propagación tradicional (Mabrouk et al., 2021). Con esta técnica biotecnológica se reduciría el impacto que se ha creado en las cactáceas debido a la sobrecolecta (López-Granero et al., 2021). La técnica se basa en la totipotencia celular que incluye la expresión total del genoma presente en la célula, que permite la multiplicación aumentando el número de individuos (Almeida et al., 2021). Esta cualidad se ve incrementada por la adición de reguladores de crecimiento en el medio de cultivo, especialmente las citoquininas y auxinas, que favorecen el desarrollo de nuevos brotes (Civatti et al., 2017). El potencial regenerativo de las plantas puede variar dependiendo de diversos factores, como el genotipo, el explante utilizado y los reguladores de crecimiento (Torres-Silva et al., 2018).
En cactáceas se ha realizado la propagación in vitro utilizando diferentes explantes como lo son plantas adultas de Opuntia ficus-indica (L.) Mil. (Khalafalla et al., 2007), activación de areolas en Turbinicarpus pseudomacrochele subsp. lausseri (Diers et G. Framk) Glass (de la Rosa-Carrillo et al., 2012), secciones transversales o longitudinales de plántulas de Melocactus glaucescens Buining et Brederoo (Torres-Silva et al., 2018) o brotes como en Echinocactus parryi Engelm. (García-González et al., 2020). Un paso fundamental en el proceso de propagación in vitro es la formación de raíces en los brotes obtenidos (Ivannikov et al., 2022). La inducción de raíces se logra con el uso de auxinas o en ocasiones, sin la necesidad de aplicarlas (Martínez et al., 2016). Por ejemplo, en la cactácea Cereus peruvianus (L.) Mill. los brotes regenerados obtuvieron 100% de enraizamiento en medio de cultivo MS (Murashige y Skoog, 1962) al 25% sin auxinas (Sawsan et al., 2004). Los brotes enraizados son transferidos a condiciones de invernadero, que es la última etapa de la propagación in vitro (Jagiello-Kubiec et al., 2021). El objetivo de la presente investigación fue evaluar diferentes concentraciones de 6-bencilaminopurina (BAP), sola o combinada con ácido indolacético (AIA) en la formación de nuevos brotes de K. grusonii; así como inducir en los brotes la formación de raíces y evaluar 2 sustratos para su adaptación a condiciones ex vitro.
Materiales y métodos
Para la inducción de brotes, se utilizaron plántulas de 90 días de cultivo in vitro de Kroenleinia grusonii como fuente de explantes, que se obtuvieron de experimentos de germinación in vitro de semillas (Osuna-Ávila et al., 2025). A las plántulas se les eliminó la raíz y se utilizaron los ápices completos, los cuales se colocaron en medio de cultivo MS a una concentración de 100% de macro y micronutrientes. El medio de cultivo se suplementó con 30g/L de sacarosa, 7 g/L de agar tipo 1 y el pH se ajustó a 5.7 ± 0.1. Posteriormente, se adicionaron diferentes concentraciones de BAP, AIA y AIA + BAP. Los tratamientos utilizados fueron 8 y consistieron en lo siguiente: control, BAP 1.0, 2.0 y 3.0 mg/L, combinada con o sin AIA. La unidad experimental fue un frasco de 100 ml conteniendo de 20-25 ml del medio de cultivo con 3 repeticiones, se colocaron 5 explantes en cada frasco con 15 explantes por tratamiento y un total de 120 unidades experimentales. Los explantes fueron subcultivados 2 veces en las mismas condiciones cada 60 días. El número total de brotes por cada explante fue registrado después de 120 días de cultivo in vitro.
Los brotes obtenidos de la propagación clonal fueron separados de los explantes utilizando pinzas y se colocaron en medio de cultivo MS al 100% adicionado con diferentes concentraciones de AIA. Los tratamientos fueron 4 y consistieron en lo siguiente: control, AIA 1.0, 2.0 y 3.0 mg/l. La unidad experimental fue el frasco de 100 ml conteniendo 20-25 ml de medio de cultivo con 8 repeticiones, se colocaron aleatoriamente 10 brotes en cada frasco para un total de 80 brotes en cada tratamiento y 320 unidades experimentales. El porcentaje de formación de raíces se evaluó después de 90 días de cultivo in vitro.
Para la adaptación de las nuevas plantas a condiciones ex vitro, se procedió a retirarlas del medio de cultivo utilizando los dedos para ablandar el agar y posteriormente enjuagando las raíces con agua de la llave. A los brotes que formaron raíces, se les midió la longitud de la raíz primaria utilizando un vernier digital y se contaron el número de raíces que se formaron en la base del brote. Se utilizaron 2 sustratos, el primero fue musgo de turba y el segundo fue una mezcla de musgo de turba y suelo natural regosol con textura franco arcillosa, pH de 8 y conductividad eléctrica de 0.45 dS m-1 (IUSS-WRB, 2015) (proporción 1:1). Cada sustrato fue colocado en una charola de 54 cm × 27 cm con 128 cavidades, en donde se colocaron los brotes que formaron raíces. Las plantas se regaron cada 24 h con agua de la llave a capacidad de campo, manteniendo humedad constante del sustrato. Después de 30 días en condiciones ex vitro se evaluó el porcentaje de sobrevivencia.
El análisis de datos fue realizado con el programa estadístico SPSS versión 24.0 (IBM. 2017). Se aplicó la prueba de Kruskal-Wallis no paramétrica para muestras independientes (prueba X²), ya que se trataba de variables discretas (número de brotes y raíces) y de una variable continua (longitud de raíz). La comparación múltiple de promedios se llevó a cabo con la prueba de Bonferroni con un nivel de significancia de 0.05 y los estadísticos descriptivos fueron obtenidos.
Resultados
El número de brotes por explante fue significativamente diferente entre los tratamientos aplicados (p < 0.05). Los mejores resultados de brotación fueron con BAP 3.0 mg/L (fig. 1A), seguido por BAP 1.0 mg/L + AIA 0.5 mg/L (fig. 1B) con un promedio de brotes de 5.13 por explante en cada uno después de 120 días de cultivo in vitro. Cuando el BAP 3.0 mg/L se combinó con AIA 0.5 mg/L, el número de brotes se redujo a 3.6 ± 0.914 (tabla 1). Los resultados no fueron significativos en el grupo control con un promedio de 0.07 ± 0.067 brotes por explante y el AIA 0.5 mg/L con 0.40 ± 0.400 brotes por explante. Los tratamientos de BAP 1.0 mg/L, BAP 2.0 mg/L, AIA 0.5 mg/l + BAP 2.0 mg/L y AIA 0.5 mg/L + BAP 3.0 mg/L, formaron brotes; sin embargo, no fueron significativos con promedios desde 2.8 hasta 3.6 brotes por explante (tabla 1). Los nuevos brotes obtenidos, presentaron diferentes tamaños desde 5 hasta 18 mm de diámetro (fig. 1C).
Tabla 1
Número de brotes obtenidos en la propagación clonal de Kroenleinia grusonii a los 120 días de cultivo in vitro (n = 15).
| BAP mg/L | AIA mg/L | Número de brotes |
| 0 (control) | 0 | 0.07 ± 0.067 b |
| 1.0 | 0 | 3.20 ± 0.890 ab |
| 2.0 | 0 | 3.13 ± 2.109 ab |
| 3.0 | 0 | 5.13 ± 0.9150 a |
| 0 | 0.5 | 0.40 ± 0.400 b |
| 1.0 | 0.5 | 5.13 ± 1.055 a |
| 2.0 | 0.5 | 2.80 ± 1.010 ab |
| 3.0 | 0.5 | 3.60 ± 0.914 ab |
Medias ± el error estándar, letras iguales no son estadísticamente diferentes (n = 80).
Tabla 2
Porcentaje de enraizamiento de brotes, número de raíces por brote y longitud de la raíz principal a los 90 días de cultivo in vitro de Kroenleinia grusonii.
| AIA mg/L | % de enraizamiento | Número de raíces | Longitud de raíces (mm) |
| Control | 66 ± 0.05 b | 3.21 ± 0.385 b | 21.86 ± 1.764 a |
| 1.0 | 77 ± 0.04 ab | 2.89 ± 0.255 b | 19.98 ± 1.631 a |
| 2.0 | 89 ± 0.03 a | 4.68 ± 0.407 a | 22.36 ± 1.583 a |
| 3.0 | 84 ±0.04 a | 3.18 ± 0.293 b | 22.24 ± 1.688 a |
Medias ± el error estándar, letras iguales no son estadísticamente diferentes (n = 80).
La tabla 2 indica que hubo diferencias entre los tratamientos para el porcentaje de inducción de raíces en los brotes cultivados in vitro por 90 días. Para el porcentaje de enraizamiento, se observó que el adicionar AIA al medio de cultivo MS promueve significativamente la formación de raíces en los brotes. Particularmente, con el tratamiento de AIA 2.0 mg/L que resultó ser el mejor con 89 ± 0.03 % de enraizamiento, en comparación con el tratamiento control que mostró 66 ± 0.05 % de brotes enraizados (tabla 2). Por tales motivos, el aplicar AIA 2.0 mg/L resulta ser, aproximadamente, 20% más efectivo para la inducción de raíces que el resto de los tratamientos.

El número de raíces por explante fue significativamente diferente entre tratamientos (p < 0.05). La comparación de promedios muestra que el AIA 2.0 mg/L presentó el mayor promedio de número de raíces con aproximadamente 5 (4.68 ± 0.407) en cada brote. Mientras que el AIA 1.0 mg/L, AIA 2.0 mg/L y el control desarrollaron, en promedio, menos de 3.2 raíces por explante (tabla 2; fig. 2).
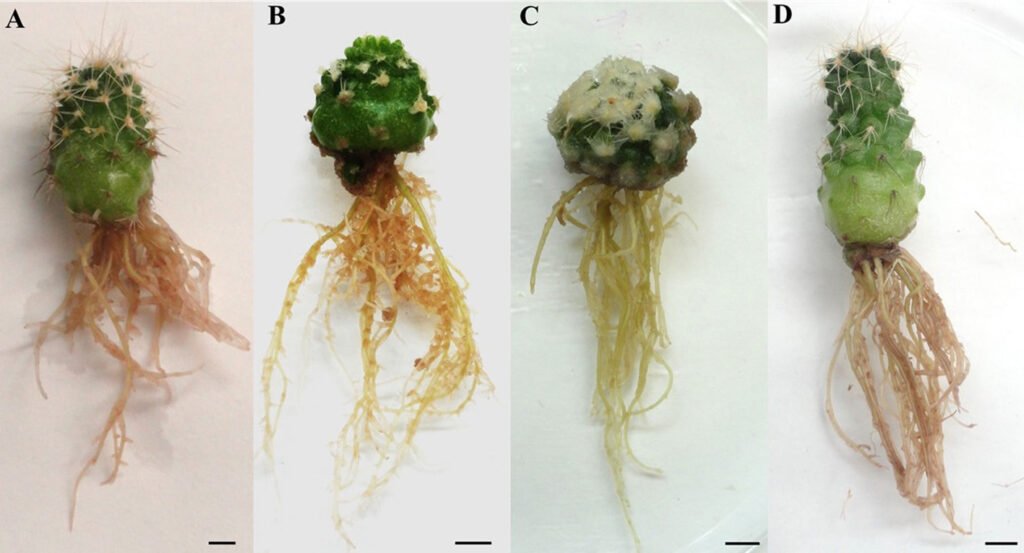

En relación con la variable largo de raíz, no se detectó efecto significativo (p = 0.604). El intervalo observado entre los tratamientos fue de 2.38 mm en promedio, es decir, la variable mostró poca variación. Sin embargo, por los resultados obtenidos con AIA 2.0 mg/L, se muestra un promedio ligeramente por arriba que el resto de los tratamientos con 22.36 ± 1.583 mm (tabla 2). Después de 60 días en condiciones ex vitro, el mejor sustrato para promover la aclimatización de las plantas fue el de suelo de turba y suelo natural (1:1). El porcentaje de sobrevivencia que presentó este sustrato fue de 68.75% después de 60 días. Mientras que el sustrato de suelo de turba mostró un porcentaje de sobrevivencia inferior, de 60.93% después de 60 días (fig. 3).
Discusión
La conservación ex situ de cactáceas a través de la propagación clonal es una alternativa viable para las especies que se encuentran en alguna situación de riesgo (Torres-Silva et al., 2021). Con el uso de citoquininas, en algunas cactáceas que no forman brotes laterales, se rompe la dominancia apical y se promueve la formación de nuevos brotes (Lema-Ruminska y Kulus, 2014). Particularmente, con los resultados observados, el uso de BAP 3.0 mg/l promovió la misma cantidad de brotes que la combinación de BAP 1.0 mg/l y AIA 0.5 mg/l, lo cual indica que para obtener resultados significativos no sería necesaria la adición de auxinas al medio de cultivo. Ramírez y Salazar (2016) reportan que la cinetina 10 mg/l es más eficiente en la formación de brotes en los explantes que al combinarla con auxina en Mammillaria petterssonii Hildm. y Coryphanta radians (D. C). Britton et Rose. El resultado es similar en Stenocereus stellatus al utilizar BAP 4.0 mg/L y obtener un promedio de 8 brotes por explante (Martínez et al., 2011). Por el contrario, existen especies que han sido propagadas y que para obtener mayor formación de brotes sí requieren una combinación de citoquinina y auxina. Por ejemplo, en M. geminispina Haw. con cinetina 10 mg/l + AIA 4.0 mg/l obtuvieron 6 brotes por explante (Ramírez y Salazar, 2016). Melocactus glaucescens Buining et Brederoo con BAP 4.0 mg/l + ácido 1-naftalenacético (ANA) 0.25 mg/l presentó 2.5 brotes por explante y sin ANA, un promedio de 0.6 (Torres-Silva et al., 2018). En Echinocactus parryi reportan que es más efectiva la combinación de BAP 2.0 mg/l + AIA 0.5 mg/l al regenerar 2.9 brotes por explante, a diferencia de los tratamientos sin AIA en los que el número de brotes no fue significativo (García-González et al., 2020).
Una consideración importante en Kroenleinia grusonii es que el número de brotes se redujo de 5.13 ± 0.9150 obtenidos con BAP 3 mg/l a 3.6 ± 0.914 al combinar el BAP 3.0 mg/l + AIA 0.5 mg/l. Resultados similares se reportaron para Coryphantha retusa (Pfeiff.) Birtton et Rose, ya que al aplicar BAP 2.0 mg/l el promedio de brotes fue de 8.8 por explante y al combinar BAP 2.0 mg/l + ANA 1.0 mg/l el número de brotes se redujo a 4.2 (Ruvalcaba-Ruíz et al., 2010). Lo mismo sucedió con Pachycereus pringlei (S. Watson) Britton et Rose, con BAP 2.0 mg/l el número de brotes fue de 3.8 ± 0.3 y se redujo a 0.6 ± 0.1 al combinarlo con ANA 0.5 mg/l (Pérez-Molphe-Balch et al., 2002). Los resultados que se obtengan en la propagación clonal dependen del genotipo y de los reguladores de crecimiento utilizados (Montiel-Frausto et al., 2016).
Es de gran importancia establecer un sistema de micropropagación específico para cada especie, no obstante, la respuesta a la formación de raíces y la aclimatización ex vitro puede variar debido a las condiciones de cultivo (Elias et al., 2015). Con los resultados obtenidos en K. grusonii, el tratamiento control mostró una respuesta favorable a la formación de raíces en los brotes. Sin embargo, al utilizar AIA 2.0 mg/l, se logra 30% más de enraizamiento, lo cual significa que se pueden obtener 70 plantas completas. El porcentaje de enraizamiento en K. grusonii se podría considerar alto con la aplicación de AIA debido a que se han reportado porcentajes inferiores de enraizamiento en diferentes especies de cactáceas. Algunos ejemplos son Cereus jamacaru DC. con 70% (Monostori et al., 2012) o Mammillaria vetula subsp. gracilis (Pfeiff.) D. R. Hunt con 20% de enraizamiento (López-Granero et al., 2021). El uso de auxinas como el ácido indolbutírico (AIB) 0.1 mg/l en Hylocereus monacanthus (Hort. ex Lem.) Britton et Rose donde el porcentaje fue mayor que en K. grusonii con 100% de enraizamiento (Montiel-Frausto et al., 2016). En contraste, para diferentes especies y con medios de cultivo sin auxinas, se ha logrado obtener hasta 95% de enraizamiento en C. retusa (Ruvalcaba-Ruíz et al., 2010), Micranthocereus flaviflorus Buining et Brederoo con 98% (Civatti et al., 2017), Mammillaria hernandezii Glass et R. A. Foster con 98.4% de enraizamiento y Mammillaria dixanthocentron Beckeb. ex Mottram con 94% (Lázaro-Castellanos et al., 2018) comparados con los reportados en la presente investigación para K. grusonii.
El uso de AIA 2.0 mg/l es la mejor opción para obtener el mayor número y longitud de raíces en K. grusonii. Resultados similares han sido reportados para H. monacanthus, donde el número de raíces obtenidas en los brotes presentó un promedio de 4.2 por planta, aunque la longitud de la raíz fue aproximadamente 6 veces menor a la de K. grusonii con 3.6 mm (Montiel-Frausto et al., 2016). También Turbinicarpus × mombergeri Říha presentó raíces de menor longitud que las de K. grusonii con 13 mm (Santos-Díaz et al., 2021). En cuanto al porcentaje de sobrevivencia de las plantas aclimatizadas, es importante resaltar que es necesario implementar métodos más eficientes para lograr aumentar el porcentaje de sobrevivencia de las plantas. Ejemplo de ello fue el trabajo realizado por Santos-Díaz et al. (2021), en donde la sobrevivencia de plantas de Turbinicarpus × mombergeri fue de 85% después de 1 año. Otro ejemplo sobresaliente fue lo mostrado por Cortés-Olmos et al. (2023), al reportar 100% de sobrevivencia en plantas de Gymnocalycium cv Fancy. De acuerdo con los resultados obtenidos y con base en literatura consultada, se infiere que las respuestas entre especies pueden llegar a ser muy diferentes, por lo cual se confirma que es necesario establecer protocolos específicos para cada especie y poder aprovechar al máximo el potencial regenerativo de cada una.
Se ha establecido un protocolo de la propagación clonal de Kroenleinia grusonii que inicia con la inducción de brotes, posteriormente el enraizamiento y finaliza con la aclimatización ex vitro. Con los resultados obtenidos en K. grusonii se logró la formación de hasta 5 brotes más con el uso de BAP 3.0 mg/l. Al inducir la formación de raíces en los brotes regenerados, es viable obtener aproximadamente 3 plantas nuevas por cada explante utilizado en la fase de inducción de brotes. Esta información representa un avance para continuar implementando técnicas de propagación in vitro en K. grusonii y que en futuras investigaciones se pueda promover un mayor número de plantas. Los resultados de este estudio, podrían contribuir a los programas de conservación ex situ e in situ de K. grusonii.
Referencias
Almeida, C. V. T., Amorim, D. S. E. P. y da Cunha, R. A. C. (2021). 5 medium MS at different concentrations in the initial development in vitro of Melocactus conoideus Buining & Brederoo. Scientia, 6, 81–91.
Civatti, L. M., Marchi, M. N. G., Schnadelbach, A. S. y Bellintani, M. C. (2017). In vitro multiplication and genetic stability of two species of Micranthocereus Backeb. (Cactaceae) endemic to Bahia, Brazil. Plant Cell, Tissue and Organ Culture, 131, 537–545. https://doi.org/10.1007/s11240-017-1304-6
Cortés-Olmos, C., Guerra-Sandoval, V. M., Blanca-Giménez, V. y Rodríguez-Burruezo, A. (2023). Micropropagation and acclimatization of Gymnocalycium cv. Fancy (Cactaceae): developmental responses to different explant types and hormone conditions. Plants, 12, 3932. https://doi.org/10.3390/plants12233932
de la Rosa-Carrillo, M. L., Domínguez-Rosales, M. S., Pérez-Reyes, M. E. y Pérez-Molphe-Balch, E. (2012). Cultivo y propagación in vitro de cactáceas amenazadas del género Turbinicarpus. Interciencia, 37, 114–120.
Elias, H., Mat, T. R., Hasbullah, N. A., Mohamed, N., Manan, A. A., Mahmad, N. et al. (2015). The effects of plant growth regulators in shoot formation, regeneration and coloured callus production in Echinocereus cinerascens in vitro. Plant Cell, Tissue and Organ Culture, 120, 729–739. https://doi.org/10.1007/s11240-014-0642-x
García-González, D. A., Santos-Díaz, M. S., Flores-Margez, J. P. y Osuna-Ávila, P. (2020). Influencia del Ca2+, pH, agar y reguladores de crecimiento en la propagación in vitro de Echinocactus parryi (Engelm). Terra Latinoamericana, 38, 489–498. https://doi.org/10.28940/terra.v38i3.734
Guadalupe-Martínez, G. J., Cárdenas, N. R. y Hernández, O. D. B. (2013). Echinocactus grusonii. The IUCN Red List of Threatened Species 2013: e.T40962A2947851. Recuperado el 29 septiembre, 2025 de: https://dx.doi.org/10.2305/IUCN.UK.2013-1.RLTS.T40962A2947851.en
IBM. (2017). IBM SPSS Estatistics for Windows, version 24.0. IBM Corp. Armonk, USA.
IUSS-WRB (International Union of Soil Sciences-World Reference Base for Soil Resources). (2015). World Reference Base for Soil Resources 2014. Update 2015 International soil classification system for naming soils and creating legends for soil maps. World Soil Resources Reports No. 106. FAO, Rome. Recuperado el 26 septiembre, 2025 de: http://www.fao.org/3/i3794en/I3794en.pdf.
Ivannikov, R., Lobova, O., Ivannikova, N. y Krasnienkova, I. (2022). Micropropagation and organogenesis of Astrophytum asterias (Zucc.) Lem. (Cactaceae Juss.), Blossfeldia liliputiana Werdem. and Strombocactus disciformis (DC.) Britton y Rose. Journal of Microbiology, Biotechnology and Food Sciences, 11, e2201. https://doi.org/10.55251/jmbfs.2201
Jagiello-Kubiec, K., Nowakowska, K., Lukaszewska, A. J. y Pacholczak, A. (2021). Acclimation to ex vitro conditions in ninebark. Agronomy, 11, 612. https://doi.org/10.3390/agronomy11040612
Khalafalla, M. M., Abdellatef, E., Mohameed, A. M. M. y Osman, M. G. (2007). Micropropagation of cactus (Opuntia ficus-indica) as strategic tool to combat desertification in arid and semi arid regions. International Journal of Sustainable Crop Production, 2, 1–8.
Lázaro-Castellanos, J. O., Mata-Rosas, M., González, D. Arias, S. y Reverchon, F. (2018). In vitro propagation of endangered Mammillaria genus (Cactaceae) species and genetic stability assessment using SSR markers. In Vitro Cellular & Developmental Biology – Plant, 54, 518–529. https://doi.org/10.1007/s11627-018-9908-z
Lema-Ruminska, J. y Kulus, D. (2014). Micropropagation of cacti- a review. Haseltonia, 19, 46–63. http://dx.doi.org/10.2985/026.019.0107
Lodé, J. (2014). Kroenleinia gen. nov. J. Lodé: a new genus for a well-known cactus: Echinocactus grusonii. International Cactus Adventures, 102, 25–29.
López-Granero, M., Arana, A., Regalado, G. J. J. y López, E. C. (2021). In vitro mass micropropagation of Mammillatia vetula ssp. gracillis var. Arizonica snowcap. Plant Cell, Tissue and Organ Culture, 155, 759–771. https://orcid.org/10.21203/rs.3.rs-738336/v1
Mabrouk, A., Abbas, Y., El Goumi, Y., El Maaiden. E., El kharrassi, Y., El Antry-Tazi, S. et al. (2021). Optimization of prickly pear cacti (Opuntia spp.) micropropagation using an experimental design method. Journal of Microbiology, Biotechnology and Food Sciences, 11, 1–7. https://doi.org/10.15414/jmbfs.1577
Manzo, R. M. S., González, R. H., García, S. G., García-Moya, E., Espinosa-Hernández, V., Corona, T. T. et al. (2022). Viabilidad y germinación de semillas de cuatro especies amenazadas de cactáceas. Caldasia, 44, 209–220. https://doi.org/10.15446/caldasia.v44n2.86192
Martínez, P. A., Cárdenas, N. R. y Hernández, O. D. B. (2016). Micropropagation of endemic Turbinicarpus valdezianus (Möeller) Glass y Foster (Cactaceae) an endemic cactus in northern Mexico. Horticultural Science, 51, 94–97.
https://doi.org/10.21273/HORTSCI.51.1.94
Martínez, V. Y. M., Andrade, R. M. Villegas, M. A., Tejal, I. A., Villegas, T. O. G. y López, M. V. (2011). Cultivo in vitro del pitayo (Stenocereus stellatus (Pfeiffer) Riccobono). Revista Chapingo Serie Horticultura, 17, 95–105.
Monostori, T., Tanács, L. y Mile, L. (2012). Studies on in vitro propagation methods in cactus species of the genera Melocactus, Cereus and Lobivia. Acta Horticulturae, 937, 255–261. https://doi.org/10.17660/ActaHortic.2012.937.31
Montiel-Frausto, L. B., Enríquez, V. J. R. y Aroldo, C. (2016). Propagación in vitro de Hylocereus monacanthus (Lem.) Britton y Rose. Biotecnología Vegetal, 16, 113–123.
Murashige, T. y Skoog, F. (1962). A revised medium for rapid growth and bioassays with tobacco tissue cultures. Physiologia Plantarum, 15, 473–497. https://doi.org/10.1111/j.1399-3054.1962.tb08052.x
Osuna-Ávila, P., Florez-Margez, J. P. y García-González, D. A. (2025). Efecto de tratamientos pregerminativos y peso de las semillas en la germinación in vitro de Kroenleinia grusonii (Cactaceae). Acta Botanica Mexicana, 132, 2414. https://doi.org/10.21829/abm132.2025.2414
Pérez-Molphe Balch, E., Santos-Díaz, M. S., Ramírez-Malagón, R. y Ochoa-Alejo, N. (2015). Tissue culture of ornamental cacti. Scientia Agricola, 72, 540–561. http://doi.org/10.1590/0103-9016-2015-0012
Pérez-Molphe Balch, E., Pérez-Reyes, M. E., Dávila-Figueroa, C. A. y Villalobos-Amador, E. (2002). In vitro propagation of three species of columnar cacti from the Sonoran Desert. Horticultural Sciences, 37, 639–696. https://doi.org/10.21273/HORTSCI.37.4.693
Ramírez, M. R. y Salazar, S. E. (2016). Propagación y conservación in vitro de siete especies de cactáceas del noreste del estado de Guanajuato. Acta Universitaria Multidisciplinary Scientific Journal, 26, 78–82. áhttp://doi.org/10.15174/au.2016.1540
Rodríguez, A. S. P., Muñoz, O. A., Durán, F. R., Hernández, F. J. Limón, M. J. P. y Hernández-Hernández, H. M. (2021). Micropropagación como alternativa para evitar la extinción de plantas endémicas. Journal of Bioengineering and Biomedicine Research, 5, 1–15.
Ruvalcaba-Ruíz, D., Rojas-Bravo, D. y Valencia-Botín, A. J. (2010). Propagación in vitro de Coryphantha retusa (Britton y Rose) un cactus endémico y amenazado. Tropical and Subtropical Agroecosystems, 12, 139–143.
Santos-Díaz, M. S., Santos-Díaz, M. L. y Alvarado-Rodríguez, J. (2021). In vitro regeneration of the endangered cactus Turbinicarpus mombergeri Riha, a hybrid of T. laui × T. pseudopectinatus. Plant Cell, Tissue and Organ Culture, 148, 271–279. https://doi.org/10.1007/s11240-021-02181-5
Sawsan, S. S. Abou-Dahab, T. A. y Youssef, E. M. A. (2004). In vitro propagation of cactus (Cereus peruvianus L.). Arab Journal of Biotechnology, 8, 196–176.
Semarnat (Secretaría de Medio Ambiente y Recursos Naturales). (2019). Modificación del Anexo Normativo III, Lista de especies en riesgo de la Norma Oficial Mexicana NOM- 059-SEMARNAT-2010, Protección ambiental-Especies nativas de México de flora y fauna silvestres-Categorías de riesgo y especificaciones para su inclusión, exclusión o cambio-Lista de especies en riesgo. Publicada el 30 de diciembre de 2010. Diario Oficial de la Federación. Cd. Mx., México. Recuperado el 25 septiembre, 2025 de: https://www.dof.gob.mx/nota_detalle.php?codigo=5578808&fecha=14/11/2019#gsc.tab=0
Torres-Silva, G., Resende, S. V., Lima-Brito, A., Bezerra, H. B., De Santana, J. R. F. y Schnadelbach, A. S. (2018). In vitro shoot production, morphological alterations and genetic instability of Melocactus glaucescens (Cactaceae), an endangered species endemic to eastern Brazil. South African Journal of Botany, 115, 100–107. https://doi.org/10.1016/j.sajb.2018.01.001
Torres-Silva, G., Selbach, S. A., Basile, B. H., Lima-Brito, A. y Vitória, R. S. (2021). In vitro conservation and genetic diversity of threatened species of Melocactus (Cactaceae). Biodiversity and Conservation, 30, 1067–1080. https://doi.org/10.1007/s10531-021-02132-8
Villavicencio-Gutiérrez, E. E., Quintana-Camargo, M., Sánchez-Barra, F., Cano-Pineda, A. y Ríos-Saucedo, J. C. (2023). Calidad de semillas de dos biznagas del género Echinocactus Tribu Cacteae (Fam.: Cactaceae). Agrofaz, Journal of Environmental and Agroecological Sciences, 5, 8–15.