Characterization and ordination of the Juniperus angosturana scrub in the Mezquital Valley, Hidalgo
Sarahí Flores-Martínez a, Ro Linx Granados-Victorino b, Diódoro Granados-Sánchez a, *, Enrique Guízar-Nolazco a, Alejandro Corona-Ambriz a, Saúl Castañeda-Díaz b y Joaquín Parra-Álvarez c
a Universidad Autónoma Chapingo, División de Ciencias Forestales, Carretera México-Texcoco, Km 38.5, 56230 Chapingo, Texcoco, Estado de México, México
b Universidad Autónoma Chapingo, Área de Biología, Departamento de Preparatoria Agrícola, Carretera México-Texcoco Km 38.5, 56230 Chapingo, Texcoco, Estado de México, México
c Universidad Autónoma Chapingo, Área de Agronomía, Departamento de Preparatoria Agrícola, Carretera México-Texcoco, Km 38.5, 56230 Chapingo, Texcoco, Estado de México, México
*Autor para correspondencia: dgranadoss@chapingo.mx (D. Granados-Sánchez)
Recibido: 13 julio 2025; aceptado: 22 octubre 2025
Resumen
Juniperus angosturana R.P. Adams, es una especie endémica de México que ha sido escasamente estudiada desde una perspectiva ecológica. Su límite sur de distribución geográfica se ubica en el Valle del Mezquital, una región con fuerte presión antrópica. Bajo este contexto, en este estudio se analizó la composición y estructura de las comunidades dominadas por Juniperus angosturana, con el fin de comprender los factores ambientales que influyen en su fisonomía. Para describir la estructura de la vegetación de estas comunidades, se empleó el método de cuadrantes centrados en un punto, mediante el cual se calcularon los valores estructurales de especies arbustivas y arbóreas. La delimitación de asociaciones vegetales se realizó mediante un análisis de agrupamiento. Así mismo, se aplicó un análisis de correspondencias canónicas para evaluar la influencia de variables ambientales y edáficas en la estructura y la composición florística. Como resultados, se identificaron 4 asociaciones dominadas por Juniperus angosturana, cuya diferenciación estructural mostró una alta correlación con las características del suelo, en particular con la textura, concentraciones de calcio, potasio y fósforo, así como con el pH.
Palabras clave: Asociaciones vegetales; Zonas áridas; Sinecología; Enebro; Análisis estructural
Abstract
Juniperus angosturana R.P. Adams is a species endemic to Mexico that has been little studied from an ecological perspective. Its southern geographical distribution limit is located in the Mezquital Valley, a region subject to strong anthropogenic pressure. In this context, this study analyzed the composition and structure of communities dominated by J. angosturana in order to understand the environmental factors that influence their appearance. To describe the vegetation structure of these communities, the point-centered quadrant method was used to calculate the structural values of shrub and tree species. Plant associations were delimited using cluster analysis. Likewise, a Canonical Correspondence Analysis was applied to evaluate the influence of environmental and edaphic variables on the structure and floristic composition. As a result, 4 associations dominated by Juniperus angosturana were identified, whose structural differentiation showed a strong correlation with soil characteristics, particularly texture, calcium, potassium, and phosphorus concentrations, as well as pH.
Keywords: Plant associations; Arid zones; Synecology; Juniper; Structural analysis
Introducción
La vegetación asociada a climas áridos y semiáridos se distribuye en varias regiones que abarcan más de la mitad del territorio mexicano (Pérez-Aguilar et al., 2021). Estas regiones presentan una gran diversidad de matorrales cuya composición y estructura varían de una zona a otra, y son ecosistemas clave para la conservación de la biodiversidad. En todos los tipos de matorrales destacan las formas de vida arbustivas por su dominancia, biomasa y su efecto en el ambiente y otras especies (González-Medrano, 2012; Rzedowski, 2006).
En términos ecológicos las especies de Juniperus L. desempeñan un papel fundamental en las zonas áridas, ya que contribuyen a la formación, protección y retención del suelo (Allegrezza et al., 2016; Romo et al., 2012), así como a la conservación de la biodiversidad al funcionar como refugio o como alimento para la fauna silvestre (Fonseca, 2006). Además, dichas especies facilitan la germinación de semillas de otras plantas al formar sitios seguros de germinación o “islas de recursos” (Miwa y Reuter, 2010; Villanueva-Díaz et al., 2016). Su alta adaptabilidad a condiciones ambientales adversas —como la tolerancia a las sequías, al fuego, a temperaturas extremas o la capacidad de crecer en suelos pobres— las convierte en especies clave para la restauración ecológica (Herrerías y Nieto, 2020).
Juniperus angosturana R.P. Adams (sinónimo: Juniperus monosperma var. gracilis Mart) es una especie arbustiva endémica de México con copas irregulares o redondeadas, que puede alcanzar hasta 2 m de altura y en condiciones idóneas específicas, hasta 7 m. Se desarrolla en regiones de clima templado semiseco, donde forma parte de pastizales, matorrales y bosques bajos escuamifolios (Rzedowski, 2006). Su distribución altitudinal varía entre 1,300 y 2,000 m snm y abarca la fachada occidental de la sierra Madre Oriental desde Coahuila y Nuevo León y el altiplano mexicano en San Luis Potosí y Guanajuato —donde establece asociaciones vegetales con Pinus cembroides Zucc. subsp. cembroides Zucc., particularmente en zonas afectadas por disturbios ecológicos (Estrada-Castillón et al., 2014)— hasta Hidalgo, en el Valle del Mezquital, límite sur de su distribución.
El Valle del Mezquital se ha caracterizado por una intensa actividad humana y cambios en el uso de suelo, lo cual ha provocado una disminución significativa de la cobertura forestal. Entre las causas principales se encuentran el sobrepastoreo, la labranza postcosecha y el manejo inadecuado del suelo agrícola (Hernández-González et al., 2018). Dado que las zonas áridas y semiáridas son especialmente sensibles al disturbio antropogénico (González-Medrano, 2012), es importante conocer la dinámica ecológica de estos matorrales con la finalidad de evitar su degradación progresiva. La caracterización y ordenación de los matorrales dominados por J. angosturana constituye una necesidad para analizar los factores que determinan su estructura y composición florística, a su vez, desarrollar estrategias pertinentes de manejo, conservación y aprovechamiento racional de la especie y de los ecosistemas en los que se encuentra.
El objetivo del presente trabajo fue caracterizar las asociaciones vegetales dominadas por J. angosturana en el Valle del Mezquital, Hidalgo, y por medio de la técnica de ordenación, definir la relación entre la estructura y los factores ambientales y edáficos. El estudio también proporciona bases técnicas y ecológicas para orientar las acciones concretas de conservación y manejo sustentable de los matorrales donde esta especie actúa como elemento estructural dominante.
Materiales y métodos
La presente investigación se realizó en el límite sur de la distribución geográfica de J. angosturana (GBIF, 2023; Natusfera, s.f.; EncicloVida, s.f.). Las localidades de colecta fueron La Florida y San Cristóbal, pertenecientes al municipio Cardonal, ubicado en el Valle del Mezquital, al noreste de Hidalgo (fig. 1), dentro del altiplano central mexicano y de la provincia fisiográfica de la Meseta Neovolcánica, ahora Faja Volcánica Transmexicana (Hernández-Armas, 2016). La zona de estudio se localiza a una altitud promedio de 2,040 m snm, los climas presentes son el templado subhúmedo con lluvias en verano (Cw1), el semiseco templado (BS1kw), semiseco semicálido (BS0hw) y seco semicálido (BS0h). La vegetación de la zona se compone de bosques de pino y encino, matorral xerófilo, pastizales y áreas destinadas a la agricultura (INEGI, 2009, en Guzmán-Cornejo et al., 2015). La precipitación anual promedio es de 409 mm y la temperatura promedio es de 18 °C (Hernández-Armas, 2016).
Se realizaron recolectas botánicas generales estacionales durante los meses de octubre de 2023 y abril, junio, agosto y noviembre de 2024, con la finalidad de obtener muestras de especies perennes y anuales. Los ejemplares recolectados fueron herborizados para su determinación taxonómica mediante el uso de claves especializadas y consultas con expertos, para finalmente ser integrados a colecciones de herbario. En total se revisaron 143 ejemplares recolectados por Enrique Guízar Nolazco (núms. 7981-8123, excepto 7997 y 8022) y Rubén Herrera Flores, depositados en CHAP herbario de la Universidad Autónoma Chapingo, con duplicados de 7981, 7982, 7986, 7992, 7994, 7995, 8015, 8023, 8025, 8027, 8030, 8031, 8039, 8040, 8042, 8045, 8069, 8072, 8076, 8080, 8082, 8083, 8111, 8113, 8114, 8115a y 8119 en UAMIZ herbario de la Universidad Autónoma Metropolitana Unidad Iztapalapa. La nomenclatura de los nombres científicos se basó en la propuesta del International Plant Name Index (IPNI, 2025).
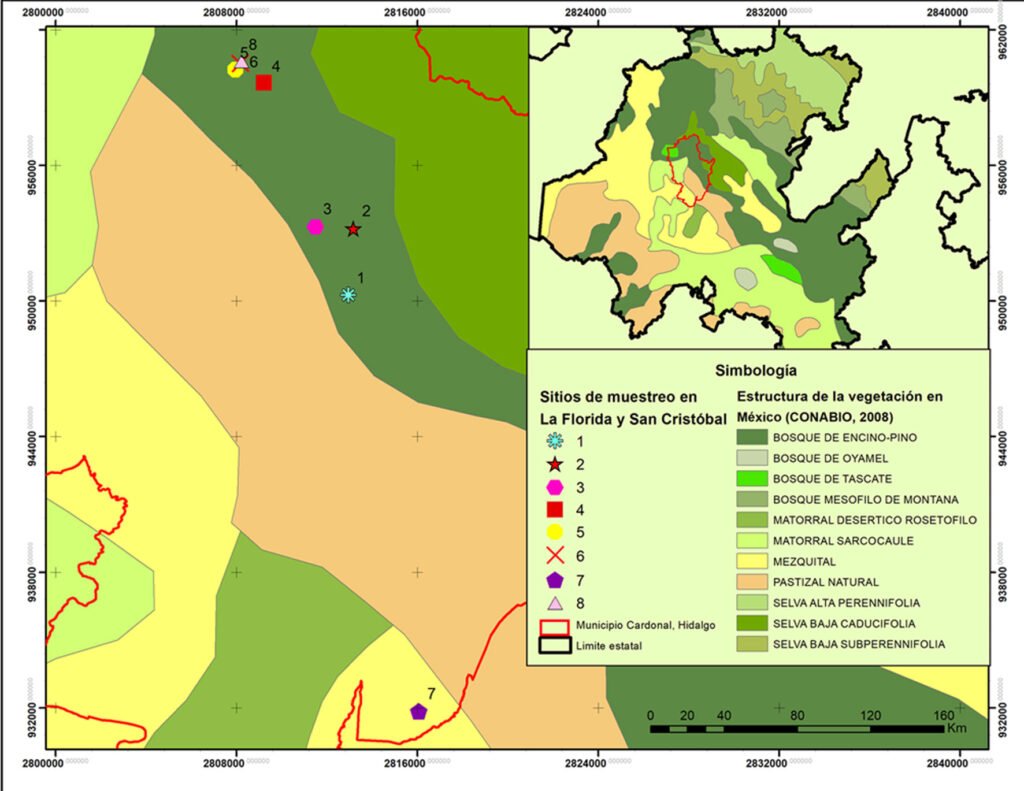
En total se tomaron muestras de 8 sitios, 4 en cada localidad. Para cada sitio se registraron las siguientes variables ambientales: exposición —determinada con una brújula —, pendiente del terreno —medida con un clinómetro Suunto— y altitud —registrada mediante una antena GPS Garmin eTrex 20x. Para determinar las condiciones edáficas, en cada sitio se recolectó una muestra de ~1 kg de suelo, previa remoción de la hojarasca superficial. Posteriormente, se realizaron las siguientes determinaciones: pH, materia orgánica (MO), nitrógeno inorgánico (N inorg.), fósforo asimilable (P), potasio (K), calcio (Ca), hierro (Fe), así como los porcentajes de limo, arena y arcilla, con los que se determinó la textura del suelo (TEX).
Para describir la estructura de la vegetación se utilizó el método de cuadrantes centrados en un punto utilizado por Granados-Victorino et al. (2015), método que no depende de un área delimitada y se basa en las distancias entre puntos fijos y los individuos más cercanos en cada cuadrante. En cada sitio se establecieron 10 puntos de muestreo, con una distancia de 20 m entre sí. En cada punto de muestreo se trazaron, de manera teórica, 4 cuadrantes a partir de ejes perpendiculares (en forma de plano cartesiano). En cada cuadrante se registró la distancia del punto central hasta el árbol o arbusto más cercano con una altura igual o mayor a un metro.
Los individuos registrados fueron identificados taxonómicamente, se midió su altura, con un flexómetro para aquellos individuos menores a 1.50 m y con un clinómetro para especies de porte mayor. Se estimó la cobertura de copa promediando 2 medidas de diámetro de la copa, tomadas en dirección norte-sur y este-oeste. Con los datos obtenidos y siguiendo la metodología propuesta por Cottam y Curtis (1956), modificada por Alanís-Rodríguez et al. (2020), se calcularon los valores relativos de abundancia, dominancia y frecuencia de las especies registradas. A partir de estos parámetros, se estimó el índice de valor de importancia relativa (VIR), el cual permite determinar la relevancia estructural de cada especie en la comunidad.
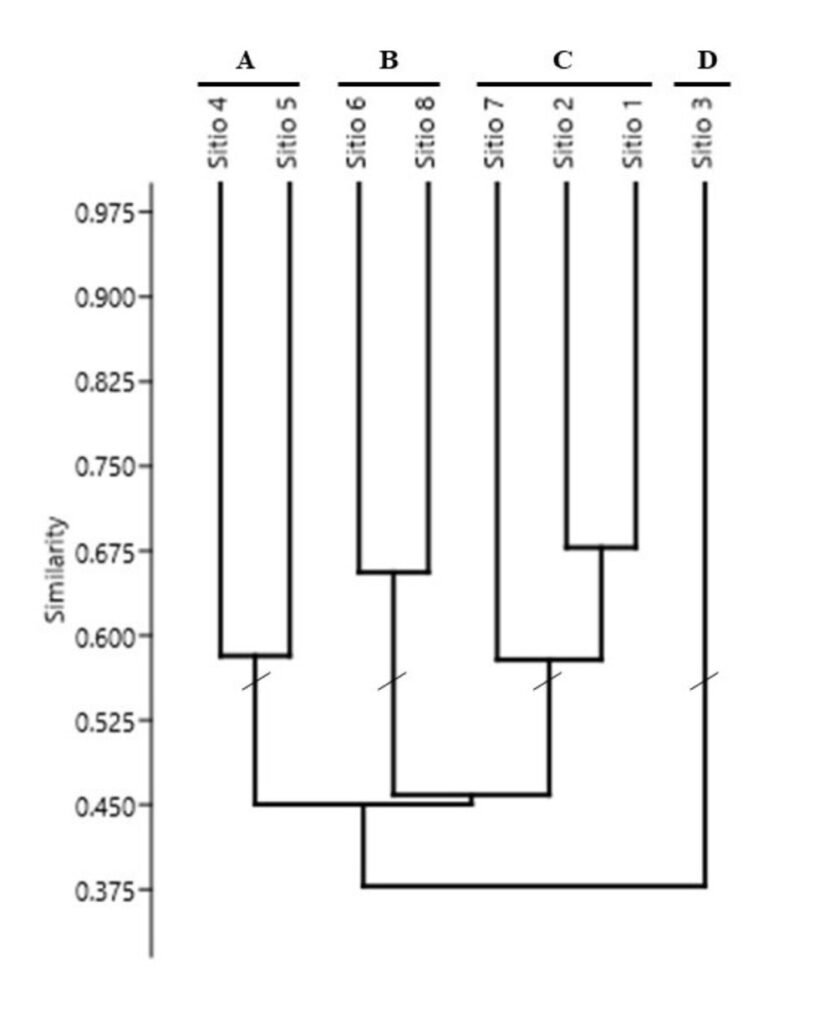
Con base en el VIR de cada especie, se realizó un análisis de agrupamiento utilizando el índice de disimilitud de Bray-Curtis como medida de distancia y el algoritmo de unión por promedio entre grupos (UPGMA). El índice de disimilitud de Bray-Curtis se utiliza para comparar la composición entre sitios e ignora los casos en los que las especies están ausentes, utiliza los valores del VIR (Rocha-Ramírez et al., 2013). A partir de un nivel de corte de 55% de la información retenida en el dendrograma, se identificaron los sitios con mayor semejanza estructural y se definieron las asociaciones vegetales dominantes.
La nomenclatura de las asociaciones vegetales se definió con base en las especies con mayor VIR en los grupos formados a partir del análisis de agrupamiento, así como la fisionomía general de las especies dominantes, de acuerdo con lo sugerido en González-Medrano (2004). Para representar gráficamente la estructura vertical y horizontal de estas asociaciones, se elaboró un perfil semirrealista de la vegetación del transecto de estudio, tomando como base los valores estructurales obtenidos. El análisis de ordenación se realizó mediante un análisis de correspondencias canónicas (ACC), que consiste en una regresión múltiple donde se relacionó el VIR de las especies con las variables ambientales y edáficas registradas. Ambos análisis se llevaron a cabo con el software Past v.4.03 (Hammer et al., 2001).
Resultados
Se identificaron 89 especies en las comunidades vegetales con presencia de Juniperus angosturana en el Valle del Mezquital, que pertenecen a 73 géneros y 41 familias. Las familias más representativas fueron Asteraceae con 10 especies, seguida de Cactaceae y Fabaceae con 8 especies cada una y Asparagaceae con 7. La localidad con mayor riqueza especifica fue La Florida con 72 especies.
Juniperus angosturana se desarrolla principalmente en matorrales, aunque también puede figurar como un elemento importante en los bosques de coníferas de las zonas semiáridas, en especial en aquellos dominados por pinos piñoneros y enebros (Juniperus spp.) (Romme et al., 2009). En las localidades del Valle del Mezquital se reconocieron 4 tipos de vegetación (tabla 1) y 4 asociaciones vegetales con presencia de J. angosturana, las cuales presentan diferencias estructurales y florísticas (figs. 2, 3). A continuación, se describen las características de cada una de dichas asociaciones: a) asociación Juniperus angosturana – Juniperus flaccida Scltdl. Esta asociación vegetal se encuentra en la localidad de San Cristóbal, en específico en los sitios 4 y 5, en altitudes que oscilan entre 1,970 y 2,070 m, con pendiente de 10 a 20% y exposición noroeste. Los suelos son pedregosos, con textura franco-arcillosa, moderadamente alcalinos, con bajo contenido de MO y altas concentraciones de Ca. La comunidad vegetal es codominada por Juniperus angosturana y Juniperus flaccida Schltdl., con VIR de 44% y 31%, respectivamente. Se trata de un bosque con baja densidad arbórea, en el que predominan los individuos de porte bajo que no sobrepasan 4 metros de altura, en cuyos claros es común la presencia de arbustos. Otras especies que se pueden encontrar son Agave lechuguilla Torr., Agave salmiana Otto ex Salm-Dyck var. salmiana, Berberis pallida Benth., Calliandra eriophylla Benth., Cercocarpus fothergilloides Kunth, Chrysactinia mexicana A. Gray, Cylindropuntia imbricata (Haw.) F.M. Knuth, Dalea bicolor Humb. et Bonpl. ex Willd., Dalea greggii A. Gray, Echinocactus platyacanthus Link et Otto, Ferocactus latispinus (Haw.) Britton et Rose, Flourensia resinosa (T. S. Brand.) Blake, Malacomeles denticulata (Kunth) Decne., Mammillaria sp., Milla biflora Cav., Opuntia rastrera F. A. C. Weber, Opuntia robusta H.L. Wendl. ex Pfeiff., Opuntia tomentosa Salm-Dyck, Perymenium mendezii DC., Sanvitalia procumbens Lam., Senna guatemalensis var. hidalgensis H. S. Irwin et Barneby, Thymophylla setifolia Lag., así como algunos individuos de Pinus cembroides Zucc, en las zonas más elevadas (fig. 4A). b) Asociación Juniperus angosturana – Pinus cembroides, se registró en los sitios 6 y 8 de San Cristóbal, entre 1,985 y 2,080 m snm, en pendientes de 10 a 30% y exposición noreste. Juniperus angosturana presentó el VIR más alto con 29%. El estrato arbóreo está compuesto por P. cembroides (21%), J. flaccida (5%) y Pinus pinceana Gordon et Glend (4.6%), conforman un dosel cuya altura varía entre 2 y 6 m. Además de J. angosturana, el estrato arbustivo incluye Ephedra compacta Rose, Rhus schiedeana Schltdl. y Rhus standleyi F.A. Barkley. Asimismo, se registraron especies como Agave lechuguilla, Agave salmiana var. salmiana, Chrysactinia mexicana, Electranthera mutica (DC.) Mesfin, D.J. Crawford et Pruski, Cylindropuntia imbricata, Dalea greggii, Flourensia resinosa, Milla biflora, Opuntia rastrera, Opuntia tomentosa, Perymenium mendezii, Sanvitalia procumbens, y Zinnia peruviana (L.) L. Este matorral se desarrolla sobre suelos pedregosos, con pH alcalino, de textura franco-arcillo-arenosa y con una elevada concentración de Ca y Fe (fig. 4B). c) Juniperus angosturana – Nolina parviflora. En esta asociación vegetal J. angosturana es la especie estructuralmente dominante, con un VIR de 57%. Coexiste con P. cembroides, Nolina parviflora (Kunth) Hemsl, J. flaccida, Dasylirion longissimum Lem., Agave salmiana Otto ex Salm-Dyck var. salmiana, Echinocactus platyacanthus Link et Otto, Ephedra compacta y diversas especies del género Opuntia. El estrato arbustivo no supera los 2 m de altura y en el estrato arbóreo los individuos más grandes llegan a medir hasta 5 m. Esta asociación, se distribuye en La Florida, específicamente en los sitios 1, 2 y 7, en altitudes que van de 1,800 a 2,050 m, en laderas con exposición sureste y pendientes de 7 a 30%. Los suelos son poco desarrollados, cuentan con una delgada capa de hojarasca y fragmentos sueltos de roca; presentan bajo contenido de materia orgánica (8%) y un pH de entre 7 y 8, y son ricos en Ca y K. Otras especies registradas fueron: Agave lechuguilla, Chrysactinia mexicana, Electranthera mutica, Cylindropuntia imbricata, Dahlia coccinea Cav., Dalea bicolor, Flourensia resinosa, Gochnatia hypoleuca (DC.) A. Gray, Lysiloma sp., Mammillaria sp., Milla biflora, Opuntia rastrera, Opuntia tomentosa, Perymenium mendezii DC., Sanvitalia procumbens, Sclerocarpus uniserialis, Thymophylla setifolia y Zinnia peruviana (fig. 4C). d) Juniperus angosturana – Neltuma laevigata, se registró únicamente en un sitio de muestreo, en La Florida, a una altitud promedio de 2,000 m, con una pendiente de 25% y exposición sureste. El suelo presenta una textura fina franco-arcillosa, y una alcalinidad ligera. Según los VIR, Juniperus angosturana es la especie dominante en el estrato arbustivo, con valor de 36% y alturas inferiores de 3 m. En el estrato arbóreo, con un dosel de entre 2 y 6 m de altura, destacan las especies Senegalia berlandieri Benth. y Neltuma laevigata (Humb. y Bonpl. ex Willd.) Britton y Rose,con un VIR conjunto de 25%. Asimismo, se registraron otras especies como Cylindropuntia imbricata, Cylindropuntia leptocaulis (DC.) F.M. Knuth, Milla biflora, Opuntia tomentosa, Jatropha dioica Sessé ex Cerv., Sclerocarpus uniserialis (Hook.) Benth. et Hook. f. ex Hemsl., Senna holwayana (Rose) I. et Barneby, Uncaria tomentosa (Willd. ex Schult.) DC. y Yucca filifera Chabaud (fig. 4D).
Tabla 1. Clasificación de la vegetación en las localidades La Florida y San Cristóbal en Cardonal, Hidalgo, basado en lo propuesto por González-Medrano (2004) para la vegetación de México.
| Categoría | Denominación |
| Tipo de vegetación | Bosque bajo de escuamifolios |
| Asociación | Juniperus angosturana – Juniperus flaccida |
| Tipo de vegetación | Bosque bajo de aciculifolios |
| Asociación | Juniperus angosturana – Pinus cembroides |
| Tipo de vegetación | Matorral mediano rosetófilo |
| Asociación | Juniperus – Nolina parviflora |
| Tipo de vegetación | Bosque bajo espinoso |
| Asociación | Juniperus angosturana – Neltuma laevigata |
Con base en los resultados obtenidos, las especies de mayor importancia ecológica en las asociaciones, además de J. angosturana, son P. cembroides, J. flaccida, Senegalia berlandieri,Neltuma laevigata y Nolina parviflora,las cuales presentaron los valores de importancia relativa más altos en las localidades muestreadas. La dominancia de Juniperus angosturana se atribuye principalmente a su mayor diámetro de copa, más que a su altura, en comparación con las demás especies representativas. La asociación más observada fue la de Pinus cembroides-Juniperus angosturana, seguida de J. angosturana-J. flaccida. Ambas asociaciones vegetales presentan acompañamiento de especies típicas de matorral xerófilo.
La diferenciación estructural de las asociaciones vegetales dominadas por Juniperus angosturana responde a un origen multifactorial y tiene una correlación, principalmente, con las variables edáficas (fig. 5). De acuerdo con el ACC, esta variación es explicada en 67.13% por los 3 primeros ejes (tablas 2, 3). Las variables edáficas más influyentes son la textura del suelo —en especial los porcentajes de arena y limo—, las concentraciones de Ca, K y P, así como el pH del suelo (tabla 2).
Discusión
Juniperus angosturana es una especie endémica de México, cuya distribución se extiende desde Coahuila hasta Hidalgo. A pesar de su relevancia estructural en las zonas áridas del país, ha sido escasamente estudiada desde una perspectiva ecológica. La mayoría de los trabajos publicados se han centrado en análisis filogenéticos (Adams, 1994; Adams y Schwarzbach, 2013; Uckele et al., 2021), en descripciones morfológicas y de distribución geográfica (Estrada-Castillón et al., 2014; Farjon, 2019; González-Elizondo et al., 2012), así como en modelos de distribución potencial o modelados de panbiología (Cartereau, et al., 2023; Morales-Garduño et al., 2021; Trájer, 2023).
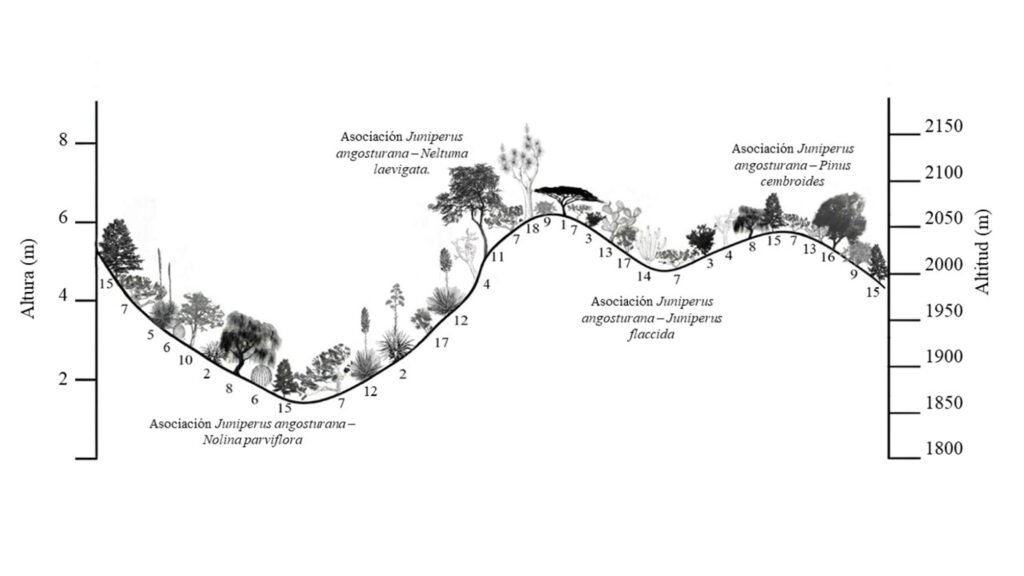

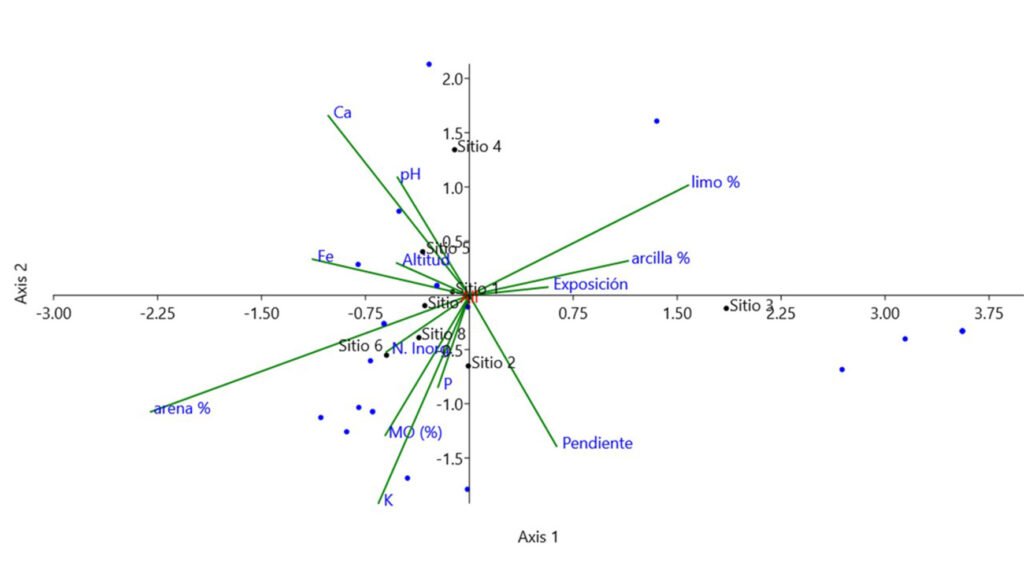
Tabla 2. Resultados de los primeros tres ejes de ordenación, de acuerdo con el análisis de correspondencias canónicas (ACC). Los valores en negritas señalan las variables con mayor peso en la definición de cada eje.
| Variable | Eje 1 | Eje 2 | Eje 3 |
| pH | -0.172893 | 0.36276 | 0.658303 |
| MO (%) | -0.202071 | -0.429806 | -0.215268 |
| N inorg. | -0.199503 | -0.173747 | 0.0472623 |
| P | -0.0753286 | -0.282118 | -0.700757 |
| K | -0.218424 | -0.638471 | -0.248518 |
| Ca | -0.339255 | 0.552029 | -0.00914643 |
| Fe | -0.377003 | 0.110919 | -0.443264 |
| arena (%) | -0.766368 | -0.357859 | 0.0899592 |
| limo (%) | 0.526614 | 0.338468 | 0.363971 |
| arcilla (%) | 0.381808 | 0.105922 | -0.377697 |
| Pendiente | 0.20969 | -0.463599 | 0.177899 |
| Exposición | 0.18856 | 0.0252954 | -0.295587 |
| Altitud | -0.174418 | 0.0991923 | -0.140028 |
| Distribución de la varianza | |||
| Valor propio | 0.521 | 0.364 | 0.318 |
| Varianza (%) | 29.07 | 20.3 | 17.76 |
| Varianza acumulada (%) | 29.07 | 49.37 | 67.13 |
Tabla 3. Matriz de correlación entre las variables ambientales y edáficas de los sitios de muestreo en Cardonal, Hidalgo. La parte superior derecha muestra los valores del coeficiente de correlación (r) y la diagonal inferior izquierda los valores de p (< 0.05)
| pH | MO (%) | N (inorgánico) | P | K | Ca | Fe | arena % | limo % | arcilla % | Pendiente | Exposición | |
| pH | -0.06 | -0.26 | -0.43 | -0.67 | -0.09 | -0.17 | -0.23 | -0.01 | 0.24 | -0.04 | -0.53 | |
| MO (%) | 0.85 | -0.56 | 0.75 | 0.56 | -0.06 | 0.57 | 0.3 | -0.69 | 0.24 | -0.07 | -0.58 | |
| N (Ing) | 0.39 | 0.05 | -0.55 | 0.11 | -0.12 | -0.12 | 0.27 | 0.37 | -0.56 | 0.04 | 0.22 | |
| P | 0.14 | 0.00 | 0.05 | 0.42 | -0.09 | 0.39 | 0.16 | -0.77 | 0.44 | 0.11 | -0.08 | |
| K | 0.01 | 0.05 | 0.72 | 0.15 | 0.21 | 0.48 | 0.63 | -0.22 | -0.48 | -0.14 | 0.01 | |
| Ca | 0.77 | 0.85 | 0.70 | 0.77 | 0.49 | 0.47 | 0.31 | 0.25 | -0.51 | -0.71 | 0.17 | |
| Fe | 0.58 | 0.04 | 0.70 | 0.19 | 0.10 | 0.11 | 0.21 | -0.24 | -0.04 | -0.77 | -0.40 | |
| arena % | 0.45 | 0.32 | 0.37 | 0.60 | 0.02 | 0.30 | 0.49 | -0.42 | -0.71 | -0.08 | -0.09 | |
| limo % | 0.97 | 0.01 | 0.21 | 0.00 | 0.47 | 0.41 | 0.43 | 0.15 | -0.34 | -0.29 | 0.31 | |
| arcilla % | 0.43 | 0.43 | 0.05 | 0.13 | 0.10 | 0.07 | 0.90 | 0.01 | 0.26 | 0.13 | -0.15 | |
| Pendiente | 0.90 | 0.82 | 0.90 | 0.72 | 0.65 | 0.01 | 0.002 | 0.80 | 0.34 | 0.67 | 0.08 | |
| Exposición | 0.06 | 0.04 | 0.47 | 0.80 | 0.97 | 0.58 | 0.18 | 0.77 | 0.30 | 0.62 | 0.80 | |
| Altitud | 0.23 | 0.21 | 0.00 | 0.07 | 0.32 | 0.80 | 0.82 | 0.70 | 0.02 | 0.02 | 0.60 | 0.95 |
En cuanto al hábitat de J. angosturana y las comunidades vegetales de las que forman parte, Estrada-Castillón et al. (2015) asocian la especie con ecotonos entre pastizales halófitos y bosques de pino piñonero en la región centro-sur de Nuevo León y el norte de Tamaulipas. De manera similar, Salinas-Rodríguez et al. (2013) reporta su presencia en el ecotono entre chaparrales de encino (Quercus spp.) y bosques de Pinus cembroides en el cañón de Iturbide, Nuevo León.
En Hidalgo, J. angosturana se desarrolla principalmente en la zona de transición entre el bosque de pino piñonero y el matorral rosetófilo. Lo anterior sugiere que es una especie ecotonal, con ventajas competitivas en los límites de la distribución de las asociaciones vegetales circundantes, es decir, en los márgenes de tolerancia física y competitiva de otras especies (Ortiz-Colín y Hulshof, 2024). Su relevancia estructural disminuye conforme se adentra en ecosistemas más homogéneos; sin embargo, se registraron matorrales dominados por J. angosturana, lo que indica una amplia tolerancia ecológica, tanto en términos edáficos como de humedad, temperatura y exposición solar. Esto refuerza su papel como especie clave en zonas de transición y como posible estabilizador ecológico en ambientes semiáridos.
Los matorrales dominados por J. angosturana forman un hábitat heterogéneo, que incluye microhábitats favorables bajo el dosel de los individuos, gracias a su amplia ramificación y extensión de copa. Esta estructura proporciona protección de la radiación solar y facilita la retención de suelo y humedad que beneficia a numerosas especies asociadas. No obstante, debido a los grandes volúmenes de enraizamiento de los arbustos, los espacios intermedios entre individuos suelen presentar escasa vegetación (Chambers et al., 1999; Rostamikia et al., 2024). Dicha configuración espacial da lugar a un mosaico ecológico conocido como islas de fertilidad o islas de recursos, que son esenciales para el mantenimiento de la biodiversidad en los ecosistemas áridos y semiáridos (Magaña et al., 2023).
En el Valle del Mezquital, la asociación más frecuente con presencia de Juniperus angosturana se presentó en los bosques de piñón-enebro, lo que evidencia una clara coexistencia con P. cembroides. No obstante, es necesario intensificar los estudios para confirmar si este patrón se mantiene en otras regiones. Romme et al. (2009) mencionan la presencia de 3 variantes para esta asociación: bosques persistentes de piñón-enebro, matorrales boscosos de piñón-enebro y sabanas de piñón-enebro, de los cuales solo los primeros 2 fueron registrados en el Valle del Mezquital, lo cual indica una alta variación estructural y ecológica.
En México, la asociación piñón-enebro se ha reportado en zonas de transición en regiones semiáridas. A pesar de su similitud estructural, existe una clara diferenciación florística regional y solo se había documentado la presencia de J. angosturana en Nuevo León, ahora se reporta también en Hidalgo. Por ejemplo, Parra-Álvarez et al. (2022) identificaron en la región central de San Luis Potosí, una asociación integrada por 5 especies de pinos piñoneros (Pinus cembroides, P. pinceana, P. nelsonii, P. discolor y P. johannis) y Juniperus flaccida. De forma similar, Granados-Victorino et al. (2015) reportaron esta asociación en la zona árida poblano-veracruzana, donde Pinus cembroides subsp. orizabensis D.K. Bailey codomina con J. flaccida o J. deppeana Steud; de la Fuente Solís et al. (2025) describen un bosque caracterizado por la asociación Pinus cembroides y Juniperus monosperma (Engelm.) Sarg. en Galeana, Nuevo León.
Baker y Shinneman (2004) señalan que estos bosques están aumentando en densidad y expandiéndose hacia los matorrales y pastizales adyacentes, los cuales frecuentemente se consideran ecosistemas en proceso de degradación. Se ha documentado que la remoción de individuos de Pinus o Juniperus puede favorecer el incremento de cobertura de gramíneas (Almalki et al., 2023), lo que representa un beneficio potencial para la ganadería. Sin embargo, esta práctica tiene efectos negativos en la biodiversidad debido a que los árboles y arbustos de las zonas áridas y semiáridas proporcionan sitios seguros de germinación, así como refugio y hábitat para numerosas especies (Allegrezza et al., 2016).
Por medio del ACC se determinó que la textura del suelo, en particular los porcentajes de arena y limo, constituye uno de los principales factores que explican la diferenciación estructural entre la vegetación de los sitios analizados. La proporción relativa de arena, limo y arcilla influye directamente en la fertilidad del suelo, pues regula la retención de humedad y la disponibilidad de nutrientes esenciales para las plantas. Los suelos con textura arenoso-limosa, al presentar baja capacidad de retención de agua y de intercambio catiónico, favorecen el desarrollo de especies adaptadas a ambientes con pulsos breves de humedad (Rostamikia et al., 2024). Por lo tanto, el gradiente de textura puede inducir un recambio en la composición vegetal, puesto que refleja la capacidad diferencial de las especies para tolerar condiciones edáficas restrictivas.
Las variaciones en la textura podrían deberse a la erosión eólica e hídrica provocadas por las diferencias en la exposición, la pendiente y la abundancia de las especies vegetales (Shukla et al., 2006). Por ejemplo, en el desierto chihuahuense, las diferencias estructurales en las asociaciones vegetales se presentan debido a los ligeros cambios en la orografía, la elevación, el ángulo de la pendiente, la rocosidad y las variables edáficas en la distribución de las plantas en ambientes áridos (Estrada-Castillón et al., 2015; Granados-Sánchez et al., 2011).
En el Valle del Mezquital, las asociaciones vegetales dominadas por especies del género Juniperus, como los bosques de enebro y los matorrales submontanos de Juniperus angosturana, se desarrollan sobre suelos de origen calcáreo, con pH alcalino y altos contenidos de Fe, características típicas de zonas áridas donde la escasez de agua limita los procesos de lixiviación, además de generar la formación de costras de carbonatos o de yesos (Hag Husein et al., 2021). Diversas especies del género Juniperus han sido reconocidas por su notable capacidad de adaptación a suelos pobres en nutrientes, poco profundos y con baja retención de humedad. Además, presentan una respuesta eficiente ante cambios ambientales, así como una alta tolerancia al fuego y a perturbaciones de origen antrópico (Cuevas-Guzmán et al., 2023; Rosas-Chavoya et al., 2016).
De forma general, las variantes estructurales de las comunidades dominadas por J. angosturana está influenciada por la textura del suelo, la disponibilidad de nutrientes y el pH, que suele ser alcalino y en menor medida, la pendiente del terreno. Por ejemplo, la asociación Juniperus angosturana-Pinus cembroides se desarrolla en suelos poco profundos con alto contenido de arena, pH ligeramente alcalino y mayor contenido de materia orgánica y, por ende, una mayor disponibilidad de nutrientes respecto a las demás asociaciones analizadas. En contraste, la asociación de matorral de Juniperus angosturana–Nolina parviflora se presentan en suelos con texturas más finas, que retienen mejor el agua superficial, sin embargo, muestran baja acumulación de materia orgánica y mayor exposición solar, lo que genera condiciones edáficas más restrictivas para el desarrollo arbóreo.
El presente estudio representa una contribución significativa al conocimiento ecológico de J. angosturana al proporcionar información básica sobre su hábitat y las asociaciones vegetales que conforma. Los resultados confirman que es una especie ecotonal, cuya plasticidad ambiental le permite establecerse y adaptarse a condiciones edáficas y climáticas variables en zonas de transición entre bosques de pino piñonero y matorral rosetófilo. La presencia de J. angosturana en Hidalgo, relativamente lejos de su distribución previamente conocida, amplía el conocimiento sobre su rango ecológico y florístico, y subraya la necesidad de llevar a cabo más estudios regionales, con un enfoque en la restauración de dichos ecotonos.
Además, su hábito de crecimiento y cobertura favorecen la generación de islas de fertilidad, promueven la biodiversidad y contribuyen a la conectividad del paisaje al conformar corredores biológicos, que facilitan el flujo de especies entre ecosistemas fragmentados. La identificación de su preferencia por suelos de textura arenoso-limosa y de origen calcáreo, así como de la coocurrencia con P. cembroides en el Valle del Mezquital, aporta elementos clave para comprender la dinámica y la diferenciación florística de los ecosistemas áridos y semiáridos donde se desarrolla J. angosturana.
En conjunto, los resultados obtenidos en este trabajo constituyen una base técnica y ecológica sólida para orientar estrategias de conservación y manejo de matorrales donde J. angosturana actúa como especie estructuralmente dominante. La identificación de los factores edáficos y ambientales que determinan su distribución, así como el reconocimiento de las especies vegetales que la acompaña, proporcionan información fundamental para el diseño de acciones de restauración ecológica y el manejo adaptativo de los ecosistemas semiáridos donde esta especie se desarrolla.
Agradecimientos
Los autores agradecen a la Universidad Autónoma Chapingo, en particular a la Dirección General de Investigación, Posgrado y Servicio y a la División de Ciencias Forestales, por las facilidades y el apoyo institucional brindados para la realización de esta investigación; a la Secretaría de Ciencia, Humanidades, Tecnología e Innovación (Secihti) por la beca de posgrado número 4008144 otorgada a la primera autora durante el desarrollo de estos estudios. A los compañeros, Diego Carrillo Martínez, Ruth del Cid, así como al técnico Rubén Herrera Flores por su apoyo en el trabajo de campo y a Ana Rosa López Ferrari por su apoyo en la identificación taxonómica de algunos ejemplares en el Herbario UAMIZ. Finalmente, se agradecen las valiosas sugerencias y observaciones de los revisores, que contribuyeron significativamente a mejorar el contenido de este escrito.
Referencias
Adams, R. P. (1994). Geographic variation and systematics of monospermous Juniperus (Cupressaceae) from the Chihuahua Desert based on RAPD’s and terpenes. Biochemical Systematics Ecology, 22, 699–710. https://doi.org/10.1016/03051978(94)90056-6
Adams, R. P. y Schwarzbach, A. E. (2013). Taxonomy of the serrate leaf Juniperus of North America: phylogenetic analyses using nrDNA and four cpDNA regions. Phytologia, 95, 172–178.
Alanis-Rodríguez, E., Mora-Olivo, A. y Marroquín-de la Fuente, J. (2020). Muestreo ecológico de la vegetación. Monterrey, México: Universidad Autónoma de Nuevo León.
Allegrezza, M., Corti, G., Cocco, S., Pesaresi, S., Chirico, G. B., Saracino, A. et al. (2016). Microclimate buffering and fertility island formation during Juniperus communis ontogenesis modulate competition-facilitation balance. Journal of Vegetation Science, 27, 616–627. https://doi.org/10.1111/jvs.12386
Almalki, Y. M., Fernald, A. G., Ochoa, C. G., Cibils, A. F., Faist, A. M., Cram, D. S. et al. (2023). Understory vegetation response to thinning pinyon-juniper woodlands. Rangeland Ecology & Management, 88, 152–158. https://doi.org/10.1016/j.rama.2023.02.012
Baker, W. L. y Shinneman, D. J. (2004). Fire and restoration of piñon-juniper woodlands in the western United States. Forest Ecology and Management, 189, 1–21. https://doi.org/10.1016/j.foreco.2003.09.006
Cartereau, M., Leriche, A., Médail, F. y Baumel, A. (2023). Tree biodiversity of warm drylands is likely to decline in a drier world. Global Change Biology, 29, 3707–3722. https://doi.org/10.1111/gcb.16722
Chambers, J. C., Vander Wall, S. B. y Schupp, E. W. (1999). Ecología de semillas y plántulas de especies de piñón y enebro en los bosques pigmeos del oeste de Norteamérica. Botanical Review, 65, 1–38. https://doi.org/10.1007/BF02856556
Cottam, G. y Curtis, J. T. (1956). The use of distance measurements in phytosociological sampling. Ecology, 37, 451–460. https://doi.org/10.2307/1930167
Cuevas-Guzmán, R., Canales-Piña, S., Sánchez-Rodríguez, E. V., Morales-Arias, J., Guzmán-Hernández, L. y Núñez-López, N. M. (2023). Atributos estructurales y hábitat de Juniperus jaliscana en Talpa de Allende, Jalisco, México. Botanical Sciences, 101, 670–684. https://doi.org/10.17129/botsci.3235
EncicloVida. (s. f.). Enebro chino. EncicloVida. Recuperado el 16 abril, 2024 de: https://enciclovida.mx/especies/155214
Estrada-Castillón E., Arévalo, J. R., Villarreal-Quintanilla, J. Á., Salinas-Rodríguez, M. M., Cantú-Ayala, C. M., González-Rodríguez, H. et al. (2014). Coníferas de Nuevo León, México. Nuevo León, México: Universidad Autónoma de Nuevo León.
Estrada-Castillón E., Arévalo, J. R., Villarreal-Quintanilla, J. Á., Salinas-Rodríguez, M. M., Encina-Domínguez, J. A., González-Rodríguez, H. et al. (2015). Classification and ordination of main plant communities along an altitudinal gradient in the arid and temperate climates of northeastern Mexico. The Science of Nature, 102, 9–10. https://doi.org/10.1007/s00114-015-1306-3
Farjon, A. (2019). Juniperus angosturana. Threatened Conifers of the World. https://threatenedconifers.rbge.org.uk/conifers/juniperus-angosturana
Fonseca, R. M. (2006). Juniperus, la ginebra, el incienso, los lápices y los repelentes. Ciencias, 81, 44–47.
Fuente-Solís, A. M., Alanís-Rodríguez, E., Yáñez-Díaz, M. I., Córdova-Silva, I., Himmelsbach, W. y Martínez del Campo-Delgado, Á. M. (2025). Analysis of the natural regeneration of a temperate arid forest in northeastern Mexico. Revista Forestal Mesoamericana Kurú, 22, 1–10. https://doi.org/10.18845/rfmk.v22i50.7755
GBIF Secretariat.(2023). Juniperus angosturana R. P. Adams. GBIF Backbone Taxonomy. https://doi.org/10.15468/39omei
González-Elizondo, M. S., González-Elizondo, M., Tena-Flores, J. A., Ruacho-González, L. y López-Enríquez, I. (2012). Vegetación de la sierra Madre Occidental, México: una síntesis. Acta Botanica Mexicana, 100, 351–403. https://doi.org/10.21829/abm100.2012.40
González-Medrano, F. (2004). Las comunidades vegetales de México. Propuesta para la unificación de la clasificación y nomenclatura de la vegetación de México, 2ª ed. México D.F.: Instituto Nacional de Ecología, Semarnat. https://www.academia.edu/16702033/Vegetacion_de_mexico_gonzalez
González-Medrano, F. (2012). Las zonas áridas y semiáridas de México y su vegetación. México D.F.: Instituto Nacional de Ecología, Semarnat. http://140.84.163.2:8080/xmlui/bitstream/handle/publicaciones/218/668_2012_Zonas_aridas_semiaridas_Mexico.pdf?sequence=1etisAllowed=y
Granados-Sánchez, D., Sánchez-González, A., Granados-Victorino, R. L. y Borja-de la Rosa, A. (2011). Ecología de la vegetación del desierto chihuahuense. Revista Chapingo Serie Ciencias Forestales y del Ambiente, 17, 111–130. https://doi.org/10.5154/r.rchscfa.2010.10.102
Granados-Victorino, R. L., Granados-Sánchez, D. y Sánchez-González, A. (2015). Caracterización y ordenación de los bosques de pino piñonero (Pinus cembroides subsp. orizabensis) de la cuenca oriental (Puebla, Tlaxcala y Veracruz). Madera y Bosques, 21, 23–42. https://doi.org/10.21829/myb.2015.212443
Guzmán-Cornejo, L., Sánchez Morales, A. y Pacheco, L. (2015). Helechos y licofitas del municipio de Cardonal, Hidalgo, México. Revista Mexicana de Biodiversidad, 86, 573–581. https://doi.org/10.1016/j.rmb.2015.06.004
Hag Husein, H., Lucke, B., Bäumler, R. y Sahwan, W. A. (2021). Contribution to soil fertility assessment for arid and semi-arid lands. Soil Systems, 5, 1–13. https://doi.org/10.3390/soilsystems5030042
Hammer, O., Harper, D. y Ryan, P. (2001). PAST: Paleontological Statistics Software Package for Education and Data Analysis. Paleontología Electrónica, 4, 1–9. https://www.researchgate.net/publication/259640226_PAST_Paleontological_Statistics_Software_Package_for_Education_and_Data_Analysis
Hernández-Armas, C. (2016). Otomíes del Valle del Mezquital: retos ante la preservación o la transformación de una cul-
tura. Divulgare. Boletín Científico de la Escuela Superior de Actopan, 3. https://doi.org/10.29057/esa.v3i5.1645
Hernández-González, D. E., Muñoz Iniestra, D. J., López Galindo, F. y Hernández Moreno, M. M. (2018). Impacto del uso de la tierra en la calidad del suelo en una zona semiárida del Valle del Mezquital, Hidalgo, México. BIOCYT Biología Ciencia y Tecnología, 11, 792–807. https://doi.org/10.22201/fesi.20072082.2018.11.65833
Herrerías, M. L. G. y Nieto, P. P. (2020). Características estructurales y demográficas de Juniperus deppeana Steud. en 2 localidades del estado de Tlaxcala. Revista Mexicana de Ciencias Forestales, 11, 124–151. https://doi.org/10.29298/rmcf.v11i61.618
IPNI (International Plant Names Index). (2025). The Royal Botanic Gardens, Kew, Harvard University Herbaria et Libraries y Australian National Herbarium. Recuperado el 24 Febrero, 2025 de: http://www.ipni.org
Natusfera. (s. f.). Enebro chino(Juniperus angosturana). Natusfera. Recuperado el 16 abril, 2024 de: https://spain.inaturalist.org/taxa/135936-Juniperus-angosturana
Magaña Ugarte, R., Gavilan, R. G. y Rubio, A. (2023). Assessing the occurrence of soil improvement and its relationship to the dominant life form in the high mountains of Central Spain. Geoderma Regional, 36, 1–11. https://doi.org/10.1016/j.geodrs.2023.e00744
Miwa, C. T. y Reuter, R. J. (2010). Persistence of western juniper (Juniperus occidentalis) resource islands following canopy removal. Northwest Science, 84, 361–368. https://doi.org/10.3955/046.084.0405
Morales-Garduño, L., Solano, E., Villaseñor, J. L. y Montaño-Arias, G. (2021). Panbiogeografía de los matorrales de la región xerofítica mexicana. Botanical Sciences, 99, 611–627. https://doi.org/10.17129/botsci.2773
Ortiz-Colin, P. y Hulshof, C. (2024). Ecotones as windows into organismal-to-biome scale responses across neotropical forests. Plants, 13, 2396. https://doi.org/10.3390/plants13172396
Parra-Álvarez, J., Granados-Sánchez, D., Granados-Victorino, R. L. y Villanueva-Morales, A. (2022). Caracterización estructural y clasificación de los bosques piñoneros de San Luis Potosí, México. Revista Chapingo Serie Ciencias Forestales y del Ambiente, 29, 61–98. https://doi.org/10.5154/r.rchscfa.2022.03.021
Pérez-Aguilar, L. Y., Plata-Rocha, W., Monjardín-Armenta, S. A., Franco-Ochoa, C. y Zambrano-Medina, Y. G. (2021). The identification and classification of arid zones through multicriteria evaluation and geographic information systems —case study: arid regions of northwest Mexico. ISPRS. International Journal of Geo-information, 10, 720. https://doi.org/10.3390/ijgi10110720
Portal de Geoinformación. (2023). Carta fisonómica-estructural de la vegetación de México. Comisión Nacional para el Conocimiento y Uso de la Biodiversidad Recuperado el 27 enero, 2025 de: http://www.conabio.gob.mx/informacion/gis/?vns=gis_root/usv/otras/vpotbt4mgw
Richards, P. (1952). The tropical rain forest an ecological study. Cambridge: Cambridge University Press.
Rocha-Ramírez, A., Chávez-López, R., Ramírez-Rojas, A. y Cházaro-Olvera, S. (2013). Comunidades. Métodos de estudios. México D.F.: Facultad de Estudios Superiores Iztacala, Universidad Nacional Autónoma de México.
Romme, W. H., Allen, C. D., Bailey, J. D., Baker, W. L., Bestelmeyer, B. T., Brown, P. M. et al. (2009). Historical and modern disturbance regimes, stand structures, and landscape dynamics in piñon-juniper vegetation of the western United States. Rangeland Ecology and Management, 62, 203–222. https://doi.org/10.2111/08-188R1
Romo, A., Salvá, C. M., Ouhammou, A. y Boratyński, A. (2012). Las formaciones de Sabina albar (Juniperus thurifera subsp. africana) en los macizos de Toubkal y Azourki del gran Atlas (Marruecos). VII Congreso Español de Biogeografía, 379-383. https://digital.csic.es/bitstream/10261/64701/1/formaciones_sabina_albar.pdf
Rosas-Chavoya, M., Granados-Sánchez, D., Granados-Victorino, R. L. y Esparza-Govea, S. (2016). Clasificación y ordenación de bosques de pino piñonero del estado de Querétaro. Revista Mexicana de Ciencias Forestales, 7, 52–73. https://doi.org/10.29298/rmcf.v7i33.90
Rostamikia, Y., Matinizadeh, M. y Anbaran S. M. (2024). Influence of scattered greek juniper trees on soil properties in semi-arid woodlands in the northwest of Iran. Journal of Forest Science, 70, 560–573. https://doi.org/10.17221/60/2024-jfs
Rzedowski, J. (2006). Vegetación de México. Comisión Nacional para el Conocimiento y Uso de la Biodiversidad. -https://www.biodiversidad.gob.mx/ecosistemas/vegetaciondeMexico
Salinas-Rodríguez, M. M., Estrada-Castillón, E. y Villarreal-Quintanilla, J. Á. (2013). Flora and phytogeography of the Cañón de Iturbide, Nuevo León, México. Journal of the Botanical Research Institute of Texas, 7, 803–819.
Shukla, M. K., Lal, R., Ebinger, M. y Meyer, C. (2006). Physical and chemical properties of soils under some piñon-juniper-oak canopies in a semi-arid ecosystem in New Mexico. Journal of Arid Environments, 66, 673–685. https://doi.org/10.1016/j.jaridenv.2005.12.002
Trájer, A. J. (2023). Clarification of the Lopingian palaeo climatic conditions of the northwestern coastal regions of Palaeotethys based on the transdanubian geological record. Review of Palaeobotany and Palynology, 316, 104917. https://doi.org/10.1016/j.revpalbo.2023.104917
Uckele, K. A., Adams, R. P., Schwarzbach, A. E. y Parchman, T. L. (2021). Genome-wide RAD sequencing resolves the evolutionary history of serrate leaf Juniperus and reveals discordance with chloroplast phylogeny. Molecular Phylogenetics and Evolution, 156, 107022. https://doi.org/10.1016/j.ympev.2020.107022
Villanueva-Díaz, J., Vázquez-Selem, L., Gómez-Guerrero, A., Cerano-Paredes, J., Aguirre-González, N. A. y Franco-Ramos, O. (2016). Potencial dendrocronológico de Juniperus monticola Martínez en el monte Tláloc, México. Revista Fitotecnia Mexicana, 39, 175–185. https://doi.org/10.35196/rfm.2016.2